никита хрущев пенсионер союзного значения хрущев с
![EVO [универсальный солдат] мусс особого значения macgyver multi-use mousse](https://www.letu.ru/common/img/pim/2023/09/GT_4d2a3bf3-c6f6-47b1-aa77-f68057f55101.jpg)
Модель:
RUR 4030
EVO [универсальный солдат] мусс особого значения macgyver multi-use mousse Муссы для волос
Модель:
RUR 230
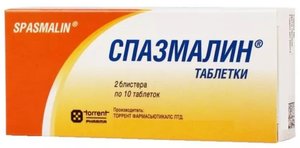
Показания Болевой синдром (слабо или умеренно выраженный) при спазмах гладкой мускулатуры внутренних органов: почечная колика, спазм мочеточника и мочевого пузыря: желчная колика, кишечная колика: дискинезия желчевыводящих путей, постхолецистэктомический синдром, хронический колит: альгодисменорея. Для кратковременного лечения: артралгия, миалгия, невралгия, ишиалгия.В качестве вспомогательного лекарственного средства: заболевания органов малого таза, болевой синдром после хирургических вмешательств и диагностических процедур. Противопоказания Противопоказания Гиперчувствительность (в т.ч. к производным пиразолона), угнетение костномозгового кроветворения, выраженная печеночная и/или почечная недостаточность, дефицит глюкозо-6-фосфатдегидрогеназы, тахиаритмии, тяжелая стенокардия, декомпенсирован- ная хроническая сердечная недостаточность, закрытоугольная глаукома, гиперплазия предстательной железы (с клиническими проявлениями), кишечная непроходимость, мегаколон, коллапс, беременность, период кормления грудью, детский возраст (до 8 лет). С осторожностью: Почечная/печеночная недостаточность, бронхиальная астма, склонность к артериальной гипотензии, гиперчувствительность к нестероидным противовоспалительным препаратам: полное или неполное сочетание бронхиальной астмы, полипоза носа и непереносимости ацетилсалициловой кислоты и других нестероидных противовоспалительных препаратов. Беременность противопоказано Применение и дозы Внутрь: взрослые и подростки старше 15 лет: 1-2 таблетки 2-3 раза в сутки, не разжевывая, запивая небольшим количеством жидкости. Суточная доза не должна превышать 6 таблеток. Продолжительность приема не более 5 дней. Дега 12-14 лет: разовая доза - 1 таблетка, максимальная суточная доза - 6 таблеток (1.5 таблетки 4 раза в сутки), 8-11 лет - 0.5 таблетки, максимальная суточная доза - 4 таблетки (по 1 таблетке 4 раза в сутки). Побочные эффекты и передозировка Побочные эффекты: Аллергические реакции: крапивница (в т.ч. на конъюнктиве и слизистых оболочках носоглотки), ангионевротический отек, в редких случаях - злокачественная экссудативная эритема (синдром Стивенса-Джонсона), токсический эпидермальный некролиз (синдром Лайелла), бронхоспастический синдром, анафилактический шок. Со стороны мочевыделительной системы: нарушение функции почек, олигурия, анурия, протеинурия, интерстициальный нефрит, окрашивание мочи в красный цвет. Со стороны сердечно-сосудистой системы: снижение артериального давления. Со стороны органов кроветворения: тромбоцитопения, лейкопения, агранулоцитоз (может проявляться следующими симптомами: немотивированный подъем температуры, озноб, боль в горле, затруднение глотания, стоматит, а также развитие явлений вагинита или проктита). Антихолинергические эффекты: сухость во рту, пониженное потоотделение, парез аккомодации, тахикардия, затрудненное мочеиспускание. Передозировка: Симптомы: рвота, снижение артериального давления, сонливость, спутанность сознания, тошнота, боли в эпигастральной области, нарушения функции печени и почек, судороги. Лечение: промывание желудка, прием активированного угля, симптоматическая терапия. Взаимодействие с другими ЛС: При совместном применении с блокаторами Н1-гнетаминовых рецепторов, производными бутирофенона и фенотиазина, трициклическими антидепрессантами, амантадином и хинидином возможно усиление м-холиноблокирующего действия. Метамизол натрия усиливает эффекты этанола: одновременное применение с хлорпромазином или другими производными фенотиазина может привести к развитию выраженной гипертермии. Трициклические антидепрессанты, пероральные контрацептивы и аллопуринол повышают токсичность препарата. Фенилбутазон, барбитураты и другие индукторы микросомальных ферментов печени при одновременном применении уменьшают эффективность метамизола натрия. Седативные и анксиолитические лекарственные средства (транквилизаторы) усиливают анальгезирующее действие метамизола натрия. Рентгеноконтрастные лекарственные средства, коллоидные кровезаменители и пенициллины не должны применяться во время лечения препаратами, содержащими метамизол натрия. При одновременном применении циклоспорина снижается концентрация последнего в крови. Метамизол натрия, вытесняя из связи с белками плазмы пероральные гипогликемические лекарственные средства, непрямые антикоагулянты, глюкокортикостероиды и индометацин, может увеличивать выраженность их действия. Тиамазол и цитостатики повышают риск развития лейкопении. Эффект усиливают кодеин, блокаторы Н2-гистаминовых рецепторов и пропранолол (замедляет инактивацию метамизола натрия). Фармакологическое действие и фармакокинетика Спазмалин® - комбинированный препарат, в состав которого входят: ненаркотический анальгетик метамизол натрия, миотропное спазмолитическое средство питофенона и м-холиноблокирующее средство фенпивериния бромид. Метамизол натрия, производное пиразолона, обладает болеутоляющим, жаропонижающим и слабым противовоспалительным действием. Питофенон, подобно папаверину, оказывает прямое миотропное действие на гладкую мускулатуру внутренних органов и вызывает ее расслабление. Фенпивериния бромид за счет м-холиноблокирующего действия оказывает дополнительное миотропное действие на гладкую мускулатуру. Фармакокинетика: Метамизол натрия: хорошо и быстро всасывается в ЖКТ. В стенке кишечника гидролизуется с образованием активного метаболита - неизмененный метамизол натрия в крови отсутствует. Связь активного метаболита с белками - 50 - 60 %. Метаболизируется в печени, выводится почками. В терапевтических дозах проникает в грудное молоко. Питофенон быстро всасывается в ЖКТ: максимальная концентрация в плазме достигается в течение 30 - 60 мин: быстро распределяется в органах и тканях и достаточно быстро выводится с мочой. Период полувыведения составляет 1,8 часа. Фенпивериния бромид также быстро всасывается из ЖКТ и достигает максимальной концентрации в плазме крови в течение 1 часа. Выводится почками 32,4 - 40,4% в неизмененном виде, с желчью выводится 2,5 - 5,3% вещества. Особые указания В период лечения препаратом не рекомендуется принимать этанол. При длительном (более недели) лечении необходим контроль картины периферической крови и функционального состояния печени. При подозрении на агранулоцитоз или при наличии тромбоцитопении необходимо прекратить прием препарата. Недопустимо использование для купирования острых болей в животе (до выяснения причины). Непереносимость встречается весьма редко, однако угроза развития анафилактического шока после в/в введения препарата относительно выше, чем после приема препарата внутрь. У больных атопической бронхиальной астмой и поллинозами имеется повышенный риск развития аллергических реакций. При лечении больных, получающих цитостатические препараты, прием метамизола натрия должен проводиться только под наблюдением врача. Возможно окрашивание мочи в красный цвет за счет выделения метаболита метамизола натрия (клинического значения не имеет). Влияние на способность управлять транспортными средствами: Во время лечения следует соблюдать осторожность водителям транспортных средств и лицам, занимающимся потенциально опасными видами деятельности, требующими быстроты физической и психической реакции. Условия хранения и отпуска из аптек Условия хранения: При температуре ниже 30°С в защищенном от света месте. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Спазмалин® Международное непатентованное название:Метамизол натрия + Питофенон + Фенпивериния бромид. Форма выпуска:Таблетки. Состав:Каждая таблетка содержит: действующие вещества: метамизол натрия (анальгин) 500 мг, питофенона гидрохлорид 5 мг и фенпивериния бромид 0,10 мг: вспомогательные вещества: целлюлоза микрокристаллическая, карбоксиметилкрахмал натрия, кремния диоксид коллоидный, тальк, магния стеарат. АТХ: Регистрация: П N015008/02 Фармгруппа: анальгезирующее средство комбинированное (анальгезирующее ненаркотическое средство + спазмолитическое средство)Дата регистрации: 22.04.2008. Окончание регстрации: . Описание:Белого или белого с желтоватым оттенком цвета, круглые, плоские таблетки с риской на одной стороне. Упаковка: Таблетки. По 10 таблеток в блистер из алюминиевой фольги и ПВХ пленки. 1, 2 или 10 блистеров по 10 таблеток с инструкцией по применению в картонную пачку. Образец не для продажи: 10 таблеток в блистер из алюминиевой фольги и ПВХ пленки. 1 блистер с инструкцией по применению в картонную пачку. таблетки (блистер) 10 х 1/2/10 Срок годности:3 года. Не использовать позднее срока годности, указанного на упаковке. Владелец рег.удостоверения:Торрент Фармасьютикалс Лтд. Производитель:TORRENT PHARMACEUTICALS, Ltd. Представительство:ТОРРЕНТ ФАРМАСЬЮТИКАЛС Лтд
Модель:
RUR 563
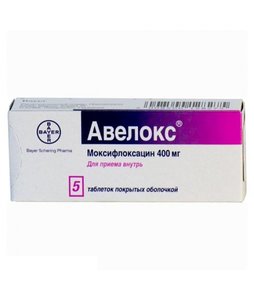
Показания Инфекционно-воспалительные заболевания, вызванные чувствительными к моксифлоксацину микроорганизмами: - Острый синусит. - Обострение хронического бронхита. - Неосложненные инфекции кожи и подкожных структур. - Внебольничная пневмония, включая внебольничную пневмонию, возбудителями которой являются штаммы микроорганизмов с множественной резистентностью к антибиотикам. - Осложненные инфекции кожи и подкожных структур (включая инфицированную диабетическую стопу). - Осложненные интраабдоминальные инфекции, включая полимикробные инфекции, в том числе внутрибрюшинные абсцессы. - Неосложненные воспалительные заболевания органов малого таза (включая сальпингиты и эндометриты). Streptococcus pneumoniae с множественной резистентностью к антибиотикам включают штаммы, резистентные к пенициллину, и штаммы, резистентные к двум или более антибиотикам из таких групп, как пенициллины (при МИК 2 мкг/мл), цефалоспорины II поколения (цефуроксим), макролиды, тетрациклины и триметоприм/сульфаметоксазол. Необходимо принимать во внимание действующие официальные руководства о правилах применения антибактериальных средств. Противопоказания Противопоказания - Гиперчувствительность к моксифлоксацину, другим хинолонам или любому другому компоненту препарата. - Возраст до 18 лет. - Беременность и период грудного вскармливания. - Наличие в анамнезе патологии сухожилий, развившейся вследствие лечения антибиотиками хинолонового ряда. - В доклинических и клинических исследованиях после введения моксифлоксацина наблюдалось изменение электрофизиологических параметров сердца, выражавшихся в удлинении интервала QT. В связи с этим, применение моксифлоксацина противопоказано у пациентов следующих категорий: врожденные или приобретенные документированные удлинения интервала QT, электролитные нарушения, особенно некоррегированная гипокалиемия: клинически значимая брадикардия: клинически значимая сердечная недостаточность со сниженной фракцией выброса левого желудочка: наличие в анамнезе нарушений ритма, сопровождавшихся клинической симптоматикой. - Моксифлоксацин нельзя применять с другими препаратами, удлиняющими интервал QT. - В связи с наличием в составе препарата лактозы, его прием противопоказан при врожденной непереносимости лактозы, дефиците лактазы, глюкозо-галактозной мальабсорбции. - В связи с ограниченным количеством клинических данным применение моксифлоксацина противопоказано пациентам с нарушением функции печени (класс С по классификации Чайлд-Пью) и пациентам с повышением трансаминаз более, чем в пять раз выше верхней границы нормы. С осторожностью: - При заболеваниях ЦНС (в т. ч. подозрительных в отношении вовлечения ЦНС), предрасполагающих к возникновению судорог и снижающих порог судорожной активности: - у пациентов с психозами и/или с психиатрическими заболеваниями в анамнезе: - у пациентов с потенциально проаритмическими состояниями (особенно у женщин и пациентов пожилого возраста), такими как острая ишемия миокарда и остановка сердца: - при миастении gravis: - у пациентов с циррозом печени: - при одновременном приеме с препаратами, снижающими содержание калия: - у пациентов с генетической предрасположенностью или фактическим наличием дефицита глюкозо-6-фосфатдегидрогеназы. Беременность Безопасность применения моксифлоксацина во время беременности не установлена и его применение противопоказано. Описаны случаи обратимых повреждений суставов у детей, получающих некоторые хинолоны, однако не сообщалось о проявлении этого эффекта у плода (при применении матерью во время беременности). В исследованиях на животных была показана репродуктивная токсичность. Потенциальный риск для человека неизвестен. Как и другие хинолоны, моксифлоксацин вызывает повреждения хрящей крупных суставов у недоношенных животных. В доклинических исследованиях установлено, что небольшое количество моксифлоксацина выделяется в грудное молоко. Данные о его применении у женщин во время лактации отсутствуют. Поэтому назначение моксифлоксацина в период грудного вскармливания противопоказано. Применение и дозы Рекомендуемый режим дозирования моксифлоксацина: 400 мг (1 таблетка) 1 раз в день при инфекциях, указанных выше. Не следует превышать рекомендуемую дозу. Таблетки следует проглатывать целиком, не разжевывая, запивая достаточным количеством воды, вне зависимости от приема пищи. Продолжительность лечения Продолжительность лечения определяется локализацией и тяжестью инфекции, а также клиническим эффектом: - Обострение хронического бронхита: 5-10 дней: - Острый синусит: 7 дней: - Неосложненные инфекции кожи и подкожных структур: 7 дней: - Внебольничная пневмония: общая продолжительность ступенчатой терапии (внутривенное введение с последующим приемом внутрь) составляет 7-14 дней: - Осложненные инфекции кожи и подкожных структур: общая продолжительность ступенчатой терапии моксифлоксацином (внутривенное введение с последующим приемом внутрь) составляет 7-21 день: - Осложненные интраабдоминальные инфекции: общая длительность ступенчатой терапии (внутривенное введение с последующим приемом внутрь) составляет 5-14 дней: - Неосложненные воспалительные заболевания органов малого таза: 14 дней. Не следует превышать рекомендуемую продолжительность лечения. По данным клинических исследований продолжительность лечения препаратом Авелокс® в таблетках может достигать 21 дня. Пациенты пожилого возраста Изменения режима дозирования у пожилых пациентов не требуется. Дети Эффективность и безопасность применения моксифлоксацина у детей и подростков не установлена. Нарушение функции печени Пациентам с нарушениями функции печени, изменения режима дозирования не требуется (для применения у пациентов с циррозом печени см. раздел "Особые указания"). Почечная недостаточность У пациентов с нарушением функции почек (в том числе при тяжелой степени почечной недостаточности с клиренсом креатинина <:30 мл/мин/1,73 м), а также у пациентов, находящихся на непрерывном гемодиализе и длительном амбулаторном перитонеальном диализе, изменения режима дозирования не требуется. Применение у пациентов различных этнических групп Изменения режима дозирования не требуется. Побочные эффекты и передозировка Побочные эффекты: Данные о неблагоприятных реакциях, зарегистрированных при применении моксифлоксацина 400 мг (внутрь, при ступенчатой терапии [внутривенное введение препарата с последующим его приемом внутрь] и только внутривенно), получены из клинических исследований и постмаркетинговых сообщений (выделены курсивом). Неблагоприятные реакции, перечисленные в группе "часто" встречались с частотой ниже 3 %, за исключением тошноты и диареи. В каждой частотной группе нежелательные лекарственные реакции перечислены в порядке убывания значимости. Частоту определяют следующим образом: часто (от 1/100 до <: 1/10), нечасто (от 1/1000 до <: 1/100), редко (от 1/10000 до <: 1/1000), очень редко (<: 1/10000). Частота развития следующих нежелательных реакций была выше в группе, получавшей ступенчатую терапию: Часто: повышение активности гамма-глутамилтрансферазы. Нечасто: желудочковые тахиаритмии, снижение артериального давления, отеки, псевдомембранозный колит (в очень редких случаях ассоциированный с угрожающими жизни осложнениями), судороги с различными клиническими проявлениями (в том числе "grand mal" припадки), галлюцинации, нарушение функции почек, почечная недостаточность (в результате дегидратации, что может привести к повреждению почек, особенно у пожилых пациентов с ранее существовавшими нарушениями функции почек). Передозировка: Имеются ограниченные данные о передозировке моксифлоксацина. Не отмечено каких-либо побочных эффектов при применении моксифлоксацина в дозе до 1200 мг однократно и по 600 мг в течение 10 дней и более. В случае передозировки следует ориентироваться на клиническую картину и проводить симптоматическую поддерживающую терапию с ЭКГ-мониторингом. Применение активированного угля сразу после перорального приема препарата может помочь предотвратить чрезмерное системное воздействие моксифлоксацина в случаях передозировки. Взаимодействие с другими ЛС: При совместном применении с атенололом, ранитидином, кальцийсодержащими добавками, теофиллином, циклоспорином, пероральными контрацептивными средствами, глибенкламидом, итраконазолом, дигоксином, морфином, пробенецидом (подтверждено отсутствие клинически значимого взаимодействия с моксифлоксацином) коррекции дозы не требуется. Препараты, удлиняющие интервал QТ Следует учитывать возможный аддитивный эффект удлинения интервала QT моксифлоксацина и других препаратов, которые влияют на удлинение интервала QT. Вследствие совместного применения моксифлоксацина и препаратов, влияющих на удлинение интервала QT, увеличивается риск развития желудочковой аритмии, включая полиморфную желудочковую тахикардию (torsade de pointes). Противопоказано совместное применение моксифлоксацина со следующими препаратами, влияющими на удлинение интервала QT: - антиаритмические препараты класса IA (хинидин, гидрохинидин, дизопирамид и др.)- антиаритмические препараты класса III (амиодарон, соталол, дофетилид, ибутилид и др.): - нейролептики (фенотиазин, пимозид, сертиндол, галоперидол, сультоприд и др.): - трициклические антидепрессанты: - антимикробные препараты (спарфлоксацин, эритромицин (внутривенно), пентамидин, противомалярийные препараты, особенно галофантрин): - антигистаминные препараты (терфенадин, астемизол, мизоластин): - другие (цизаприд, винкамин (внутривенно), бепридил, дифеманил). Антацидные средства, поливитамины и минералы Прием моксифлоксацина одновременно с антацидными средствами, поливитаминами и минералами может приводить к нарушению всасывания моксифлоксацина, вследствие образования хелатных комплексов с многовалентными катионами, содержащимися в этих препаратах. В результате концентрация моксифлоксацина в плазме крови может быть значительно ниже желаемой. В связи с этим антацидные препараты, антиретровирусные препараты (например, диданозин) и другие препараты, содержащие магний или алюминий, сукральфат и другие препараты, содержащие железо или цинк, следует применять не менее чем за 4 часа до или через 4 часа после приема внутрь моксифлоксацина. Варфарин При сочетанном применении с варфарином протромбиновое время и другие параметры свертывания крови не изменяются. Изменение значения МНО. У пациентов, получавших антикоагулянты в сочетании с антибиотиками, в том числе с моксифлоксацином, отмечаются случаи повышения антикоагуляционной активности противосвертывающих препаратов. Факторами риска являются наличие инфекционного заболевания (и сопутствующий воспалительный процесс), возраст и общее состояние пациента. Несмотря на то, что взаимодействия между моксифлоксацином и варфарином не выявлено, у пациентов, получающих сочетанное лечение этими препаратами, необходимо проводить мониторинг МНО и при необходимости корректировать дозу непрямых антикоагулянтов. Дигоксин Моксифлоксацин и дигоксин не оказывают существенного влияния на фармакокинетические параметры друг друга. При применении повторных доз моксифлоксацина максимальная концентрация дигоксина увеличивалась приблизительно на 30%, при этом значение площади под кривой "концентрация-время" (AUC) и минимальная концентрация дигоксина не изменялись. Активированный уголь При одновременном применении активированного угля и моксифлоксацина внутрь в дозе 400 мг системная биодоступность препарата снижается более чем на 80% в результате торможения его абсорбции. В случае передозировки применение активированного угля на ранней стадии всасывания препятствует дальнейшему повышению системного воздействия. Фармакологическое действие и фармакокинетика Механизм действия Моксифлоксацин - бактерицидный антибактериальный препарат широкого спектра действия, 8-метоксифторхинолон. Бактерицидное действие моксифлоксацина обусловлено ингибированием бактериальных топоизомераз II и IV, что приводит к нарушению процессов репликации, репарации и транскрипции биосинтеза ДНК микробной клетки и, как следствие, к гибели микробных клеток. Минимальные бактерицидные концентрации моксифлоксацина в целом сопоставимы с его минимальными ингибирующими концентрациями. Механизмы резистентности Механизмы, приводящие к развитию устойчивости к пенициллинам, цефалоспоринам, аминогликозидам, макролидам и тетрациклинам, не влияют на антибактериальную активность моксифлоксацина. Перекрестной устойчивости между этими группами антибактериальных препаратов и моксифлоксацином не отмечается. До сих пор также не наблюдалось случаев плазмидной устойчивости. Общая частота развития устойчивости очень незначительна (10 *АUIС - площадь под ингибирующей кривой (соотношение AUC/MИK90). Фармакокинетика: Всасывание При пероральном приеме моксифлоксацин всасывается быстро и почти полностью. Абсолютная биодоступность составляет около 91%. Фармакокинетика моксифлоксацина при приеме в дозе от 50 до 1200 мг однократно, а также по 600 мг/сутки в течение 10 дней является линейной. Равновесное состояние достигается в течение 3 дней. После однократного применения 400 мг моксифлоксацина Сmах в крови достигается в течение 0,5-4 ч и составляет 3,1 мг/л. После приема внутрь 400 мг моксифлоксацина 1 раз в сутки Css) и у пациентов, находящихся на непрерывном гемодиализе и длительном амбулаторном перитонеальном диализе. Нарушение функции печени Не было существенных различий в концентрации моксифлоксацина у пациентов с нарушениями функции печени (классы А и В по классификации Чайлд-Пью) по сравнению со здоровыми добровольцами и пациентами с нормальной функцией печени. Особые указания В некоторых случаях уже после первого применения препарата может развиться гиперчувствительность и аллергические реакции, о чем следует немедленно информировать врача. Очень редко, даже после первого применения препарата, анафилактические реакции могут прогрессировать до угрожающего жизни анафилактического шока. В этих случаях лечение препаратом Авелокс® следует прекратить и немедленно начать проводить необходимые лечебные мероприятия (в том числе противошоковые). При применении препарата Авелокс® у некоторых пациентов может отмечаться удлинение интервала QT. Препарат Авелокс® следует применять с осторожностью у женщин и пациентов пожилого возраста. Поскольку женщины по сравнению с мужчинами имеют более длинный интервал QT, они могут быть более чувствительны к препаратам, удлиняющим интервал QT. Пожилые пациенты также более подвержены действию препаратов, оказывающих влияние на интервал QT. Удлинение интервала QT сопряжено с повышенным риском желудочковых аритмий, включая полиморфную желудочковую тахикардию. Степень удлинения интервала QT может нарастать с повышением концентрации препарата, поэтому не следует превышать рекомендованную дозу. Однако у пациентов с пневмонией корреляции между концентрацией моксифлоксацина в плазме крови и удлинением интервала QT отмечено не было. Ни у одного из 9000 пациентов, получавших Авелокс®, не отмечалось сердечно-сосудистых осложнений и летальных случаев, связанных с удлинением интервала QT. При применении препарата Авелокс® может увеличиваться риск развития желудочковых аритмий у пациентов с предрасполагающими к аритмиям состояниями. В связи с этим препарат Авелокс® противопоказан при: - изменениях электрофизиологических параметров сердца, выражающихся в удлинении интервала QT: врожденных или приобретенных документированных удлинениях интервала QT, электролитных нарушениях, особенно некоррегированной гипокалиемии: клинически значимой брадикардии: клинически значимой сердечной недостаточности со сниженной фракцией выброса левого желудочка: наличии в анамнезе нарушений ритма, сопровождавшихся клинической симптоматикой: - применении с другими препаратами, удлиняющими интервал QT (см. раздел "Взаимодействие с другими лекарственными препаратами"). Препарат Авелокс® следует применять с осторожностью: - у пациентов с потенциально проаритмическими состояниями, такими как острая ишемия миокарда и остановка сердца: - у пациентов с циррозом печени (так как у данной категории пациентов нельзя исключить риск развития удлинения интервала QT). При приеме препарата Авелокс® сообщалось о случаях фульминантного гепатита, потенциально приводящего к развитию печеночной недостаточности (включая фатальные случаи) (см. раздел "Побочное действие"). Пациента следует информировать о том, что в случае появления симптомов печеночной недостаточности необходимо обратиться к врачу, прежде чем продолжить лечение препаратом Авелокс®. При приеме препарата Авелокс® сообщалось о случаях развития буллезных поражений кожи, таких как синдром Стивенса-Джонсона или токсический эпидермальный некролиз (см. раздел "Побочное действие"). Пациента следует информировать о том, что в случае появления симптомов поражения кожи или слизистых оболочек необходимо обратиться к врачу, прежде чем продолжить лечение препаратом Авелокс®. Применение препаратов хинолонового ряда сопряжено с возможным риском развития судорог. Препарат Авелокс® следует применять с осторожностью у пациентов с заболеваниями ЦНС и с нарушениями со стороны ЦНС, предрасполагающими к возникновению судорог или снижающими порог судорожной активности. Применение антибактериальных препаратов широкого спектра действия, включая препарат Авелокс®, сопряжено с риском развития псевдомембранозного колита. Этот диагноз следует иметь в виду у пациентов, у которых на фоне лечения препаратом Авелокс® развилась тяжелая диарея. В этом случае немедленно должна быть назначена соответствующая терапия. Препараты, угнетающие перистальтику кишечника, противопоказаны при развитии тяжелой диареи. Препарат Авелокс® следует использовать с осторожностью у пациентов с миастенией gravis в связи с возможным обострением заболевания. На фоне терапии хинолонами, в том числе моксифлоксацином, возможно развитие тендинита и разрыва сухожилия особенно у пожилых и пациентов, получающих глюкокортикостероиды. Описаны случаи, которые возникли в течение нескольких месяцев после завершения лечения. При первых симптомах боли или воспаления в месте повреждения прием препарата следует прекратить и разгрузить пораженную конечность. При применении хинолонов отмечаются реакции фоточувствительности. Однако при проведении доклинических и клинических исследований, а также при применении препарата Авелокс® в практике не отмечалось реакций фоточувствительности. Тем не менее пациенты, получающие препарат Авелокс®, должны избегать воздействия прямых солнечных лучей и ультрафиолетового света. Применение препарата в форме таблеток для приема внутрь не рекомендуется у пациенток с осложненными воспалительными заболеваниями органов малого таза (например, связанными с тубоовариальными или тазовыми абсцессами). Не рекомендуется использовать моксифлоксацин для лечения инфекций, вызванных штаммами Staphylococcus aureus резистентными к метициллину (MRSА). В случае предполагаемых или подтвержденных инфекций, вызванных MRSA, следует назначить лечение соответствующими антибактериальными препаратами (см. раздел "Фармакодинамика"). Способность препарата Авелокс® подавлять рост микобактерий может стать причиной взаимодействия in vitro моксифлоксацина с тестом на Mycobacterium spp, приводящего к ложноотрицательным результатам при анализе образцов пациентов, которым в этот период проводится лечение препаратом Авелокс®. У пациентов, которым проводилось лечение хинолонами, включая препарат Авелокс®, описаны случаи сенсорной или сенсомоторной полинейропатии, приводящей к парестезиям, гипестезиям, дизестезиям или слабости. Пациентов, которым проводится лечение препаратом Авелокс®, следует предупредить о необходимости немедленного обращения к врачу перед продолжением лечения в случае возникновения симптомов нейропатии, включающих боль, жжение, покалывание, онемение или слабость (см. раздел "Побочное действие"). Реакции со стороны психики могут возникнуть даже после первого применения фторхинолонов, включая моксифлоксацин. В очень редких случаях депрессия или психотические реакции прогрессируют до возникновения суицидальных мыслей и поведения с тенденцией к самоповреждению, включая суицидальные попытки (см. раздел "Побочное действие"). В случае развития у пациентов таких реакций следует отменить препарат Авелокс® и принять необходимые меры. Необходимо соблюдать осторожность при применении препарата Авелокс® пациентами с психозами и/или с психиатрическими заболеваниями в анамнезе. Из-за широкого распространения и растущей заболеваемости инфекциями, вызванными резистентной к фторхинолонам Neisseria gonorrhoeae при лечении пациентов с воспалительными заболеваниями органов малого таза не следует проводить монотерапию моксифлоксацином, за исключением случаев, когда присутствие резистентной к фторхинолонам N. gonorrhoeae исключено. Если нет возможности исключить присутствие резистентной к фторхинолонам N. gonorrhoeae, необходимо решить вопрос о дополнении эмпирической терапии моксифлоксацином соответствующим антибиотиком, который активен в отношении N. Gonorrhoeae (например, цефалоспорин). Дисгликемия Как и в случае с другими фторхинолонами, при применении препарата Авелокс® отмечалось изменение концентрации глюкозы в крови, включая гипо- и гипергликемию. На фоне терапии препаратом Авелокс® дисгликемия возникала преимущественно у пожилых пациентов с сахарным диабетом, получающих сопутствующую терапию пероральными гипогликемическими препаратами (например, препаратами сульфонилмочевины) или инсулином. При проведении лечения у пациентов с сахарным диабетом рекомендуется тщательный мониторинг концентрации глюкозы в крови (см. раздел "Побочное действие"). Влияние на способность управлять транспортными средствами: Фторхинолоны, включая моксифлоксацин, могут нарушать способность пациентов управлять автомобилем и заниматься другими потенциально опасными видами деятельности, требующими повышенного внимания и быстроты психомоторных реакций, вследствие влияния на ЦНС и нарушения зрения. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25 °С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Авелокс® Международное непатентованное название:Моксифлоксацин. Форма выпуска:таблетки, покрытые пленочной оболочкой. Состав:В 1 таблетке содержится: Действующее вещество: моксифлоксацина гидрохлорид 436,8 мг, эквивалентно 400,0 мг моксифлоксацина. Вспомогательные вещества: микрокристаллическая целлюлоза (136,0 мг), натрия кроскармеллоза (32,0 мг), лактозы моногидрат (68,0 мг), магния стеарат (6,0 мг), оболочка пленочная - гипромеллоза (9,0-12,6 мг), краситель железа оксид красный (0,3-0,42 мг), макрогол 4000 (3,0-4,2 мг), титана диоксид (2,7-3,78 мг). АТХ: Регистрация: Лекарственное средство П N012034/01 Фармгруппа: Противомикробное средство - фторхинолон. Дата регистрации: 17.05.2010 / 14.01.2013. Окончание регстрации: . Описание:Розовые, матовые, продолговатые, двояковыпуклые, с фаской таблетки, покрытые пленочной оболочкой, с гравировкой "BAYER" на одной стороне и "М400" на другой стороне. Упаковка:Таблетки, покрытые пленочной оболочкой, 400 мг. По 5 таблеток в блистер из фольги алюминиевой и ПА/Ал/ПВХ или из фольги алюминиевой и ПП. По 1 или 2 блистера вместе с инструкцией по применению в картонной пачке, или. По 7 таблеток в блистер из фольги алюминиевой и ПА/Ал/ПВХ или фольги алюминиевой и ПП. По 1 блистеру вместе с инструкцией по применению в картонной пачке. Срок годности:5 лет. Не использовать после истечения срока годности, указанного на упаковке. Владелец рег.удостоверения:Байер Фарма АГ Производитель:BAYER PHARMA, AG. Представительство:БАЙЕР, АО

Модель:
RUR 1150
Состав Противопоказания Показания к применению Условия хранения Способ применения и дозы Информация Состав Активное вещество: Пальма карликовая, ягоды(Serenoa serrulata) 115 мг Тыква, семена (Cururbita maxima) 90 мг Пигеум африканский(Pygeum africanum)75 мг Витамин E (d-альфа токоферола ацетат)30 М.Е. Цинка глицинат (20% цинка) 62,5 мг L-Глутамин 25 мг Лопух, корень (Arctium maius) 15 мг L-Аланин 12,5 мг Тополь белый кора 12,5 мг Золотарник листья, стебель (Solidago adorax) 7,5 мг Меди глицинат ( 3% меди ) 15,15 мг Магния стеарат. Описание: В силу своей природы мужчины редко уделяют внимание своему здоровью, руководствуясь принципом: "Не болит - значит здоров". Поэтому, таким тревожным сигналам, как дискомфорт в области промежности, учащенное мочеиспускание большинство мужчин не придают значения и воспринимают их как временное явление, а ведь эти симптомы - первые признаки простатита - заболевания, с которым сталкиваются около 70% мужчин репродуктивного возраста. При отсутствии своевременного лечения именно простатит приводит к серьезным последствиям для здоровья мужчины: снижению полового влечения, нарушению потенции и бесплодию. Что бы избежать всех этих проблем, необходима профилактика простатита, т.е. поддерживать правильную работу предстательной железы специальными препаратами. Тем более, что это совсем несложно. На сегодняшний день эффективным и безопасным является натуральный биокомплекс Простата Форте™. Благодаря специальному витаминно-микроэлементному составу и экстрактам лекарственных растений, Простата Форте™ комплексно воздействует на мужской организм. Простата Форте™ эффективно нормализует обменные процессы в предстательной железе, снимает воспаление и отек простаты, дискомфорт в промежности, устраняет болевые ощущения при мочеиспускании. Простата Форте™ с успехом прошел клинические исследования, проведенные в НИИ Урологии МЗ РФ, которые подтвердили его эффективность при лечении простатита, аденомы предстательной железы, отмечен значимый клинический эффект при лечении инфекционно-воспалительных заболеваниях мужской мочеполовой системы. Форма выпуска: 60 капсул. Противопоказания Индивидуальная непереносимость компонентов комплекса. Перед применением рекомендуется проконсультироваться с врачом. не является лекарством. Показания к применению - затрудненное мочеиспускание при заболеваниях простаты - ухудшение работы мочеполовой системы Рекомендован в качестве биологически активной добавки. Условия хранения Хранить в недоступном для детей, сухом месте при комнатной температуре. Способ применения и дозы Для профилактики простатита препарат следует принимать внутрь, взрослым по 1 капсуле 2 раза в день во время еды. Продолжительность курса - 1 месяц. При необходимости прием можно повторить. Длительность курса лечения простатита может составлять от трех до шести месяцев, в зависимости от индивидуальных показаний. Перед началом второго курса лечения простатита следует проконсультироваться с врачом. Информация Внешний вид товара может отличаться от изображённого на фотографии. Имеются противопоказания. Необходимо ознакомиться с инструкцией или проконсультироваться со специалистом

Модель:
RUR 971
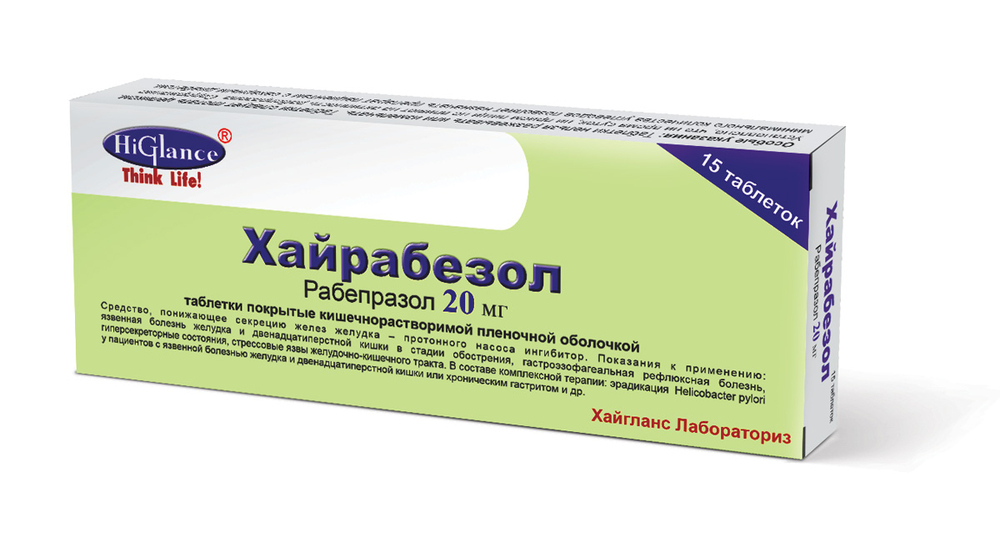
Показания Пациенты старше 18 лет - Артериальная гипертензия: - хроническая сердечная недостаточность (II-IV функциональный класс по классификации NYHA) в составе комплексной терапии (на фоне стандартной терапии) у пациентов, не получающих ингибиторы АПФ: - повышение выживаемости пациентов после перенесенного острого ИМ, осложненного левожелудочковой недостаточностью и/или систолической дисфункцией левого желудочка (ЛЖ), при наличии стабильных показателей гемодинамики. Пациенты от 6 до 18 лет - Артериальная гипертензия у детей и подростков от 6 до 18 лет. Противопоказания Противопоказания - Повышенная чувствительность к валсартану или к другим компонентам препарата: - тяжелые нарушения функции печени (более 9 баллов по шкале Чайлд-Пью), билиарный цирроз и холестаз: - одновременное применение с алискиреном у пациентов с сахарным диабетом или умеренными и тяжелыми нарушениями функции почек (КК менее 60 мл/мин): - беременность и период грудного вскармливания: - возраст до 6 лет - по показанию артериальная гипертензия, до 18 лет - по другим показаниям: - дефицит лактазы, непереносимость лактозы, синдром глюкозо-галактозной мальабсорбции, так как в состав препарата Вальсакор входит лактоза. С осторожностью: Гиперкалиемия, одновременное применение калийсберегающих диуретиков, препаратов калия, калийсодержащих пищевых добавок или других препаратов, способных повышать содержание калия в плазме крови (например, гепарин), легкие и умеренные нарушения функции печени небилиарного генеза без явлений холестаза, тяжелые нарушения функции почек (КК менее 10 мл/мин) (нет клинических данных), нарушения функции почек у пациентов от 6 до 18 лет (КК менее 30 мл/мин), в том числе находящихся на гемодиализе, гипонатриемия, соблюдение диеты с ограничением потребления поваренной соли, состояния, сопровождающиеся снижением объема циркулирующей крови (ОЦК) (в том числе диарея, рвота), двусторонний стеноз почечных артерий или стеноз артерии единственной почки, состояние после трансплантации почки, первичный гиперальдостеронизм, у пациентов с хронической сердечной недостаточностью III-IV функционального класса (по NYНA), функция почек которых зависит от состояния ренин-ангиотензин-альдостероновой системы (РААС), стеноз аортального и/или митрального клапана, гипертрофическая обструктивная кардиомиопатия (ГОКМП), у пациентов с наследственным ангионевротическим отеком, либо ангионевротическим отеком на фоне предшествующей терапии АРА II или ингибиторами АПФ. Не рекомендуется применять АРА II, включая валсартан, одновременно с ингибиторами АПФ, поскольку их одновременное применение не имеет преимуществ перед монотерапией валсартаном или ингибитором АПФ в отношении показателей общей смертности. Беременность Применение АРА II в I триместре беременности не рекомендуется. Применение АРА II противопоказано во II-III триместрах беременности, поскольку применение во II-III триместрах беременности может вызвать фетотоксические эффекты (снижение функции почек, маловодие, замедление окостенения костей черепа плода) и неонатальные токсические эффекты (почечную недостаточность, артериальную гипотензию, гиперкалиемию). Если все же применяли препарат во II-III триместрах беременности, то необходимо провести ультразвуковое исследование почек и костей черепа плода. При планировании беременности рекомендуется пациентку перевести на альтернативную гипотензивную терапию с учетом профиля безопасности. При подтверждении беременности препарат Вальсакор необходимо отменить как можно раньше. Новорожденные, матери которых получали АРА II во время беременности, нуждаются в медицинском наблюдении, так как существует риск развития артериальной гипотензии. Нет данных о выделении валсартана в грудное молоко. Поэтому следует решить вопрос о прекращении кормления грудью или отмене терапии валсартаном и переводе на альтернативную гипотензивную терапию с учетом профиля безопасности. Применение и дозы Внутрь, независимо от времени приема пищи. Пациенты старше 18 лет Артериальная гипертензия Рекомендуемая начальная доза препарата Вальсакор составляет 80 мг 1 раз в сутки, вне зависимости от расовой принадлежности, возраста и пола пациента. Антигипертензивный эффект развивается в течение 2-х недель и достигает своего максимума через 4 недели. Пациентам, у которых не удается достичь адекватного контроля АД, суточная доза валсартана может быть постепенно увеличена до максимальной суточной дозы 320 мг. С целью дополнительного снижения АД возможно применение диуретических средств (гидрохлоротиазид), а также одновременное применение других гипотензивных средств. Хроническая сердечная недостаточность Рекомендуемая начальная доза препарата Вальсакор составляет 40 мг 2 раза в сутки. Дозу препарата следует постепенно увеличивать в течение, как минимум, 2-х недель до 80 мг 2 раза в сутки, а при хорошей переносимости - до 160 мг 2 раза в сутки. Максимальная суточная доза составляет 320 мг в два приема. При этом может потребоваться снижение дозы одновременно принимаемых диуретиков. Возможно одновременное применение с другими лекарственными средствами, предназначенными для лечения ХСН. Однако одновременная терапия препаратами трех классов: валсартаном, ингибиторами АПФ и бета-адреноблокаторами не рекомендуется. Оценка состояния пациентов с ХСН должна включать контроль функции почек. Применение после перенесенного острого инфаркта миокарда Лечение следует начинать уже через 12 часов после развития острого ИМ при наличии стабильных показателей гемодинамики. После применения начальной дозы 20 мг 2 раза в сутки (1/2 таблетки 40 мг), дозу препарата Вальсакор можно постепенно увеличить методом титрования до: 40 мг, 80 мг и 160 мг 2 раза в сутки в течение нескольких недель. Максимальная суточная доза составляет 320 мг в 2 приема. Рекомендуется увеличение дозы до 80 мг 2 раза в сутки к концу 2-й недели, а максимальная целевая доза 160 мг 2 раза в сутки может быть достигнута к концу 3-го месяца терапии препаратом Вальсакор. Достижение целевой дозы зависит от переносимости валсартана в период титрования доз. При развитии чрезмерного снижения АД, сопровождающегося клиническими проявлениями, или нарушением функции почек следует уменьшить дозу препарата. Возможно одновременное применение с другими лекарственными средствами, в том числе тромболитическими средствами, ацетилсалициловой кислотой в качестве антиагрегантного средства, бета-адреноблокаторами и ингибиторами ГМГ-КоА-редуктазы (статинами). Одновременное применение с ингибиторами АПФ не рекомендуется. Оценка состояния пациентов после перенесенного острого ИМ должна включать контроль функции почек. Пациенты от 6 до 18 лет Артериальная гипертензия Рекомендуемая начальная доза препарата Вальсакор у детей и подростков от 6 до 18 лет составляет 40 мг при массе тела ребенка менее 35 кг и 80 мг при массе тела ребенка более 35 кг. Рекомендуется коррекция дозы с учетом снижения АД. Максимальные рекомендованные суточные дозы отражены в таблице ниже. Применение более высоких доз не рекомендовано.ТАБЛИЦЪХроническая сердечная недостаточность и перенесенный острый инфаркт миокарда. Препарат Вальсакор не рекомендован для лечения ХСН и перенесенного острого инфаркта миокарда у пациентов младше 18 лет. Пациенты пожилого возраста. Коррекции дозы препарата у пациентов старше 65 лет не требуется. Нарушение функции почек. Коррекции дозы у пациентов с КК более 10 мл/мин не требуется. Одновременное применение препарата Вальсакор с алискиреном у пациентов с умеренными и тяжелыми нарушениями функции почек (КК менее 60 мл/мин) противопоказано. Нарушение функции печениУ пациентов с легким или умеренным нарушением функции печени небилиарного генеза без явлений холестаза препарат следует применять с осторожностью, суточная доза не должна превышать 80 мг. Пациенты с сахарным диабетом Одновременное применение препарата Вальсакор с алискиреном у пациентов с СД противопоказано. Побочные эффекты и передозировка Побочные эффекты: Классификация частоты развития побочных эффектов Всемирной организации здравоохранения (ВОЗ): очень часто 1/10 часто от 1/100 до <: 1/10 нечасто от 1/1000 до <: 1/100 редко от 1/10000 до <: 1/1000 очень редко <: 1/10000 частота неизвестна не может быть оценена на основе имеющихся данных. Профиль безопасности валсартана у пациентов с АГ в возрасте от 6 до 18 лет не отличается от профиля безопасности валсартана у пациентов с АГ старше 18 лет. Артериальная гипертензия Нарушения со стороны крови и лимфатической системы: частота неизвестна: снижение гемоглобина, снижение гематокрита, нейтропения, тромбоцитопения. Нарушения со стороны иммунной системы: частота неизвестна: реакции повышенной чувствительности, включая сывороточную болезнь. Нарушения со стороны обмена веществ и питания: частота неизвестна: повышение содержания калия в сыворотке крови, гипонатриемия. Нарушения со стороны органа слуха и лабиринтные нарушения: нечасто: вертиго. Нарушения со стороны сосудов: частота неизвестна: васкулит. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: нечасто: кашель. Нарушения со стороны желудочно-кишечного тракта: нечасто: боль в животе. Нарушения со стороны печени и желчевыводящих путей: частота неизвестна: нарушение функции печени, включая повышение концентрации билирубина в плазме крови. Нарушения со стороны кожи и подкожных тканей: частота неизвестна: ангионевротический отек, кожная сыпь, кожный зуд, буллезный дерматит. Нарушения со стороны скелетно-мышечной и соединительной ткани: частота неизвестна: миалгия. Нарушения со стороны почек и мочевыводящих путей: частота неизвестна: нарушение функции почек и почечная недостаточность, повышение концентрации креатинина в сыворотке крови. Общие расстройства и нарушения в месте введения: нечасто: повышенная утомляемость. В ходе клинических исследований у пациентов с АГ наблюдались следующие нежелательные явления, причинно-следственная связь которых с приемом валсартана не установлена: артралгия, астения, боль в спине, диарея, головокружение, бессонница, снижение либидо, тошнота, периферические отеки, фарингит, ринит, синусит, инфекции верхних дыхательных путей. После перенесенного острого инфаркта миокарда и/или при хронической сердечной недостаточности (II-IV функциональный класс по классификации NYHA) Нарушения со стороны крови и лимфатической системы: частота неизвестна: тромбоцитопения. Нарушения со стороны иммунной системы: частота неизвестна: реакции повышенной чувствительности, включая сывороточную болезнь. Нарушения со стороны обмена веществ и питания: нечасто: гиперкалиемия: частота неизвестна: повышение содержания калия в сыворотке крови, гипонатриемия. Нарушения со стороны нервной системы: часто: головокружение, постуральное головокружение: нечасто: обморок, головная боль. Нарушения со стороны органа слуха и лабиринтные нарушения: нечасто: вертиго. Нарушения со стороны сердца: нечасто: усиление симптомов хронической сердечной недостаточности. Нарушения со стороны сосудов: часто: выраженное снижение АД, ортостатическая гипотензия: частота неизвестна: васкулит. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: нечасто: кашель. Нарушения со стороны желудочно-кишечного тракта: нечасто: тошнота, диарея. Нарушения со стороны печени и желчевыводящих путей: частота неизвестна: нарушение функции печени. Нарушения со стороны кожи и подкожных тканей: нечасто: ангионевротический отек: частота неизвестна: кожная сыпь, кожный зуд, буллезный дерматит. Нарушения со стороны скелетно-мышечной и соединительной ткани: редко: рабдомиолиз: частота неизвестна: миалгия. Нарушения со стороны почек и мочевыводящих путей: часто: нарушение функции почек и почечная недостаточность: нечасто: острая почечная недостаточность, повышение концентрации креатинина в сыворотке крови: частота неизвестна: повышение содержания азота мочевины в плазме крови. Общие расстройства и нарушения в месте введения: нечасто: астения, повышенная утомляемость. Передозировка: Симптомы: основным ожидаемым проявлением передозировки валсартана является выраженное снижение АД, которое может привести к нарушению сознания, коллапсу и/или шоку. Лечение: симптоматическое, рекомендуется вызвать рвоту и промыть желудок. При развитии выраженного снижения АД необходимо перевести пациента в положение "лежа" на спине с приподнятыми вверх ногами, внутривенно ввести 0,9% раствор натрия хлорида. Рекомендуется регулярный контроль деятельности сердца и дыхательной системы, ОЦК и количества выделяемой мочи. Гемодиализ неэффективен. Взаимодействие с другими ЛС: Одновременное применение противопоказано Одновременное применение АРА II, включая валсартан, или ингибиторов АПФ с алискиреном противопоказано у пациентов с СД или умеренными и тяжелыми нарушениями функции почек (КК менее 60 мл/мин). Одновременное применение не рекомендуется Литий Одновременное применение с препаратами лития не рекомендуется, так как возможно обратимое увеличение концентрации лития в плазме крови и усиление его токсического действия. Риск токсических проявлений, связанных с применением препаратов лития, может дополнительно увеличиваться при одновременном применении с препаратом Вальсакор и диуретиками. При необходимости одновременного применения с препаратами лития следует тщательно контролировать концентрацию лития в плазме крови. Калийсберегающие диуретики (спиронолактон, эплеренон, триамтерен, амилорид), препараты калия, калийсодержащие пищевые добавки и другие лекарственные средства и вещества, которые могут вызвать гиперкалиемию (например, гепарин) При необходимости одновременного применения с препаратами, влияющими на содержание калия, рекомендуется контролировать содержание калия в плазме крови. Одновременное применение с осторожностью Двойная блокада ренин-ангиотензин-альдостероновой системы У некоторых пациентов двойная блокада РААС сопровождалась развитием артериальной гипотензии, обморока, гиперкалиемии и нарушением функции почек (включая острую почечную недостаточность (ОПН)). Требуется соблюдать осторожность при одновременном применении АРА II, включая валсартан с лекарственными средствами, оказывающими влияние на РААС, такими как, ингибиторы АПФ или алискирен. Нестероидные противовоспалительные препараты (НПВП), в том числе селективные ингибиторы циклооксигеназы-2 (ЦОГ-2), ацетилсалициловая кислота в дозе более 3 г/сут и неселективные НПВП При одновременном применении с валсартаном возможно уменьшение антигипертензивного эффекта, увеличение риска развития нарушений функции почек и повышение содержания калия в плазме крови. До начала комбинированной терапии рекомендуется оценить функцию почек, а также провести коррекцию нарушений водноэлектролитного баланса. Белки-переносчики Исследования in vitro на культурах печени показали, что валсартан является субстратом для белков-переносчиков ОАТР1В1/ОАТР1ВЗ и MRP2. Одновременное применение валсартана с ингибиторами белка-переносчика ОАТР1В1/ОАТР1ВЗ (рифампицин, циклоспорин) или MRP2 (ритонавир) может увеличить системную экспозицию валсартана (Сmах и AUC). Необходимо соблюдать осторожность в начале одновременного применения с вышеуказанными препаратами или после их отмены. Отсутствие лекарственного взаимодействия Не выявлено клинически значимых взаимодействий со следующими лекарственными средствами: циметидин, варфарин, фуросемид, дигоксин, атенолол, индометацин, гидрохлоротиазид, амлодипин и глибенкламид. Пациенты от 6 до 18 лет У детей и подростков АГ часто связана с нарушением функции почек. Одновременное применение валсартана с другими лекарственными средствами, влияющими на РААС, может вызывать повышение содержания калия в плазме крови у таких пациентов. Необходимо соблюдать осторожность при одновременном применении вышеуказанной комбинации и регулярно контролировать функцию почек и содержание калия в плазме крови у данной группы пациентов. Фармакологическое действие и фармакокинетика Валсартан является селективным антагонистом рецепторов ангиотензина II (типа AT1) для приема внутрь, небелковой природы. Избирательно блокирует AT1-рецепторы. Следствием блокады AT1-рецепторов является повышение плазменной концентрации ангиотензина II, который может стимулировать незаблокированные АТ2-рецепторы, что уравновешивает вазопрессорные эффекты, связанные с возбуждением AT1-рецепторов. Валсартан не имеет агонистической активности в отношении АТ1-рецепторов. Его сродство к АТ1-рецепторам примерно в 20 000 раз выше, чем к АТ2-рецепторам. Валсартан не ингибирует ангиотензинпревращающий фермент (АПФ), известный также под названием кининазы II, который превращает ангиотензин I в ангиотензин II и разрушает брадикинин. В связи с отсутствием влияния на АПФ, не потенцируются эффекты брадикинина и субстанции Р. Частота развития сухого кашля ниже у пациентов, получавших антагонисты рецепторов ангиотензина II (АРА II), в сравнении с пациентами, получавшими ингибитор АПФ. Валсартан не вступает во взаимодействие и не блокирует рецепторы других гормонов или ионные каналы, участвующие в регуляции функций сердечно-сосудистой системы. Применение при артериальной гипертензии у пациентов старше 18 лет При лечении артериальной гипертензии (АГ) валсартан снижает артериальное давление (АД), не влияя на частоту сердечных сокращений (ЧСС). После приема внутрь разовой дозы валсартана антигипертензивный эффект развивается в течение 2-х часов, а максимальное снижение АД достигается через 4-6 часов. Антигипертензивный эффект валсартана сохраняется в течение 24 часов после его применения. При постоянном применении валсартана максимальное снижение АД, вне зависимости от дозы, достигается через 2-4 недели и поддерживается на достигнутом уровне в ходе длительной терапии. Одновременное применение с гидрохлоротиазидом позволяет достичь значимого дополнительного снижения АД. Внезапная отмена валсартана не сопровождается резким повышением АД или другими нежелательными клиническими последствиями (то есть синдром "отмены" не развивается). У пациентов с АГ, сахарным диабетом (СД) 2 типа и нефропатией, принимающих валсартан в дозе 160-320 мг/сут отмечается значительное снижение протеинурии (36-44%). Применение после острого инфаркта миокарда у пациентов старше 18 лет При применении валсартана в течение 2-х лет, с началом приема от 12 часов до 10 дней после развития инфаркта миокарда (ИМ) (осложненного левожелудочковой недостаточностью и/или систолической дисфункцией левого желудочка) снижаются показатели общей смертности, сердечно-сосудистой смертности и удлиняется время до первой госпитализации по поводу обострения течения хронической сердечной недостаточности (ХСН), повторного ИМ, внезапной остановки сердца и инсульта (без летального исхода). ХСН у пациентов старше 18 лет При применении валсартана (в средней суточной дозе 254 мг) в течение 2-х лет у пациентов с ХСН II-IV функционального класса по классификации NYHA с фракцией выброса левого желудочка (ФВЛЖ) менее 40% и внутренним диастолическим диаметром ЛЖ более 2,9 см/м 2, получающих стандартную терапию (ингибиторы АПФ, диуретики, дигоксин, бета-адреноблокаторы), было отмечено достоверное снижение риска госпитализации по поводу обострения течения ХСН, замедление прогрессирования ХСН, улучшение функционального класса ХСН по классификации NYHA, увеличение ФВЛЖ, а также уменьшение выраженности симптомов сердечной недостаточности и улучшению качества жизни по сравнению с плацебо. Применение у пациентов старше 18 лет с АГ и нарушением толерантности к глюкозе При применении валсартана и изменении образа жизни отмечалось статистически достоверное снижение риска развития СД у пациентов с АГ и нарушением толерантности к глюкозе. Валсартан не оказывал влияния на частоту летальных исходов в результате сердечно-сосудистых событий, ИМ и транзиторных ишемических атак без летального исхода, на частоту госпитализаций по причине обострения течения ХСН или нестабильной стенокардии, артериальной реваскуляризации у данной категории пациентов, отличающихся по возрасту, полу и расовой принадлежности. У пациентов, получающих валсартан, риск развития микроальбуминурии был достоверно ниже, чем у пациентов, не получающих данную терапию. Рекомендуемая начальная доза валсартана у пациентов с АГ и нарушением толерантности к глюкозе составляет 80 мг 1 раз в сутки. При необходимости доза может быть увеличена до 160 мг. Применение у детей и подростков от 6 до 18 лет при АГ У детей и подростков от 6 до 18 лет валсартан обеспечивает дозозависимое плавное снижение АД. При применении валсартана максимальное снижение АД, вне зависимости, от принятой внутрь дозы, достигается в течение 2-х недель и поддерживается на достигнутом уровне в ходе длительной терапии. Фармакокинетика: Всасывание После приема валсартана внутрь максимальная концентрация (Cmax) в плазме крови достигается в течение 2-4 часов. Средняя абсолютная биодоступность составляет 23%. При применении валсартана с пищей площадь под кривой "концентрация-время" (AUC) и Сmах в плазме крови уменьшаются на 40% и 50% соответственно. Тем не менее через 8 часов после приема препарата плазменные концентрации валсартана, принятого натощак и с пищей, одинаковы. Уменьшение AUC не сопровождается клинически значимым снижением терапевтического эффекта валсартана, поэтому препарат Вальсакор можно принимать независимо от времени приема пищи. Распределение Объем распределения (Vd) валсартана в период равновесного состояния после внутривенного введения составлял около 17 л, что указывает на отсутствие выраженного распределения валсартана в тканях. Валсартан активно связывается с белками плазмы крови (94-97%), преимущественно с альбумином. Метаболизм Валсартан не подвергается существенной биотрансформации, только около 20% дозы, принятой внутрь, выводится в виде метаболитов. Гидроксильный метаболит определяется в плазме крови в низких концентрациях (менее 10% от AUC валсартана). Этот метаболит не обладает фармакологической активностью. Выведение Валсартан выводится двухфазно: α-фаза с периодом полувыведения (Т1/2α) менее 1 часа и β-фаза с Т1/2β - около 9 часов. Валсартан выводится, в основном, в неизмененном виде через кишечник (около 83%) и почками (около 13%). После внутривенного введения плазменный клиренс валсартана составляет около 2 л/час, почечный клиренс - 0,62 л/час (около 30% от общего клиренса). Т1/2 валсартана составляет 6 часов. Фармакокинетика особых групп пациентов Пациенты с ХСН У пациентов с ХСН время достижения Сmax и Т1/2 сходны с аналогичными показателями у здоровых добровольцев. Повышение AUC и Сmах прямо пропорционально увеличению дозы валсартана (с 40 мг до 160 мг 2 раза в сутки). Фактор кумуляции составляет, в среднем, 1,7. При приеме внутрь клиренс валсартана составляет около 4,5 л/час. Возраст пациентов с ХСН не оказывал влияния на клиренс валсартана. Пациенты пожилого возраста (старше 65 лет) У некоторых пациентов в возрасте старше 65 лет биодоступность валсартана была выше таковой у пациентов молодого возраста, что не имеет клинического значения. Пациенты с нарушениями функции почек Почечный клиренс валсартана составляет только 30% от общего клиренса, поэтому корреляции между функцией почек и системной биодоступностью валсартана нет. Коррекции дозы у пациентов с нарушением функции почек (клиренс креатинина (КК) более 10 мл/мин) не требуется. Безопасность валсартана у пациентов с КК менее 10 мл/мин и пациентов, находящихся на гемодиализе, не установлена, поэтому у таких пациентов препарат следует применять с осторожностью. Так как степень связывания валсартана с белками плазмы крови высокая, его выведение при гемодиализе маловероятно. Пациенты с нарушениями функции печени Около 70% всосавшейся дозы валсартана выводится через кишечник, преимущественно, в неизмененном виде. Валсартан в существенной степени не подвергается метаболизму. У пациентов с легким или умеренным нарушением функции печени отмечалось повышение биодоступности (AUC) валсартана в 2 раза по сравнению с таковой у здоровых добровольцев. Однако не наблюдается корреляции значений AUC валсартана со степенью нарушения функции печени. Применение валсартана у пациентов с тяжелым нарушением функции печени не изучалось. Пациенты от 6 до 18 лет Фармакокинетика валсартана у детей и подростков от 6 до 18 лет не отличается от фармакокинетики валсартана у пациентов старше 18 лет. Особые указания Гиперкалиемия При одновременном применении калийсберегающих диуретиков (спиронолактон, эплеренон, триамтерен, амилорид), препаратов калия, калийсодержащих заменителей соли или других препаратов, способных повышать содержание калия в плазме крови (например, гепарин), следует соблюдать осторожность. Необходимо регулярно контролировать содержание калия в плазме крови. Нарушение функции почек У пациентов с нарушением функции почек не требуется изменения доз препарата. Так как отсутствуют данные о применении препарата при тяжелой почечной недостаточности (КК менее 10 мл/мин или 0,167 мл/с) и у пациентов, находящихся на гемодиализе, в таких случаях препарат рекомендуется применять с осторожностью. Одновременное применение валсартана с алискиреном у пациентов с умеренными и тяжелыми нарушениями функции почек (КК менее 60 мл/мин) противопоказано. Нарушение функции печени У пациентов с легкими и умеренными нарушениями функции печени без явлений холестаза препарат Вальсакор следует применять с осторожностью. Пациенты с гипонатриемией и/или дегидратацией У пациентов с выраженной гипонатриемией и/или дегидратацией, например, вследствие приема больших доз диуретиков, в редких случаях в начале терапии препаратом Вальсакор может развиться артериальная гипотензия с клиническими проявлениями. Перед началом лечения рекомендовано восстановить содержание натрия и/или ОЦК, в частности путем уменьшения доз диуретиков. Стеноз почечной артерии Применение валсартана коротким курсом у пациентов с реноваскулярной гипертензией, развившейся вторично вследствие стеноза артерии единственной почки, не вызывает существенных изменений показателей почечной гемодинамики, концентрации креатинина или азота мочевины в сыворотке крови. Однако, учитывая, что другие лекарственные средства, оказывающие влияние на РААС, могут вызывать повышение концентрации мочевины и креатинина в сыворотке крови у пациентов с двусторонним стенозом почечных артерий или стенозом артерии единственной почки, необходимо регулярно контролировать концентрации креатинина и остаточного азота мочевины в сыворотке крови. Состояние после перенесенной трансплантации почки Безопасность применения препарата Вальсакор у пациентов, недавно перенесших трансплантацию почки, не установлена. Первичный гиперальдостеронизм Пациенты с первичным гиперальдостеронизмом резистентны к гипотензивным препаратам, влияющим на РААС, поэтому таким пациентам применение препарата Вальсакор не рекомендуется. Стеноз аортального и/или митрального клапанов, ГОКМП Препарат Вальсакор необходимо с осторожностью применять у пациентов с гемодинамически значимым стенозом аортального и/или митрального клапанов или с ГОКМП. Период после перенесенного ИМ Одновременное применение с ингибиторами АПФ не рекомендуется, так как не имеет дополнительных клинических преимуществ перед монотерапией и увеличивает риск развития нежелательных явлений. Применение валсартана у пациентов после перенесенного ИМ часто приводит к небольшому снижению АД, однако прекращение терапии по причине артериальной гипотензии обычно не требуется, если выполнять рекомендации по дозированию препарата. Терапию препаратом Вальсакор следует начинать осторожно. Оценка состояния больных после перенесенного острого инфаркта миокарда должна включать контроль функции почек. Возможно одновременное применение при остром ИМ с другими лекарственными средствами: тромболитики, ацетилсалициловая кислота, бета-адреноблокаторы и ингибиторы ГМГ-КоА-редуктазы (статины). Хроническая сердечная недостаточность У пациентов с ХСН не рекомендуется одновременное применение трех классов препаратов: ингибиторов АПФ, бета-адреноблокаторов и валсартана, так как эта терапия не давала дополнительного клинического эффекта, при этом увеличивался риск развития нежелательных явлений. Применение у пациентов с ХСН обычно сопровождается снижением АД, однако при соблюдении рекомендаций по подбору доз лечение редко требует отмены по причине артериальной гипотензии. Терапию препаратом Вальсакор у пациентов с ХСН следует начинать с осторожностью. Вследствие подавления активности РААС у некоторых пациентов (например, у пациентов с хронической сердечной недостаточностью III-IV функционального класса по классификации NYNA, функция почек которых зависит от состояния РААС) на фоне терапии ингибиторами АПФ возможно изменение функции почек: развитие олигурии и/или прогрессирующей азотемии, а в редких случаях - ОПН и/или летальный исход. Препарат Вальсакор блокирует рецепторы ангиотензина II, поэтому у пациентов с ХСН необходим регулярный контроль функции почек. Ангионевротический отек в анамнезе Среди пациентов с ангионевротическим отеком на фоне терапии препаратом Вальсакор, наблюдались случаи развития ангионевротического отека в анамнезе, в том числе и на ингибиторы АПФ. При развитии ангионевротического отека следует немедленно отменить препарат и исключить возможность повторного применения. Специальная информация по вспомогательным веществам Препарат Вальсакор содержит лактозу, поэтому не следует применять при следующих состояниях: непереносимость лактозы, дефицит лактазы, синдром глюкозо-галактозной мальабсорбции. Влияние на способность управлять транспортными средствами: В связи с возможностью возникновения головокружения или слабости на фоне применения препарата Вальсакор необходимо соблюдать осторожность при управлении транспортными средствами и занятии потенциально опасными видами деятельности. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25 °С, в оригинальной упаковке. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Вальсакор Международное непатентованное название:Валсартан. Форма выпуска:таблетки, покрытые пленочной оболочкой. Состав:на 1 таблетку 40 мг, покрытую пленочной оболочкой: Ядро: Действующее вещество: валсартан 40,00 мг: Вспомогательные вещества: лактозы моногидрат 15,00 мг, целлюлоза микрокристаллическая 20,50 мг, повидон-К25 0,75 мг, кроскармеллоза натрия 1,00 мг, кремния диоксид коллоидный 0,50 мг, магния стеарат 2,25 мг. Оболочка пленочная: гипромеллоза 6ср 1,38 мг, титана диоксид (Е171) 0,27 мг, краситель железа оксид желтый (Е172) 0,20 мг, макрогол-4000 0,15 мг. на 1 таблетку 80 мг, покрытую пленочной оболочкой: Ядро: Действующее вещество: валсартан 80,00 мг: Вспомогательные вещества: лактозы моногидрат 30,00 мг, целлюлоза микрокристаллическая 41,00 мг, повидон-К25 1,50 мг, кроскармеллоза натрия 2,00 мг, кремния диоксид коллоидный 1,00 мг, магния стеарат 4,50 мг. Оболочка пленочная: гипромеллоза 6ср 3,00 мг, титана диоксид (Е171) 0,68 мг, краситель железа оксид красный (Е172) 0,02 мг, макрогол-4000 0,30 мг. на 1 таблетку 160 мг, покрытую пленочной оболочкой: Ядро: Действующее вещество: валсартан 160,00 мг: Вспомогательные вещества: лактозы моногидрат 60,00 мг, целлюлоза микрокристаллическая 82,00 мг, повидон-К25 3,00 мг, кроскармеллоза натрия 4,00 мг, кремния диоксид коллоидный 2,00 мг, магния стеарат 9,00 мг. Оболочка пленочная: гипромеллоза 6ср 5,52 мг, титана диоксид (Е171) 1,36 мг, краситель железа оксид желтый (Е172) 0,50 мг, краситель железа оксид красный (Е172) 0,02 мг, макрогол-4000 0,60 мг АТХ: Регистрация: Лекарственное средство ЛСР-004921/08 Фармгруппа: Ангиотензина II рецепторов антагонист. Дата регистрации: 25.06.2008 / 24.11.2014. Окончание регстрации: . Описание:Таблетки 40 мг: круглые, слегка двояковыпуклые таблетки с риской на одной стороне, покрытые пленочной оболочкой коричневато-желтого цвета. Вид на изломе: белая шероховатая масса с пленочной оболочкой коричневато-желтого цвета. Таблетки 80 мг: круглые, двояковыпуклые таблетки с риской на одной стороне, покрытые пленочной оболочкой розового цвета. Вид на изломе: белая шероховатая масса с пленочной оболочкой розового цвета. Таблетки 160 мг: овальные, двояковыпуклые таблетки с риской на одной стороне, покрытые пленочной оболочкой коричневато-желтого цвета. Вид на изломе: белая шероховатая масса с пленочной оболочкой коричневато-желтого цвета. Упаковка:Таблетки, покрытые пленочной оболочкой, 40 мг, 80 мг и 160 мг. По 7, 10, 14 или 15 таблеток в блистере (контурной ячейковой упаковке) из комбинированного материала ПВХ/ПЭ/ПВДХ - алюминиевой фольги. По 2, 4, 8, 12, 14 или 20 блистеров (контурных ячейковых упаковок) (по 7 таблеток), или по 2, 3, 6 или 9 блистеров (контурных ячейковых упаковок) (по 10 таблеток), или по 1,2, 4, 6, 7 или 10 блистеров (контурных ячейковых упаковок) (по 14 таблеток), или по 2, 4 или 6 блистеров (контурных ячейковых упаково
Модель:
RUR 583
Показания Язвенная болезнь желудка в стадии обострения и язва анастомоза: Язвенная болезнь двенадцатиперстной кишки в стадии обострения: Эрозивная и язвенная гастроэзофагеальная рефлюксная болезнь или рефлюкс- эзофагит: Поддерживающая терапия гастроэзофагеальной рефлюксной болезни: Неэрозивная гастроэзофагеальная рефлюксная болезнь: Синдром Золлингера-Эллисона и другие состояния, характеризующиеся патологической гиперсекрецией: В комбинации с соответствующей антибактериальной терапией для Helicobacter pilory у пациентов с язвенной болезнью. Противопоказания Противопоказания Гиперчувствительность к рабепразолу, замещенным бензимидазолам или другим вспомогательным компонентам препарата: беременность: период лактации: детский возраст (до 12 лет). С осторожностью: Тяжелая печеночная недостаточность, тяжелая почечная недостаточность. Беременность Рабепразол не следует назначать беременным женщинам (данных по безопасности применения рабепразола во время беременности нет). На время лечения следует прекратить грудное вскармливание. Неизвестно, выделяется ли рабепразол с грудным молоком. Соответствующие исследования у кормящих женщин не проводились. Применение и дозы Таблетки препарата Хайрабезол нельзя разжевывать или измельчать. Таблетки следует глотать целиком. Установлено, что ни время суток, ни прием пищи не влияют на активность рабепразола. При язвенной болезни желудка в стадии обострения и язве анастомоза рекомендуется принимать внутрь по 10 мг или по 20 мг один раз в день. Обычно излечение наступает после 6 недель терапии, однако в некоторых случаях длительность лечения может быть увеличена еще на 6 недель. При язвенной болезни двенадцатиперстной кишки в стадии обострения рекомендуется принимать внутрь по 20 мг один раз в день. В некоторых случаях лечебный эффект наступает при приеме 10 мг один раз в день. Длительность лечения составляет от 2 до 4 недель. В случае необходимости длительность лечения может быть увеличена еще на 4 недели. При лечении эрозивной гастроэзофагеальной рефлюксной болезни (ГЭРБ) или рефлюкс эзофагите рекомендуется принимать внутрь по 10 мг или по 20 мг один раз в день. Длительность лечения составляет от 4 до 8 недель. В случае необходимости длительность лечения может быть увеличена еще на 8 недель. При поддерживающей терапии гастроэзофагеальной рефлюксной болезни (ГЭРБ) рекомендуется принимать внутрь по 10 мг или по 20 мг один раз в день. Длительность лечения зависит от состояния пациента. При неэрозивной гастроэзофагеальной рефлюксной болезни (НЭРБ) без эзофагита рекомендуется принимать внутрь по 10 мг или по 20 мг один раз в день. Если после четырех недель лечения симптомы не исчезают, следует провести дополнительное исследование пациента. После купирования симптомов для предупреждения их последующего возникновения следует принимать препарат внутрь в дозе 10 мг один раз в день по требованию. Для лечения синдрома Золлингеуа-Элисона и других состояний, характеризующихся патологической гиперсекрецией, дозу подбирают индивидуально. Начальная доза - 60 мг в день, затем дозу повышают и назначают препарат в дозе до 100 мг в день при однократном приеме или по 60 мг два раза в день. Для некоторых пациентов дробное дозирование препарата является предпочтительным. Лечение должно продолжаться по мере клинической необходимости. У некоторых больных с синдромом Золлингера-Элисона длительность лечения рабепразолом составляет до одного года. Для лечения язвенной болезни двенадиатиперстной кишки или хронического гастрита, связанного с инфицированием Н. pylori, рекомендуется курс лечения длительностью 7 дней одной из следующих комбинаций препаратов: Хайрабезол по 20 мг 2 раза в день + кларитромицин по 500 мг 2 раза в день и амоксициллин по 1г. 2 раза в день. Хайрабезол по 20 мг 2 раза в день + кларитромицин по 500 мг 2 раза в день и метронидазол по 400 мг 2 раза в день. Пациенты с почечной и печеночной недостаточностью Коррекции дозы пациентам с почечной недостаточностью не требуется. У пациентов с легкой и умеренной степенью печеночной недостаточности концентрация рабепразола в крови обычно выше, чем у здоровых пациентов. При назначении препарата Хайрабезол пациентам с тяжелой степенью печеночной недостаточности следует соблюдать осторожность. Пожилые пациенты Коррекции дозы не требуется. Дети. Безопасность и эффективность рабепразола 20 мг для краткосрочного (до 8 недель) лечения ГЭРБ у детей в возрасте 12 лет и более подтверждена экстраполяцией результатов адекватных и хорошо контролируемых исследований, подкрепляющих эффективность рабепразола для взрослых и исследованиями безопасности и фармакокинетики для пациентов детского возраста. Рекомендуемая доза для детей в возрасте 12 лет и более составляет 20 мг 1 раз в день продолжительностью до 8 недель. Безопасность и эффективность рабепразола для лечения ГЭРБ у детей в возрасте младше 12 лет не установлена. Безопасность и эффективность рабепразола для применения по другим показаниям не установлена для пациентов детского возраста. Побочные эффекты и передозировка Побочные эффекты: Исходя из опыта клинических испытаний, можно сделать вывод, что рабепразол обычно хорошо переносится пациентами. Побочные эффекты в целом слабо выраженные или умеренные и носят преходящий характер. При приеме рабепразола в ходе клинических исследований отмечались следующие побочные действия: головная боль, боль в животе, диарея, метеоризм, запор, сухость во рту, головокружение, сыпь, периферический отек. В ходе пострегистрационного применения рабепразола сообщалось о следующих побочных эффектах: повышение уровня печеночных ферментов, редко - гепатит и желтуха. У пациентов с циррозом печени редко сообщалось о развитии печеночной энцефалопатии. Также в редких случаях отмечались тромбоцитопения, нейтропения, лейкопения, буллезные высыпания, крапивница,острые системные аллергические реакции, миалгия, артралгия, гипомагниемия. Очень редко сообщалось о развитии интерстициального нефрита, гинекомастии, мультиформной эритемы, токсического эпидермального некролиза, синдрома Стивенса-Джонсона. Согласно данным постмаркетингового наблюдения при приеме ингибиторов протонной помпы возможно увеличение риска возникновения переломов (см. раздел "Особые указания") Передозировка: Симптомы: Данные о намеренной или случайной передозировке минимальны. Случаев сильной передозировки рабепразолом не было отмечено. Лечение: Специфический антидот для рабепразола неизвестен. Рабепразол хорошо связывается с белками плазмы, и поэтому слабо выводится при диализе. При передозировке необходимо проводить симптоматическое и поддерживающее лечение. Взаимодействие с другими ЛС: Рабепразол замедляет выведение некоторых лекарственных средств, метаболизирующихся в печени путем микросомального окисления (диазепам, фенитоин, непрямые антикоагулянты). Снижает концентрацию кетоконазола на 33%, дигоксина - на 22%. Не взаимодействует с жидкими антацидами. Совместим с препаратами, метаболизирующимися системой CYP450 (варфарин, фенитоин, теофиллин, диазепам). Фармакологическое действие и фармакокинетика Противоязвенное средство из группы ингибиторов протонного насоса (Н+/К-АТФ-азы), метаболизируется в париетальных клетках желудка до активных сульфонамидных производных, которые инактивируют сульфгидрильные группы Н+/К-АТФ-азы. Блокирует заключительную стадию секреции хлористоводородной кислоты, снижая содержание базальной и стимулированной секреции, независимо от природы раздражителя. Обладает высокой липофильностью, легко проникает в париетальные клетки желудка и концентрируется в них, оказывая цитопротекторное действие. Антисекреторный эффект после перорального приема 20 мг наступает в течение 1 ч и достигает максимума через 2-4 ч: угнетение базальной и стимулированной пищей секреции кислоты через 23 ч после приема первой дозы составляет 62% и 82%, соответственно: продолжительность действия - 48 ч. После окончания приема секреторная активность нормализуется в течение 2-3 дней. В первые 2-8 недель терапии концентрация гастрина в сыворотке крови увеличивается и возвращается к исходным уровням в течение 1-2 недель после отмены препарата. Не влияет на центральную нервную систему, сердечно-сосудистую и дыхательную системы. Фармакокинетика: Абсорбция происходит в тонком кишечнике (из-за наличия кислотоустойчивой кишечнорастворимой оболочки) высокая, время достижения максимальной концентрации - 3,5 ч. Значения максимальной концентрации (Сmах) и площади под кривой "концентрация действующего вещества - время" (AUC) носят линейный характер в диапазоне доз от 10 до 40 мг. Метаболизируется в печени с участием изоферментов цитохрома Р-450 CYP2C19 и CYP3A4. Биодоступность - 52%, не увеличивается при многократном приеме. Период полувыведения (T1/2) - 0,7-1,5 ч, клиренс - 283 ± 98 мл/мин. У пациентов с хронической печеночной недостаточностью слабой или средней степени после однократного приема AUC увеличивается в 2 раза, Т1/2 - в 2-3 раза. После приема 20 мг рабепразола в течение 7 дней AUC увеличивается в 1,5 раза, Т1/2 - в 1,2 раза. У пациентов со стабильной терминальной стадией почечной недостаточности, нуждающихся в гемодиализе (клиренс креатинина менее 5 мл/мин/1,73 м 2), распределение рабепразола натрия близко к таковому у здоровых лиц. У пожилых пациентов после приема рабепразола в течение 7 дней AUC в 2 раза больше, Сmах - на 60% больше, чем у молодых. Связь с белками плазмы - 97%. Выводится почками - 90% в виде двух метаболитов: конъюгата меркаптуровой кислоты (М5) и карбоновой кислоты (Мб): кишечником - 10%. У пациентов с замедленным метаболизмом CYP2C19 после 7 дней приема рабепразола в дозе 20 мг в сутки AUC увеличивается в 1,9 раза, а период полувыведения в 1,6 раза по сравнению с теми же параметрами у "быстрых метаболизаторов", в то время как Сmах увеличивается на 40 %. Особые указания Ответ пациента на терапию рабепразолом не исключает наличие злокачественных новообразований в желудке. Таблетки препарата Хайрабезол нельзя разжевывать или измельчать. Таблетки следует глотать целиком. Установлено, что ни время суток, ни прием пищи не влияют на активность рабепразола. В специальном исследовании у пациентов с легкими или умеренными нарушениями функции печени не было обнаружено значимого отличия частоты побочных эффектов рабепразола от таковой у подобранных по полу и возрасту здоровых лиц, но, несмотря на это, рекомендуется соблюдать осторожность при первом назначении пациентам с тяжелыми нарушениями функции печени. Пациентам с нарушениями функции почек или печени корректировка дозы препарата Хайрабезол не требуется. AUC рабепразола у пациентов с тяжелым нарушением функции печени примерно в два раза выше, чем у здоровых пациентов. Гипомагниемия. При лечении ингибиторами протонной помпы на протяжении, по крайней мере, 3 месяцев в редких случаях были отмечены случаи симптоматической или асимптоматической гипомагниемии. В большинстве случаев эти сообщения поступали через год после проведения терапии. Серьезными побочными явлениями были тетания, аритмия и судороги. Большинству пациентов требовалось лечение гипомагниемии, включающее замещение магния и отмену терапии ингибиторами протонной помпы. У пациентов, которые будут получать длительное лечение или которые принимают ингибиторы протонной помпы с препаратами, такими как дигоксин или препаратами, которые могут вызвать гипомагниемию (например, диуретики), медицинские работники должны контролировать уровень магния до начала лечения ингибиторами протонной помпы и в период лечения. Переломы. Согласно данным наблюдательных исследований можно предположить, что терапия ингибиторами протонной помпы может привести к возрастанию риска, связанного с остеопорозом переломов бедра, запястья, позвоночника. Риск переломов был увеличен у пациентов, принимавших высокие дозы ингибиторов протонной помпы в течение года и более. Влияние на способность управлять транспортными средствами: В случае появления в процессе лечения сонливости следует отказаться от управления автомобилем и других видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций. Условия хранения и отпуска из аптек Условия хранения: В сухом, защищенном от света месте, при температуре от 8 °С до 25 °С. Хранить в недоступном для детей месте Отпуск из аптек: По рецепту Регистрационные данные Торговое название Хайрабезол® Международное непатентованное название:Рабепразол. Форма выпуска:таблетки покрытые кишечнорастворимой пленочной оболочкой. Состав:Дозировка 10 мг: Активный ингредиент: рабепразол натрия - 10 мг. Вспомогательные ингредиенты: магния оксид 50 мг, маннитол 17,5 мг, крахмал кукурузный 2,5 мг, повидон-КЗО 1,5 мг, гипролоза низкозамещенная 16 мг, натрия стеарилфумарат 2мг. Оболочка: целлацефат 11,25 мг, титана диоксид 1 мг, краситель железа оксид красный 0,1 мг. Дозировка 20 мг: Активный ингредиент: рабепразол натрия - 20 мг. Вспомогательные ингредиенты: магния оксид 69 мг, маннитол 40 мг, крахмал кукурузный 2,5 мг, повидон-КЗО 1,5 мг, гипролоза низкозамещенная 24 мг, натрия стеарилфумарат 2 мг. Оболочка: целлацефат 18 мг, титана диоксид 1,6 мг, краситель железа оксид желтый 0,16 мг АТХ: Регистрация: ЛП-001479 Фармгруппа: средство, понижающее секрецию желез желудка - протонного насоса ингибитор. Дата регистрации: 06.02.2012. Окончание регстрации: . Описание:Дозировка 10 мг: круглые двояковыпуклые таблетки, покрытые оболочкой от светло-розового до красновато-розового цвета. На поперечном разрезе ядро белого или белого с желтоватым оттенком цвета. Дозировка 20 мг:круглые двояковыпуклые таблетки, покрытые оболочкой от светло-желтого до желтого цвета. На поперечном разрезе ядро белого или белого с желтоватым оттенком цвета. Упаковка:таблетки покрытые кишечнорастворимой пленочной оболочкой 10мг и 20мг. Для аптек: 10, 14, 15 таблеток в Ал/Ал блистер или в Ал/Ал стрип. 1 или 10 стрипов/блистеров по 10 таблеток, 1 или 2 стрипа/блистера по 14 таблеток, 1, 2 или 10 стрипов/блистеров по 15 таблеток вместе с инструкцией по применению в пачку картонную. 1 стрип/блистер по 14 или 15 таблеток вместе с инструкцией по применению в пачку картонную с клапаном и перфорацией, защищенной пленкой ПВХ с внутренней стороны пачки (7 перфораций в виде круга). Для стационаров: 100, 500, 1000 таблеток в пакет из полиэтилена. пакет вместе с инструкцией по применению в банку из полиэтилена высокой плотности. На банку наклеивают этикетку. Срок годности:2 года. Не использовать по истечению срока годности указанного на упаковке. Владелец рег.удостоверения:Хайгланс Лабораториз Пвт. Лтд. Производитель:HIGLANCE LABORATORIES Pvt. Ltd. Представительство:ХАЙГЛАНС ЛАБОРАТОРИЗ
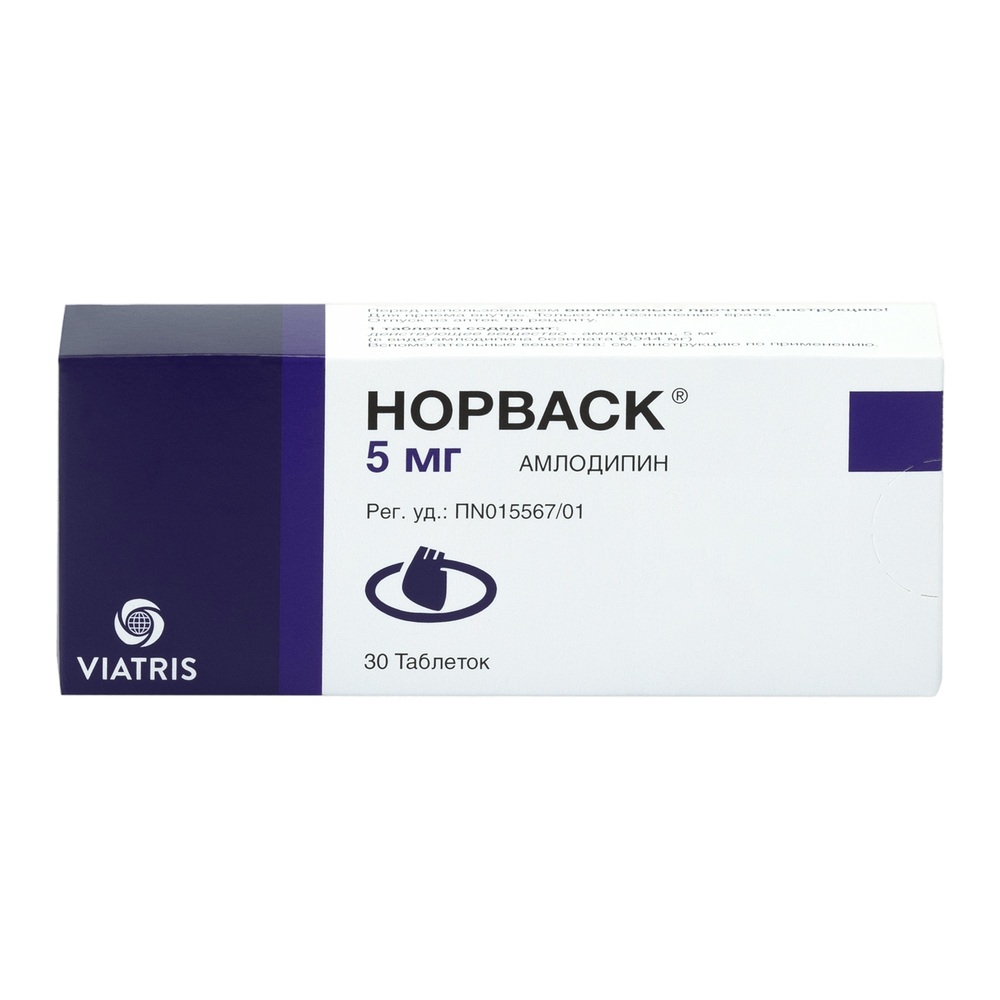
Модель:
RUR 174
Показания Артериальная гипертензия (как в монотерапии, гак и в сочетании с другими гипотензивными средствами). - Стабильная стенокардия и вазоспастическая стенокардия (стенокардия Принцметала или вариантная стенокардия) как в монотерапии, так и в сочетании с другими антиангинальными средствами. Противопоказания Противопоказания - Повышенная чувствительность к амлодипину и другим производным дигидропиридина, а также вспомогательным веществам, входящим в состав препарата. - Тяжелая артериальная гипотензия (систолическое АД менее 90 мм рт.ст.). - Обструкция выносящего тракта левого желудочка (включая, тяжелый аортальный стеноз). - Шок (включая кардиогенный) - Гемодинамически нестабильная сердечная недостаточность после инфаркта миокарда. - Возраст до 18 лет (эффективность и безопасность не установлены). С осторожностью: С ОСТОРОЖНОСТЬЮ применять у пациентов с печеночной недостаточностью, ХСН неишемической этиологии III-IV функционального класса по классификации NYHA, нестабильной стенокардией, аортальным стенозом, митральным стенозом, гипертрофической обструктивной кардиомиопатией, острым инфарктом миокарда (и в течение 1 мес после него), синдромом слабости синусового узла (выраженная тахикардия, брадикардия), артериальной гипотензией, при одновременном применении с ингибиторами или индукторами изофермента CYP3A4. Беременность Безопасность применения препарата Норваск® во время беременности не установлена, поэтому применение во время беременности возможно только в случае, когда польза для матери превышает риск для плода и новорожденного. Данные, свидетельствующие о выделении амлодипина в грудное молоко, отсутствуют. Однако известно, что другие БМКК - производные дигидропиридина, выделяются в грудное молоко. В связи с чем, при необходимости применения препарата Норваск® в период лактации следует решить вопрос о прекращении грудного вскармливания. Не было выявлено влияния амлодипина на фертильность при исследовании на крысах. Применение и дозы Внутрь, один раз в сутки, запивая необходимым количеством воды (100 мл). При артериальной гипертензии, стенокардии обычно начальная доза составляет 5 мг, в зависимости от терапевтического ответа ее можно увеличить до максимальной суточной дозы - 10 мг. Применение у пожилых пациентов Норваск® рекомендуется применять в средней терапевтической дозе, коррекции дозы не требуется. Применение у пациентов с нарушенной функцией печени Несмотря на то, что Т1/2 Норваска®, как и всех БМКК, увеличивается у пациентов с нарушениями функции печени, коррекции дозы обычно не требуется (см. раздел "Особые указания"). Применение у пациентов с нарушенной функцией почек Рекомендуется применять Норваск® в обычных дозах, однако необходимо учитывать возможное незначительное увеличение Т1/2. Нс требуется коррекции дозы при одновременном применении с тиазидными диуретиками, бета-адреноблокаторами и ингибиторами ангиотензинпревращающего фермента. Побочные эффекты и передозировка Побочные эффекты: Частота побочных реакций, приведенных ниже, определялась соответственно следующему (классификация Всемирной организации здравоохранения): очень часто - более 1/10часто - от более 1/100 до менее 1/10нечасто - от более 1/1000 до менее 1/100,редко - от более 1/10000 до менее 1/1000,очень редко - от менее 1/10000, включая отдельные сообщения,неизвестно - невозможно оценить частоту на основании имеющихся данных. Со стороны сердечно-сосудистой системы: часто - ощущение сердцебиения, периферические отеки (лодыжек и стоп), "приливы" крови к коже лица: нечасто - чрезмерное снижение АД: очень редко - обморок, одышка, васкулит, ортостатическая гипотензия, развитие или усугубление течения ХСН, нарушения ритма сердца (включая брадикардию, желудочковую тахикардию и мерцание предсердий), инфаркт миокарда, боль в грудной клетке. Со стороны опорно-двигательного аппарата: нечасто - артралгия, судороги мышц, миалгия, боль в спине, артроз, редко - миастения. Со стороны нервной системы: часто - головные боли, головокружение, повышенная утомляемость, сонливость: нечасто - астения, общее недомогание, гипестезия, парестезия, периферическая нейропатия, тремор, бессонница, лабильность настроения, необычные сновидения, повышенная возбудимость, депрессия, тревога, звон в ушах, извращение вкуса: очень редко - мигрень, повышенное потоотделение, апатия, ажитация, атаксия, амнезия: неизвестно - экстрапирамидные нарушения. Со стороны пищеварительной системы: часто - тошнота, боли в животе: нечасто - рвота, запор или диарея, метеоризм, диспепсия, анорексия, сухость слизистой оболочки полости рта, жажда: редко - гиперплазия десен, повышение аппетита: очень редко - панкреатит, гастрит, желтуха (обусловленные холестазом), гипербилирубинемия, повышение активности "печеночных" трансаминаз, гепатит. Со стороны органов кроветворения: очень редко - тромбоцитопеническая пурпура, лейкопения, тромбоцитопения. Со стороны дыхательной системы: нечасто - одышка, ринит, носовое кровотечение: очень редко - кашель. Со стороны органов чувств: нечасто - диплопия, нарушение аккомодации, ксерофтальмия, конъюнктивит, боль в глазах, нарушения зрения: Со стороны мочеполовой системы: нечасто - учащенное мочеиспускание, болезненное мочеиспускание, никтурия, нарушение эректильной функции: очень редко - дизурия, полиурия. Со стороны кожных покровов: редко - дерматит: очень редко - алопеция, ксеродермия, холодный нот, нарушение пигментации кожи. Метаболические нарушения: очень редко - гипергликемия: нечасто - увеличение/снижение массы тела Аллергические реакции: нечасто - кожный зуд, сыпь (в т.ч. эритематозная, макулопапулезная сыпь, крапивница), очень редко - ангионевротический отек, мультиформная эритема. Лабораторные показатели: очень редко - гипергликемия. Прочие: нечасто - озноб, гинекомастия, боль неуточненной локализации: очень редко - паросмия. Передозировка: Симптомы: выраженное снижение АД с возможным развитием рефлекторной тахикардии и чрезмерной периферической вазодилатации (риск развития выраженной и стойкой артериальной гипотензии, в т.ч. с развитием шока и летального исхода). Лечение: промывание желудка, назначение активированного угля (особенно в первые 2 ч после передозировки), поддержание функции сердечно-сосудистой системы, возвышенное положение нижних конечностей, мониторинг показателей работы сердца и легких, контроль объема циркулирующей крови (ОЦК) и диуреза. Для восстановления тонуса сосудов - применение сосудосуживающих средств (при отсутствии противопоказаний к их применению): для устранения последствий блокады кальциевых каналов - внутривенное введение глюконата кальция. Гемодиализ неэффективен. Взаимодействие с другими ЛС: Амлодипин может безопасно применяться для терапии артериальной гипертензии вместе с тиазидными диуретиками, альфа-адреноблокаторами, бета-адреноблокаторами или ингибиторами АПФ. У пациентов со стабильной стенокардией амлодипин можно комбинировать с другими антиангинальными средствами, например, с нитратами пролонгированного или короткого действия, бета-адреноблокаторами. В отличие от других БМКК клинически значимого взаимодействия амлодипина (III поколение БМКК) не было обнаружено при совместном применении с нестероидными противовоспалительными препаратами (НПВП), в том числе и с индометацином. Возможно усиление антиангинального и гипотензивного действия БМКК при совместном применении с тиазидными и "петлевыми" диуретиками, ингибиторами АПФ, бета-адреноблокаторами и нитратами, а так же усиление их гипотензивного действия при совместном применении с альфа 1-адреноблокаторами, нейролептиками. Хотя при изучении амлодипина отрицательного инотропного действия обычно не наблюдали, тем не менее, некоторые БМКК могут усиливать выраженность отрицательного инотропного действия антиаритмических средств, вызывающих удлинение интервала QT (например, амиодарон и хинидин). Амлодипин может также безопасно применяться одновременно с антибиотиками и гипогликемическими средствами для приема внутрь. Однократный прием 100 мг силденафила у пациентов с эссенциальной гипертензией не оказывает влияния на параметры фармакокинетики амлодипина. Повторное применение амлодипина в дозе 10 мг и аторвастатина в дозе 80 мг не сопровождается значительными изменениями показателей фармакокинетики аторвастатина. Симвастатин: одновременное многократное применение амлодипина в дозе 10 мг и симвастатина в дозе 80 мг приводит к повышению экспозиции симвастатина на 77 %. В таких случаях следует ограничить дозу симвастатина до 20 мг. Этанол (напитки, содержащие алкоголь): амлодипин при однократном и повторном применении в дозе 10 мг нс влияет на фармакокинетику этанола. Противовирусные средства (ритонавир): увеличивает плазменные концентрации БМКК, в том числе и амлодипина. Нейролептики и изофлуран: усиление гипотензивного действия производных дигидропиридина. Препараты кальция могут уменьшить эффект БМКК. При совместном применении БМКК с препаратами лития (для амлодипина данные отсутствуют), возможно, усиление проявления их нейротоксичности (тошнота, рвота, диарея, атаксия, тремор, шум в ушах). Исследования одновременного применения амлодипина и циклоспорина у здоровых добровольцев и всех групп пациентов, за исключением пациентов после трансплантации почки, не проводились. Различные исследования взаимодействия амлодипина с циклоспорином у пациентов после трансплантации почки показывают, что применение данной комбинации может не приводить к какому-либо эффекту, либо повышать минимальную концентрацию циклоспорина в различной степени до 40 %. Следует принимать во внимание эти данные и контролировать концентрацию циклоспорина у этой группы пациентов при одновременном применении циклоспорина и амлодипина. Не оказывает влияние на концентрацию в сыворотке крови дигоксина и его почечный клиренс. Не оказывает существенного влияния на действие варфарина (протромбиновое время). Циметидин не влияет на фармакокинетику амлодипина. В исследованиях in vitro амлодипин не влияет на связывание с белками плазмы крови дигоксина, фенитоина, варфарина и индометацина. Грейпфрутовый сок: одновременный однократный прием 240 мг грейпфрутового сока и 10 мг амлодипина внутрь не сопровождается существенным изменением фармакокинетики амлодипина. Тем не менее, не рекомендуется применять грейпфрутовый сок и амлодипин одновременно, гак как при генетическом полиморфизме изофермента CYP3A4 возможно повышение биодоступности амлодипина и, вследствие этого, усиление гипотензивного эффекта. Алюминий- или магнийсодержащие антациды: их однократный прием не оказывает существенного влияния на фармакокинетику амлодипина. Ингибиторы изофермента CYP3A4: при одновременном применении дилтиазема в дозе 180 мг и амлодипина в дозе 5 мг у пациентов от 69 до 87 лет с артериальной гипертензией, отмечается повышение системной экспозиции амлодипина на 57 %. Одновременное применение амлодипина и эритромицина у здоровых добровольцев (от 18 до 43 лет) не приводит к значительным изменениям экспозиции амлодипина (увеличение площади под кривой "концентрация-время" (AUC) на 22 %). Несмотря на то, что клиническое значение этих эффектов до конца не ясно, они могут быть более ярко выражены у пожилых пациентов. Мощные ингибиторы изофермента CYP3A4 (например, кетоконазол, итраконазол) могут приводить к увеличению концентрации амлодипина в плазме крови в большей степени, чем дилтиазем. Следует с осторожностью применять амлодипин и ингибиторы изофермента CYP3A4. Кларитромицин: ингибитор изофермента CYP3A4. У пациентов, принимающих одновременно кларитромицин и амлодипин, повышен риск снижения артериального давления. Пациентам, принимающим такую комбинацию, рекомендуется находиться под тщательным медицинским наблюдением. Индукторы изофермента CYP3A4: данных о влиянии индукторов изофермента CYP3A4 на фармакокинетику амлодипина нет. Следует тщательно контролировать артериальное давление при одновременном применении амлодипина и индукторов изофермента CYP3A4. Такролимус: при одновременном применении с амлодипином есть риск увеличения концентрации такролимуса в плазме крови. Для того чтобы избежать токсичности такролимуса при одновременном применении с амлодипином, следует контролировать концентрацию такролимуса в плазме крови пациентов и корректировать дозу такролимуса в случае необходимости. Фармакологическое действие и фармакокинетика Производное дигидропиридина - блокатор "медленных" кальциевых каналов (БМКК), оказывает гипотензивное и антиангинальное действие. Блокирует "медленные" кальциевые каналы, снижает трансмембранный переход ионов кальция в клетку (в большей степени в гладкомышечные клетки сосудов, чем в кардиомиоциты). Антиангинальное действие обусловлено расширением коронарных и периферических артерий и артериол: - при стенокардии уменьшает выраженность ишемии миокарда: расширяя периферические артериолы, снижает общее периферическое сосудистое сопротивление, уменьшает постнагрузку на сердце, снижает потребность миокарда в кислороде: - расширяя коронарные артерии и артериолы в неизмененных и в ишемизированных зонах миокарда, увеличивает поступление кислорода в миокард (особенно при вазоспастической стенокардии): предотвращает спазм коронарных артерий (вт.ч. вызванной курением). У пациентов стабильной стенокардией разовая суточная доза увеличивает толерантность к физической нагрузке, замедляет развитие приступов стенокардии и "ишемической" депрессии сегмента ST, снижает частоту приступов стенокардии и потребления нитроглицерина и других нитратов. Оказывает длительное дозозависимое гипотензивное действие. Гипотензивное действие обусловлено прямым вазодилатирующим влиянием на гладкие мышцы сосудов. При артериальной гипертензии разовая доза обеспечивает клинически значимое снижение артериального давления (АД) на протяжении 24 ч (в положении больного "лежа" и "стоя"). Ортостатическая гипотензия при применении амлодипина встречается достаточно редко. Амлодипин не вызывает снижения толерантности к физической нагрузке, фракции выброса левого желудочка. Уменьшает степень гипертрофии миокарда левого желудочка. Не оказывает влияния на сократимость и проводимость миокарда, не вызывает рефлекторного увеличения частоты сердечных сокращений (ЧСС), тормозит агрегацию тромбоцитов, увеличивает скорость клубочковой фильтрации, обладает слабым натрийуретическим действием. При диабетической нефропатии не увеличивает выраженность микроальбуминурии. Не оказывает какого-либо неблагоприятного влияния на обмен веществ и концентрацию липидов плазмы крови и может применяться при терапии пациентов с бронхиальной астмой, сахарным диабетом и подагрой. Значимое снижение АД наблюдается через 6-10 ч. длительность эффекта - 24 ч. У пациентов с заболеваниями сердечно-сосудистой системы (включая коронарный атеросклероз с поражением одного сосуда и до стеноза 3-х и более артерий, атеросклероз сонных артерий), перенесших инфаркт миокарда, чрескожную транслюминальную коронарную ангиопластику (ЧТКА) или у пациентов со стенокардией, применение амлодипина предупреждает развитие утолщения интимы-медии сонных артерий, снижает летальность от инфаркта миокарда, инсульта, ЧТКА, аорто-коронарного шунтирования: приводит к снижению числа госпитализаций по поводу нестабильной стенокардии и прогрессирования хронической сердечной недостаточности (ХСН): снижает частоту вмешательств, направленных на восстановление коронарного кровотока. Не повышает показатель смертности или развития осложнений и летальных исходов у пациентов с ХСН (III-IV функциональный класс по классификации NYHA) на фоне терапии дигоксином, диуретиками и ингибиторами ангиотензинпревращающего фермента (АПФ). У пациентов с ХСН (III-IV функциональный класс по классификации NYHA) неишемической этиологии при применении амлодипина существует вероятность возникновения отека легких. Фармакокинетика: Подле приема внутрь амлодипин хорошо абсорбируется из желудочно-кишечного тракта. Средняя абсолютная биодоступность составляет 64-80 %, максимальная концентрация в сыворотке крови определяется через 6-12 ч. Равновесные концентрации достигаются подле 7-8 дней терапии. Одновременный прием пищи не влияет на абсорбцию амлодипина. Средний объем распределения составляет 21 л/кг массы тела, что указывает на то, что большая часть препарата находится в тканях, а меньшая - в крови. Большая часть препарата, находящегося в крови (97,5 %) связывается с белками плазмы крови. Амлодипин подвергается медленному, но активному метаболизму в печени при отсутствии значимого эффекта "первичного прохождения" через печень. Метаболиты не обладают существенной фармакологической активностью. После однократного приема период полувыведения (T1/2) варьирует от 35 до 50 ч. при повторном назначении T1/2 составляет приблизительно 45 ч. Около 60 % принятой внутрь дозы выводится почками преимущественно в виде метаболитов, 10 % - в неизмененном виде, а 20-25 % - через кишечник с желчью. Общий клиренс амлодипина составляет 0,116 мл/с/кг (7 мл/мин./кг. 0,42 л/ч/кг). Применение у пожилых пациентов У пожилых пациентов (старше 65 лет) выведение амлодипина замедлено (T1/2 - 65 ч) по сравнению с молодыми пациентами, однако эта разница не имеет клинического значения. Применение у пациентов с печеночной недостаточностью Удлинение T1/2 у пациентов с печеночной недостаточностью предполагает, что при длительном применении кумуляция препарата в организме будет выше (T1/2 - до 60 ч). Применение у пациентов с почечной недостаточностью Почечная недостаточность не оказывает существенного влияния на кинетику амлодипина. Амлодипин проникает через гематоэнцефалический барьер. При гемодиализе не удаляется. Особые указания Необходимо поддержание гигиены зубов и наблюдение у стоматолога (для предотвращения болезненности, кровоточивости и гиперплазии десен). У пациентов пожилого возраста может увеличиваться T1/2 и снижаться клиренс препарата. Изменения доз не требуется, но необходимо более тщательное наблюдение за пациентами данной категории. Эффективность и безопасность применения препарата Норваск® при гипертоническом кризе не установлена. Несмотря на отсутствие у БМКК синдрома "отмены", прекращение лечения препаратом Норваск® желательно проводить, постепенно уменьшая дозу препарата. На фоне применения Норваска® у пациентов с хронической сердечной недостаточностью класс III и IV функционального класса по классификации NYHA неишемического генеза, отмечалось повышение частоты развития отека легких, несмотря на отсутствие признаков ухудшения сердечной недостаточности. Влияние на способность управлять транспортными средствами: Хотя на фоне применения препарата Норваск® какого-либо отрицательного влияния на способность управлять автотранспортом или другими сложными механизмами не наблюдалось, однако, вследствие возможного чрезмерного снижения АД, развития головокружения, сонливости и других побочных реакций, следует соблюдать осторожность в перечисленных ситуациях, особенно в начале лечения и при увеличении дозы. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25 °С. Хранить в недоступном для детей месте! Отпуск из аптек: По рецепту Регистрационные данные Торговое название Норваск® Международное непатентованное название:Амлодипин. Форма выпуска:таблетки. Состав:Состав 1 таблетка дозировкой 5 мг содержит: Активное вещество: амлодипин - 5 мг (в виде амлодипина безилата - 6,944 мг). Вспомогательные вещества: целлюлоза микрокристаллическая - 124,056 мг, кальция гидрофосфат - 63 мг, карбоксиметилкрахмал натрия - 4 мг, магния стеарат - 2 мг. 1 таблетка дозировкой 10 мг содержит: Активное вещество: амлодипин - 10 мг (в виде амлодипина безилата - 13,889 мг). Вспомогательные вещества: целлюлоза микрокристаллическая -248,111 мг, кальция гидрофосфат - 126 мг, карбоксиметилкрахмал натрия - 8 мг, магния стеарат - 4 мг. АТХ: Регистрация: Лекарственное средство П N015567/01 Фармгруппа: блокатор "медленных" кальциевых каналов. Дата регистрации: 13.05.2009. Окончание регстрации: . Описание:Таблетки 5 мг - белые или почти белые таблетки в форме изумруда (восьмигранник с неровными сторонами) с гравировкой Pfizer на одной стороне и AML-5 на другой. Таблетки 10 мг - белые или почти белые таблетки в форме изумруда (восьмигранник с неровными сторонами) с гравировкой Pfizer на одной стороне и AML-10 на другой. Упаковка:Таблетки, 5 и 10 мг. По 10 или 14 таблеток в блистере из ПВХ/алюминиевой фольги. 3, 4 или 9 блистеров по 10 таблеток, или 1 блистер по 14 таблеток с инструкцией по применению в картонной пачке, на лицевой стороне которой с целью контроля первого вскрытия наносится перфорированная строчка. Срок годности:4 года. Не применять по истечении срока годности. Владелец рег.удостоверения:Пфайзер ГмбХ Производитель:Р-Фарм Германия, ГмбХ. Представительство:Пфайзер ООО
Модель:
RUR 815
Показания Язвенная болезнь желудка в стадии обострения и язва анастомоза: Язвенная болезнь двенадцатиперстной кишки в стадии обострения: Эрозивная и язвенная гастроэзофагеальная рефлюксная болезнь или рефлюкс- эзофагит: Поддерживающая терапия гастроэзофагеальной рефлюксной болезни: Неэрозивная гастроэзофагеальная рефлюксная болезнь: Синдром Золлингера-Эллисона и другие состояния, характеризующиеся патологической гиперсекрецией: В комбинации с соответствующей антибактериальной терапией для Helicobacter pilory у пациентов с язвенной болезнью. Противопоказания Противопоказания Гиперчувствительность к рабепразолу, замещенным бензимидазолам или другим вспомогательным компонентам препарата: беременность: период лактации: детский возраст (до 12 лет). С осторожностью: Тяжелая печеночная недостаточность, тяжелая почечная недостаточность. Беременность Рабепразол не следует назначать беременным женщинам (данных по безопасности применения рабепразола во время беременности нет). На время лечения следует прекратить грудное вскармливание. Неизвестно, выделяется ли рабепразол с грудным молоком. Соответствующие исследования у кормящих женщин не проводились. Применение и дозы Таблетки препарата Хайрабезол нельзя разжевывать или измельчать. Таблетки следует глотать целиком. Установлено, что ни время суток, ни прием пищи не влияют на активность рабепразола. При язвенной болезни желудка в стадии обострения и язве анастомоза рекомендуется принимать внутрь по 10 мг или по 20 мг один раз в день. Обычно излечение наступает после 6 недель терапии, однако в некоторых случаях длительность лечения может быть увеличена еще на 6 недель. При язвенной болезни двенадцатиперстной кишки в стадии обострения рекомендуется принимать внутрь по 20 мг один раз в день. В некоторых случаях лечебный эффект наступает при приеме 10 мг один раз в день. Длительность лечения составляет от 2 до 4 недель. В случае необходимости длительность лечения может быть увеличена еще на 4 недели. При лечении эрозивной гастроэзофагеальной рефлюксной болезни (ГЭРБ) или рефлюкс эзофагите рекомендуется принимать внутрь по 10 мг или по 20 мг один раз в день. Длительность лечения составляет от 4 до 8 недель. В случае необходимости длительность лечения может быть увеличена еще на 8 недель. При поддерживающей терапии гастроэзофагеальной рефлюксной болезни (ГЭРБ) рекомендуется принимать внутрь по 10 мг или по 20 мг один раз в день. Длительность лечения зависит от состояния пациента. При неэрозивной гастроэзофагеальной рефлюксной болезни (НЭРБ) без эзофагита рекомендуется принимать внутрь по 10 мг или по 20 мг один раз в день. Если после четырех недель лечения симптомы не исчезают, следует провести дополнительное исследование пациента. После купирования симптомов для предупреждения их последующего возникновения следует принимать препарат внутрь в дозе 10 мг один раз в день по требованию. Для лечения синдрома Золлингеуа-Элисона и других состояний, характеризующихся патологической гиперсекрецией, дозу подбирают индивидуально. Начальная доза - 60 мг в день, затем дозу повышают и назначают препарат в дозе до 100 мг в день при однократном приеме или по 60 мг два раза в день. Для некоторых пациентов дробное дозирование препарата является предпочтительным. Лечение должно продолжаться по мере клинической необходимости. У некоторых больных с синдромом Золлингера-Элисона длительность лечения рабепразолом составляет до одного года. Для лечения язвенной болезни двенадиатиперстной кишки или хронического гастрита, связанного с инфицированием Н. pylori, рекомендуется курс лечения длительностью 7 дней одной из следующих комбинаций препаратов: Хайрабезол по 20 мг 2 раза в день + кларитромицин по 500 мг 2 раза в день и амоксициллин по 1г. 2 раза в день. Хайрабезол по 20 мг 2 раза в день + кларитромицин по 500 мг 2 раза в день и метронидазол по 400 мг 2 раза в день. Пациенты с почечной и печеночной недостаточностью Коррекции дозы пациентам с почечной недостаточностью не требуется. У пациентов с легкой и умеренной степенью печеночной недостаточности концентрация рабепразола в крови обычно выше, чем у здоровых пациентов. При назначении препарата Хайрабезол пациентам с тяжелой степенью печеночной недостаточности следует соблюдать осторожность. Пожилые пациенты Коррекции дозы не требуется. Дети. Безопасность и эффективность рабепразола 20 мг для краткосрочного (до 8 недель) лечения ГЭРБ у детей в возрасте 12 лет и более подтверждена экстраполяцией результатов адекватных и хорошо контролируемых исследований, подкрепляющих эффективность рабепразола для взрослых и исследованиями безопасности и фармакокинетики для пациентов детского возраста. Рекомендуемая доза для детей в возрасте 12 лет и более составляет 20 мг 1 раз в день продолжительностью до 8 недель. Безопасность и эффективность рабепразола для лечения ГЭРБ у детей в возрасте младше 12 лет не установлена. Безопасность и эффективность рабепразола для применения по другим показаниям не установлена для пациентов детского возраста. Побочные эффекты и передозировка Побочные эффекты: Исходя из опыта клинических испытаний, можно сделать вывод, что рабепразол обычно хорошо переносится пациентами. Побочные эффекты в целом слабо выраженные или умеренные и носят преходящий характер. При приеме рабепразола в ходе клинических исследований отмечались следующие побочные действия: головная боль, боль в животе, диарея, метеоризм, запор, сухость во рту, головокружение, сыпь, периферический отек. В ходе пострегистрационного применения рабепразола сообщалось о следующих побочных эффектах: повышение уровня печеночных ферментов, редко - гепатит и желтуха. У пациентов с циррозом печени редко сообщалось о развитии печеночной энцефалопатии. Также в редких случаях отмечались тромбоцитопения, нейтропения, лейкопения, буллезные высыпания, крапивница,острые системные аллергические реакции, миалгия, артралгия, гипомагниемия. Очень редко сообщалось о развитии интерстициального нефрита, гинекомастии, мультиформной эритемы, токсического эпидермального некролиза, синдрома Стивенса-Джонсона. Согласно данным постмаркетингового наблюдения при приеме ингибиторов протонной помпы возможно увеличение риска возникновения переломов (см. раздел "Особые указания") Передозировка: Симптомы: Данные о намеренной или случайной передозировке минимальны. Случаев сильной передозировки рабепразолом не было отмечено. Лечение: Специфический антидот для рабепразола неизвестен. Рабепразол хорошо связывается с белками плазмы, и поэтому слабо выводится при диализе. При передозировке необходимо проводить симптоматическое и поддерживающее лечение. Взаимодействие с другими ЛС: Рабепразол замедляет выведение некоторых лекарственных средств, метаболизирующихся в печени путем микросомального окисления (диазепам, фенитоин, непрямые антикоагулянты). Снижает концентрацию кетоконазола на 33%, дигоксина - на 22%. Не взаимодействует с жидкими антацидами. Совместим с препаратами, метаболизирующимися системой CYP450 (варфарин, фенитоин, теофиллин, диазепам). Фармакологическое действие и фармакокинетика Противоязвенное средство из группы ингибиторов протонного насоса (Н+/К-АТФ-азы), метаболизируется в париетальных клетках желудка до активных сульфонамидных производных, которые инактивируют сульфгидрильные группы Н+/К-АТФ-азы. Блокирует заключительную стадию секреции хлористоводородной кислоты, снижая содержание базальной и стимулированной секреции, независимо от природы раздражителя. Обладает высокой липофильностью, легко проникает в париетальные клетки желудка и концентрируется в них, оказывая цитопротекторное действие. Антисекреторный эффект после перорального приема 20 мг наступает в течение 1 ч и достигает максимума через 2-4 ч: угнетение базальной и стимулированной пищей секреции кислоты через 23 ч после приема первой дозы составляет 62% и 82%, соответственно: продолжительность действия - 48 ч. После окончания приема секреторная активность нормализуется в течение 2-3 дней. В первые 2-8 недель терапии концентрация гастрина в сыворотке крови увеличивается и возвращается к исходным уровням в течение 1-2 недель после отмены препарата. Не влияет на центральную нервную систему, сердечно-сосудистую и дыхательную системы. Фармакокинетика: Абсорбция происходит в тонком кишечнике (из-за наличия кислотоустойчивой кишечнорастворимой оболочки) высокая, время достижения максимальной концентрации - 3,5 ч. Значения максимальной концентрации (Сmах) и площади под кривой "концентрация действующего вещества - время" (AUC) носят линейный характер в диапазоне доз от 10 до 40 мг. Метаболизируется в печени с участием изоферментов цитохрома Р-450 CYP2C19 и CYP3A4. Биодоступность - 52%, не увеличивается при многократном приеме. Период полувыведения (T1/2) - 0,7-1,5 ч, клиренс - 283 ± 98 мл/мин. У пациентов с хронической печеночной недостаточностью слабой или средней степени после однократного приема AUC увеличивается в 2 раза, Т1/2 - в 2-3 раза. После приема 20 мг рабепразола в течение 7 дней AUC увеличивается в 1,5 раза, Т1/2 - в 1,2 раза. У пациентов со стабильной терминальной стадией почечной недостаточности, нуждающихся в гемодиализе (клиренс креатинина менее 5 мл/мин/1,73 м 2), распределение рабепразола натрия близко к таковому у здоровых лиц. У пожилых пациентов после приема рабепразола в течение 7 дней AUC в 2 раза больше, Сmах - на 60% больше, чем у молодых. Связь с белками плазмы - 97%. Выводится почками - 90% в виде двух метаболитов: конъюгата меркаптуровой кислоты (М5) и карбоновой кислоты (Мб): кишечником - 10%. У пациентов с замедленным метаболизмом CYP2C19 после 7 дней приема рабепразола в дозе 20 мг в сутки AUC увеличивается в 1,9 раза, а период полувыведения в 1,6 раза по сравнению с теми же параметрами у "быстрых метаболизаторов", в то время как Сmах увеличивается на 40 %. Особые указания Ответ пациента на терапию рабепразолом не исключает наличие злокачественных новообразований в желудке. Таблетки препарата Хайрабезол нельзя разжевывать или измельчать. Таблетки следует глотать целиком. Установлено, что ни время суток, ни прием пищи не влияют на активность рабепразола. В специальном исследовании у пациентов с легкими или умеренными нарушениями функции печени не было обнаружено значимого отличия частоты побочных эффектов рабепразола от таковой у подобранных по полу и возрасту здоровых лиц, но, несмотря на это, рекомендуется соблюдать осторожность при первом назначении пациентам с тяжелыми нарушениями функции печени. Пациентам с нарушениями функции почек или печени корректировка дозы препарата Хайрабезол не требуется. AUC рабепразола у пациентов с тяжелым нарушением функции печени примерно в два раза выше, чем у здоровых пациентов. Гипомагниемия. При лечении ингибиторами протонной помпы на протяжении, по крайней мере, 3 месяцев в редких случаях были отмечены случаи симптоматической или асимптоматической гипомагниемии. В большинстве случаев эти сообщения поступали через год после проведения терапии. Серьезными побочными явлениями были тетания, аритмия и судороги. Большинству пациентов требовалось лечение гипомагниемии, включающее замещение магния и отмену терапии ингибиторами протонной помпы. У пациентов, которые будут получать длительное лечение или которые принимают ингибиторы протонной помпы с препаратами, такими как дигоксин или препаратами, которые могут вызвать гипомагниемию (например, диуретики), медицинские работники должны контролировать уровень магния до начала лечения ингибиторами протонной помпы и в период лечения. Переломы. Согласно данным наблюдательных исследований можно предположить, что терапия ингибиторами протонной помпы может привести к возрастанию риска, связанного с остеопорозом переломов бедра, запястья, позвоночника. Риск переломов был увеличен у пациентов, принимавших высокие дозы ингибиторов протонной помпы в течение года и более. Влияние на способность управлять транспортными средствами: В случае появления в процессе лечения сонливости следует отказаться от управления автомобилем и других видов деятельности, требующих повышенной концентрации внимания и быстроты психомоторных реакций. Условия хранения и отпуска из аптек Условия хранения: В сухом, защищенном от света месте, при температуре от 8 °С до 25 °С. Хранить в недоступном для детей месте Отпуск из аптек: По рецепту Регистрационные данные Торговое название Хайрабезол® Международное непатентованное название:Рабепразол. Форма выпуска:таблетки покрытые кишечнорастворимой пленочной оболочкой. Состав:Дозировка 10 мг: Активный ингредиент: рабепразол натрия - 10 мг. Вспомогательные ингредиенты: магния оксид 50 мг, маннитол 17,5 мг, крахмал кукурузный 2,5 мг, повидон-КЗО 1,5 мг, гипролоза низкозамещенная 16 мг, натрия стеарилфумарат 2мг. Оболочка: целлацефат 11,25 мг, титана диоксид 1 мг, краситель железа оксид красный 0,1 мг. Дозировка 20 мг: Активный ингредиент: рабепразол натрия - 20 мг. Вспомогательные ингредиенты: магния оксид 69 мг, маннитол 40 мг, крахмал кукурузный 2,5 мг, повидон-КЗО 1,5 мг, гипролоза низкозамещенная 24 мг, натрия стеарилфумарат 2 мг. Оболочка: целлацефат 18 мг, титана диоксид 1,6 мг, краситель железа оксид желтый 0,16 мг АТХ: Регистрация: ЛП-001479 Фармгруппа: средство, понижающее секрецию желез желудка - протонного насоса ингибитор. Дата регистрации: 06.02.2012. Окончание регстрации: . Описание:Дозировка 10 мг: круглые двояковыпуклые таблетки, покрытые оболочкой от светло-розового до красновато-розового цвета. На поперечном разрезе ядро белого или белого с желтоватым оттенком цвета. Дозировка 20 мг:круглые двояковыпуклые таблетки, покрытые оболочкой от светло-желтого до желтого цвета. На поперечном разрезе ядро белого или белого с желтоватым оттенком цвета. Упаковка:таблетки покрытые кишечнорастворимой пленочной оболочкой 10мг и 20мг. Для аптек: 10, 14, 15 таблеток в Ал/Ал блистер или в Ал/Ал стрип. 1 или 10 стрипов/блистеров по 10 таблеток, 1 или 2 стрипа/блистера по 14 таблеток, 1, 2 или 10 стрипов/блистеров по 15 таблеток вместе с инструкцией по применению в пачку картонную. 1 стрип/блистер по 14 или 15 таблеток вместе с инструкцией по применению в пачку картонную с клапаном и перфорацией, защищенной пленкой ПВХ с внутренней стороны пачки (7 перфораций в виде круга). Для стационаров: 100, 500, 1000 таблеток в пакет из полиэтилена. пакет вместе с инструкцией по применению в банку из полиэтилена высокой плотности. На банку наклеивают этикетку. Срок годности:2 года. Не использовать по истечению срока годности указанного на упаковке. Владелец рег.удостоверения:Хайгланс Лабораториз Пвт. Лтд. Производитель:HIGLANCE LABORATORIES Pvt. Ltd. Представительство:ХАЙГЛАНС ЛАБОРАТОРИЗ

Модель:
RUR 1434
Показания Контрацепция. Противопоказания Противопоказания Препарат Ярина® противопоказан при наличии любого из состояний/заболеваний, перечисленных ниже. Если какие-либо из этих состояний/заболеваний развиваются впервые на фоне приема, препарат должен быть немедленно отменен- тромбозы (венозные и артериальные) и тромбоэмболии (в том числе тромбоз глубоких вен, тромбоэмболия легочной артерии, инфаркт миокарда, инсульт), цереброваскулярные нарушения - в настоящее время или в анамнезе- состояния, предшествующие тромбозу (в том числе транзиторные ишемические атаки, стенокардия) в настоящее время или в анамнезе- выявленная приобретенная или наследственная предрасположенность к венозному или артериальному тромбозу, включая резистентность к активированному протеину С, дефицит антитромбина III, дефицит протеина С, дефицит протеина S, гипергомоцистеинемия, антитела к фосфолипидам (антитела к кардиолипину, волчаночный антикоагулянт)- наличие высокого риска венозного или артериального тромбоза (смотри раздел "Особые указания")- мигрень с очаговыми неврологическими симптомами в настоящее время или в анамнезе- сахарный диабет с сосудистыми осложнениями- панкреатит с выраженной гипертриглицеридемией в настоящее время или в анамнезе- печеночная недостаточность и тяжелые заболевания печени (до нормализации печеночных проб)- опухоли печени (доброкачественные или злокачественные) в настоящее время или в анамнезе- тяжелая или острая почечная недостаточность: - выявленные гормонозависимые злокачественные заболевания (в том числе половых органов или молочных желез) или подозрение на них- кровотечение из влагалища неясного генеза- беременность или подозрение на нее- период грудного вскармливания- повышенная чувствительность к любому из компонентов препарата Ярина®: - непереносимость лактозы, дефицит лактазы, глюкозо-галактозная мальабсорбция (в состав препарата входит лактозы моногидрат). С осторожностью: Следует тщательно взвешивать потенциальный риск и ожидаемую пользу применения КОК в каждом индивидуальном случае при наличии следующих заболеваний/состояний и факторов риска- факторы риска развития тромбоза и тромбоэмболий: курение: ожирение: дислипопротеинемия, контролируемая артериальная гипертензия: мигрень без очаговой неврологической симптоматики: пороки клапанов сердца: наследственная предрасположенность к тромбозу (тромбозы, инфаркт миокарда или нарушение мозгового кровообращения в молодом возрасте у кого-либо из ближайших родственников)- другие заболевания, при которых могут отмечаться нарушения периферического кровообращения: сахарный диабет: системная красная волчанка: гемолитико-уремический синдром: болезнь Крона и язвенный колит: серповидно-клеточная анемия: флебит поверхностных вен- наследственный ангионевротический отек- гипертриглицеридемия- заболевания печени, не относящиеся к противопоказаниям (см. "Противопоказания")- заболевания, впервые возникшие или усугубившиеся во время беременности или на фоне предыдущего приема половых гормонов (например, желтуха и/или зуд, связанные с холестазом, холелитиаз, отосклероз с ухудшением слуха, порфирия, герпес во время беременности, хорея Сиденгама): - послеродовый период. Беременность Препарат Ярина® противопоказан во время беременности и в период грудного вскармливания. Если беременность выявляется во время приема препарата Ярина®, препарат следует сразу же отменить. Обширные эпидемиологические исследования не выявили повышенного риска дефектов развития у детей, рожденных женщинами, получавшими половые гормоны до беременности или тератогенного действия в случаях приема половых гормонов по неосторожности в ранние сроки беременности. В то же время имеющиеся данные о применении препарата Ярина® во время беременности ограничены, что не позволяет сделать какие-либо выводы о негативном влиянии препарата на беременность, здоровье плода и новорожденного ребенка. В настоящее время какие-либо значимые эпидемиологические данные отсутствуют. Прием препарата может уменьшать количество грудного молока и изменять его состав, поэтому применение препарата противопоказано до прекращения грудного вскармливания. Небольшое количество половых гормонов и/или их метаболитов может проникать в грудное молоко и оказывать влияние на здоровье ребенка. Применение и дозы Как и когда принимать таблетки Календарная упаковка препарата Ярина® содержит 21 таблетку. Каждая таблетка в упаковке маркируется днем недели, в который она должна быть принята. Таблетки следует принимать внутрь каждый день в течение 21 дня по порядку, указанному на упаковке, примерно в одно и то же время, запивая небольшим количеством воды. Прием таблеток из следующей упаковки начинается после 7-дневного перерыва, во время которого обычно развивается менструальноподобное кровотечение (кровотечение "отмены"). Как правило, оно начинается на 2-3 день после приема последней таблетки и может не закончиться до начала приема таблеток из новой упаковки. После 7-дневного перерыва начать прием таблеток из новой упаковки необходимо даже в случае, если менструальноподобное кровотечение еще не прекратилось. Это означает, что начинать прием таблеток из новой упаковки необходимо в один и тот же день недели, и что каждый месяц кровотечение "отмены" будет наступать примерно в один и тот же день недели. Прием таблеток из первой упаковки препарата Ярина® - Когда никакое гормональное противозачаточное средство не применялось в предыдущем месяце Прием препарата Ярина® следует начать в первый день менструального цикла (т.е. в первый день менструального кровотечения). Необходимо принять таблетку, которая промаркирована соответствующим днем недели. Затем следует принимать таблетки по порядку. Допускается начать прием препарата на 2-5 день менструального цикла, но в этом случае в течение первых 7 дней приема таблеток из первой упаковки рекомендуется дополнительно использовать барьерный метод контрацепции. - При переходе с других комбинированных контрацептивных препаратов (КОК, вагинального кольца или трансдермального пластыря) Предпочтительно начать прием препарата Ярина® на следующий день после приема последней активной таблетки из предыдущей упаковки, но ни в коем случае не позднее следующего дня после обычного 7-дневного перерыва (для препаратов, содержащих 21 таблетку) или после приема последней неактивной таблетки (для препаратов, содержащих 28 таблеток в упаковке). Прием препарата Ярина® следует начинать в день удаления вагинального кольца или пластыря, но не позднее дня, когда должно быть введено новое кольцо или наклеен новый пластырь. - При переходе с контрацептивов, содержащих только гестагены ("мини-пили", инъекционные формы, имплантат) или с внутриматочной терапевтической системы с высвобождением гестагена Перейти с "мини-пили" на препарат Ярина® можно в любой день (без перерыва), с имплантата или внутри маточного контрацептива с гестагеном - в день их удаления, с инъекционной формы - в день, когда должна быть сделана следующая инъекция. Во всех этих случаях в течение первых 7 дней приема таблеток препарата Ярина® необходимо дополнительно использовать барьерный метод контрацепции (например, презерватив). - После аборта (в том числе самопроизвольного) в первом триместре беременности Начать прием препарата можно немедленно. При соблюдении этого условия дополнительных мер контрацепции не требуется- После родов (при отсутствии грудного вскармливания) или аборта (в том числе самопроизвольного) во втором триместре беременности. Начать прием препарата рекомендуется на 21-28 день после родов (при отсутствии грудного вскармливания) или аборта во втором триместре беременности. Если прием препарата начат позднее, необходимо использовать дополнительно барьерный метод контрацепции в течение первых 7 дней приема таблеток. Если половой контакт имел место до начала приема препарата Ярина®, необходимо исключить беременность. Прием пропущенных таблеток. Если опоздание в приеме препарата составило менее 12 часов, контрацептивная защита не снижается. Нужно принять пропущенную таблетку как можно скорее, следующая таблетка принимается в обычное время. Если опоздание в приеме таблеток составило более 12 часов, контрацептивная защита снижается. Чем больше таблеток пропущено, и чем ближе пропуск к 7-дневному перерыву в приеме таблеток, тем выше вероятность наступления беременности. При этом необходимо помнить- Прием препарата никогда не должен быть прерван более чем на 7 дней- 7 дней непрерывного приема таблеток требуется для достижения адекватного подавления гипоталамо-гипофизарно-яичниковой системы. Соответственно, если опоздание в приеме таблеток превышает 12 часов (интервал с момента приема последней таблетки - более 36 часов), в зависимости от недели, когда пропущена таблетка, необходимо: Первая неделя приема препарата. Необходимо принять последнюю пропущенную таблетку как можно скорее, как только женщина вспомнит об этом (даже если для этого нужно принять две таблетки одновременно). Следующую таблетку необходимо принять в обычное время. В течение последующих 7 дней дополнительно должен быть использован барьерный метод контрацепции (например, презерватив). Если половой контакт имел место в течение 7 дней перед пропуском таблетки, необходимо учесть возможность наступления беременности. Вторая неделя приема препарата. Необходимо принять последнюю пропущенную таблетку как можно скорее, как только женщина вспомнит об этом (даже если для этого нужно принять две таблетки одновременно). Следующую таблетку необходимо принять в обычное время. При условии, если женщина принимала таблетки правильно в течение предшествующих 7 дней, нет необходимости в использовании дополнительных контрацептивных мер. В противном случае, а также при пропуске двух и более таблеток, необходимо дополнительно использовать барьерные методы контрацепции (например, презерватив) в течение последующих 7 дней. Третья неделя приема препарата. Риск снижения контрацептивной надежности неизбежен из-за предстоящего перерыва в приеме таблеток. В этом случае необходимо придерживаться следующих алгоритмов- если в течение 7 дней, предшествующих первой пропущенной таблетке, все таблетки принимались правильно, нет необходимости использовать дополнительные методы контрацепции. При приеме пропущенных таблеток руководствуйтесь пунктами 1 или 2- если в течение 7 дней, предшествующих первой пропущенной таблетке, таблетки принимались неправильно, то в течение последующих 7 дней необходимо дополнительно использовать барьерный метод контрацепции (например, презерватив) и в этом случае следует руководствоваться пунктом 1 для приема пропущенных таблеток.1. Необходимо принять пропущенную таблетку как можно скорее, как только женщина вспомнит об этом (даже если это означает прием двух таблеток одновременно). Следующие таблетки принимают в обычное время, пока не закончатся таблетки из текущей упаковки. Прием таблеток из следующей упаковки следует начать сразу же без обычного 7-дневного перерыва. Кровотечение "отмены" маловероятно, пока не закончатся таблетки из второй упаковки, но могут отмечаться "мажущие" выделения и/или "прорывные" кровотечения в дни приема препарата.2. Можно также прервать прием таблеток из текущей упаковки, сделать перерыв на 7 или менее дней (включай дни пропуска таблеток), после чего начать прием таблеток из новой упаковки. Если женщина пропустила прием таблеток, а во время перерыва в приеме у нее нет кровотечения "отмены", необходимо исключить беременность (см. рис.). Допускается принимать не более двух таблеток в один день. Рекомендации при желудочно-кишечных расстройствах. При тяжелых желудочно-кишечных расстройствах всасывание препарата может быть неполным, поэтому следует использовать дополнительные методы контрацепции. Если в течение 3-4 часов после приема таблеток отмечается рвота или диарея, в зависимости от недели приема препарата следует ориентироваться на рекомендации при пропуске таблеток, указанные выше. Если женщина не хочет менять свою обычную схему приема и переносить начало менструации на другой день недели, дополнительную таблетку следует принять из другой упаковки. Прекращение приема препарата Ярина®Прием препарата Ярина® можно прекратить в любое время. Если женщина не планирует беременность, следует позаботиться о других методах контрацепции. Если планируется беременность, следует просто прекратить прием препарата Ярина® и подождать естественного менструального кровотечения. Отсрочка начала менструальноподобного кровотечения. Для того, чтобы отсрочить начало менструальноподобного кровотечения, необходимо продолжить дальнейший прием таблеток из новой упаковки препарата Ярина® без 7-дневного перерыва. Таблетки из новой упаковки могут приниматься так долго, как это необходимо, в том числе до тех пор, пока таблетки в упаковке не закончатся. На фоне приема препарата из второй упаковки могут отмечаться "мажущие" кровянистые выделения из влагалища и/или "прорывные" маточные кровотечения. Возобновить прием препарата Ярина® из очередной упаковки следует после обычного 7-дневного перерыва. Изменение дня начала менструальноподобного кровотечения. Для того чтобы перенести день начала менструальноподобного кровотечения на другой день недели, женщине следует сократить (но не удлинять) ближайший 7-дневный перерыв в приеме таблеток на столько дней, на сколько женщина хочет. Например, если цикл обычно начинается в пятницу, а в будущем женщина хочет, чтобы он начинался во вторник (3 днями ранее), прием таблеток из следующей упаковки необходимо начать на 3 дня раньше, чем обычно. Чем короче перерыв в приеме таблеток, тем выше вероятность, что менструальноподобное кровотечение не наступит, и во время приема таблеток из второй упаковки будут наблюдаться "мажущие" выделения и/или "прорывные" кровотечения. Применение у отдельных групп пациентокУ детей и подростков. Препарат Ярина® показан только после наступления менархе. Имеющиеся данные не предполагают коррекции дозы у данной группы пациенток.У пожилых. Не применимо. Препарат Ярина® не показан после наступления менопаузы. При нарушениях функции печени. Препарат Ярина® противопоказан к применению у женщин с тяжелыми заболеваниями печени до тех пор, пока показатели функции печени не придут в норму. См. также раздел "Противопоказания" и "Фармакологические свойства". При нарушениях функции почек Препарат Ярина® противопоказан женщинам с тяжелой почечной недостаточностью или с острой почечной недостаточностью. См. также разделы "Противопоказания" и "Фармакологические свойства". Побочные эффекты и передозировка Побочные эффекты: Данные о частоте возникновения побочных реакций, о которых сообщалось в ходе клинических исследований препарата Ярина® (N=4897), приведены в таблице ниже. В пределах каждой группы, выделенной в зависимости от частоты возникновения, побочные реакции представлены в порядке уменьшения их тяжести. По частоте они разделяются на частые (>:1/100 и <:1/10), нечастые (>:1/1000 и <:1/100) и редкие (>:1/10000 и <:1/1000). Для дополнительных побочных реакций, выявленных только в процессе постмаркетинговых исследований, и для которых оценку частоты возникновения провести не представлялось возможным, указано "частота неизвестна". ТАБЛИЦЪ Нежелательные явления в ходе клинических исследований были кодифицированы с использованием словаря MedDRA (Медицинский Словарь Регуляторной Деятельности, версия 12.1). Различные термины MedDRA, отражающие один и тот же симптом, были сгруппированы вместе и представлены в качестве единственной побочной реакции, во избежание ослабления или размытия истинного эффекта. * Расчетная частота по данным эпидемиологических исследований, охватывавших группу КОК. Венозные и артериальные тромбоэмболические осложнения объединяют следующие нозологические формы: окклюзия периферических глубоких вен, тромбоз и тромбоэмболия /окклюзия легочных сосудов, тромбоз, эмболия и инфаркт /инфаркт миокарда/церебральный инфаркт и инсульт не классифицированный как геморрагический. Для венозной и артериальном тромбоэмболии, мигрени см. также "Противопоказания" и "Особые указания". Ниже перечислены побочные реакции с очень низкой частотой возникновения или с отсроченным развитием симптомов, которые считаются связанными с группой КОК (см. также разделы "Противопоказания”, “Особые указания"): Опухоли - У женщин, применяющих КОК, очень незначительно повышена частота выявления рака молочной железы. Поскольку рак молочной железы редко встречается у женщин моложе 40 лет, повышение частоты рака у женщин, применяющих КОК, незначительно по отношению к общему риску возникновения рака молочной железы. Причинно-следственная связь с применением КОК неизвестна. - Опухоли печени (доброкачественные и злокачественные). Прочие состояния - Узловатая эритема. - Женщины с гипертриглицеридемией (повышенный риск панкреатита при применении КОК). - Повышение артериального давления. - Наступление или ухудшение состояний, при которых связь с применением КОК не является неоспоримой: желтуха и/или зуд, связанные с холестазом: образование камней желчного пузыря: порфирия: системная красная волчанка: гемолитико-уремический синдром: хорея Сиденгама: герпес во время беременности: потеря слуха, связанная с отосклерозом. - У женщин с наследственным ангионевротическим отеком экзогенные эстрогены могут вызвать или усилить симптомы ангионевротического отека. - Нарушения функции печени. - Нарушения толерантности к глюкозе или влияние на периферическую инсулинорезистентность. - Болезнь Крона, язвенный колит- Хлоазма- Гиперчувствительность (включая такие симптомы как сыпь, крапивница). Взаимодействие Вследствие взаимодействия других препаратов (индукторов ферментов) с пероральными контрацептивами могут возникать "прорывные" кровотечения и/или снижение контрацептивного эффекта (см. раздел "Взаимодействие с другими лекарственными препаратами"). Передозировка: О серьезных нарушениях при передозировке не сообщалось. На основании суммарного опыта применения КОК симптомы, которые могут отмечаться при передозировке: тошнота, рвота, мажущие кровянистые выделения из влагалища, метроррагия. Специфического антидота нет, следует проводить симптоматическое лечение. Взаимодействие с другими ЛС: Влияние других лекарственных средств на препарат Ярина®Возможно взаимодействие с лекарственными средствами, индуцирующими микросомальные ферменты печени, в результате чего может увеличиваться клиренс половых гормонов, что, в свою очередь, может приводить к "прорывным" маточным кровотечениям и/или снижению контрацептивного эффекта. Женщинам, которые получают лечение такими препаратами в дополнение к препарату Ярина®, рекомендуется использовать барьерный метод контрацепции или выбрать иной негормональный метод контрацепции. Барьерный метод контрацепции следует использовать в течение всего периода приема сопутствующих препаратов, а также в течение 28 дней после их отмены. Если период применения барьерного метода контрацепции заканчивается позже, чем таблетки в упаковке препарата Ярина®, следует начать прием таблеток препарата Ярина® из новой упаковки без перерыва в приеме таблеток- Вещества, увеличивающие клиренс препарата Ярина® (ослабляющие эффективность путем индукции ферментов): фенитоин, барбитураты, примидон, карбамазепин, рифампицин и, возможно, также окскарбазепин, топирамат, фелбамат, гризеофульвин, а также препараты, содержащие зверобой продырявленный- Вещества с различным влиянием на клиренс препарата Ярина®При совместном применении с препаратом Ярина® многие ингибиторы протеаз ВИЧ или вируса гепатита С и ненуклеозидные ингибиторы обратной транскриптазы могут как увеличивать, так и уменьшать концентрацию эстрогенов или прогестинов в плазме крови. В некоторых случаях такое влияние может быть клинически значимо- Вещества, снижающие клиренс КОК (ингибиторы ферментов)Сильные и умеренные ингибиторы CYP3A4, такие как азольные антимикотики (например, итраконазол, вориконазол, флюконазол), верапамил, макролиды (например, кларитромицин, эритромицин), дилтиазем и грейпфрутовый сок могут повышать плазменные концентрации эстрогена или прогестина, или их обоих. Было показано, что эторикоксиб в дозах 60 и 120 мг/сутки при совместном приеме с КОК, содержащими 0,035 мг этинилэстрадиола, повышает концентрацию этинилэстрадиола в плазме крови в 1,4 и 1,6 раза соответственно. Влияние препарата Ярина® на другие лекарственные препаратыКОК могут влиять на метаболизм других препаратов, что приводит к повышению (например, циклоспорин) или снижению (например, ламотриджин) их концентрации в плазме крови и тканях. In vitro дроспиренон способен слабо или умеренно ингибировать ферменты цитохрома Р450 CYP1A1, CYP2C9, CYP2C19 и CYP3A4. На основании исследований взаимодействия in vivo у женщин-добровольцев, принимавших омепразол, симвастатин или мидазолам в качестве маркерных субстратов, можно заключить, что клинически значимое влияние 3 мг дроспиренона на метаболизм лекарственных препаратов, опосредованный ферментами цитохрома Р450, маловероятно. In vitro этинилэстрадиол является обратимым ингибитором CYP2C19, CYP1A1 и CYP1A2, а также необратимым ингибитором CYP3A4/5, CYP2C8 и CYP2J2. В клинических исследованиях назначение гормонального контрацептива, содержащего этинилэстрадиол, не приводило к какому-либо повышению или приводило лишь к слабому повышению концентраций субстратов CYP3A4 в плазме крови (например, мидазолама), в то время как плазменные концентрации субстратов CYP1A2 могут возрастать слабо (например, теофиллин) или умеренно (например, мелатонин и тизанидин). Другие формы взаимодействия У пациенток с ненарушенной функцией почек сочетанное применение дроспиренона и ингибиторов ангиотензинпревращающего фермента или нестероидных противовоспалительных препаратов не оказывает значимого эффекта на концентрацию калия в плазме крови. Тем не менее сочетанное применение препарата Ярина® с антагонистами альдостерона или калийсберегающими диуретиками не изучено. При совместном приеме с данными препаратами концентрацию калия в плазме крови необходимо контролировать в течение первого цикла приема (см. раздел "Особые указания"). Фармакологическое действие и фармакокинетика Препарат Ярина® - низкодозированный монофазный пероральный комбинированный эстроген-гестагенный контрацептивный препарат. Контрацептивный эффект препарата Ярина® осуществляется в основном посредством взаимодополняющих механизмов, к наиболее важным из которых относятся подавление овуляции и повышение вязкости секрета шейки матки, в результате чего она становится непроницаемой для сперматозоидов. При правильном применении препарата Ярина® индекс Перля (показатель, отражающий число беременностей у 100 женщин, применяющих контрацептив в течение года) составляет менее 1. При пропуске таблеток или неправильном применении индекс Перля может возрастать. Повышенный риск венозной тромбоэмболии (ВТЭ), связываемый с применением комбинированных пероральных контрацептивов (КОК), относится, прежде всего, к эстрогенному компоненту. В настоящее время продолжаются научные споры относительно модулирующего эффекта прогестина, входящего в состав КОК, в отношении риска ВТЭ. Сравнительные эпидемиологические исследования риска ВТЭ при применении КОК, содержащих этинилэстрадиол/дроспиренон, и риска при применении левоноргестрел-содержащих КОК показали различные результаты - от отсутствия отличий по степени риска, до трехкратного возрастания риска. В большинстве исследований изучался препарат Ярина®. Для оценки риска ВТЭ при применении препарата Ярина® (этинилэстрадиол/дроспиренон в дозах 0,03 мг/3 мг) были проведены два пострегистрационных исследования. Первое проспективное наблюдательное исследование показало, что частота возникновения ВТЭ у женщин, применяющих препарат Ярина®, при наличии или в отсутствии других факторов риска ВТЭ была в том же диапазоне, что и для женщин, применяющих левоноргестрел-содержащие и другие КОК. Второе проспективное контролируемое исследование баз данных, в ходе которого проводилась сравнительная оценка женщин, применяющих препарат Ярина®, с женщинами, применяющими другие КОК, также подтвердило сходную частоту ВТЭ среди всех когорт женщин.У женщин, принимающих КОК, цикл становится более регулярным, реже наблюдаются болезненные менструальноподобные кровотечения, уменьшается интенсивность и продолжительность кровотечения, в результате чего снижается риск железодефицитной анемии. Также имеются данные о снижении риска рака эндометрия и яичников при приеме КОК. Дроспиренон, входящий в состав препарата Ярина®, обладает атиминералокортикоидной активностью и способен предупреждать увеличение массы тела и появление других симптомов (например, отеков), связанных с эстрогензависимой задержкой жидкости. Дроспиренон также обладает антиандрогенной активностью и способствует уменьшению угрей (акне), жирности кожи и волос (себореи). Эти особенности дроспиренона следует учитывать при выборе контрацептива женщинам с гормонозависимой задержкой жидкости, а также женщинам с акне и себореей. По своим характеристикам дроспиренон схож с естественным прогестероном, вырабатываемым женским организмом. Фармакокинетика: Дроспиренон Абсорбция При приеме внутрь дроспиренон быстро и почти полностью абсорбируется. После однократного приема максимальная концентрация (Сmax) дроспиренона в плазме крови, равная 38 нг/мл, достигается через 1-2 часа. Прием пищи не влияет на биодоступность, которая колеблется в диапазоне от 76 до 85%. Распределение Дроспиренон связывается с альбумином плазмы крови и не связывается с глобулином, связывающим половые гормоны (ГСПГ), или кортикостероид-связывающим глобулином (КСГ). Лишь 3-5% от общей концентрации вещества в плазме крови присутствует в виде свободного гормона, 95-97% вещества неспецифически связываются с альбумином. Индуцированное этинилэстрадиолом повышение ГСПГ не влияет на связывание дроспиренона белками плазмы крови. Средний кажущийся объем распределения составляет 3,7±1,2 л/кг. Метаболизм После перорального приема дроспиренон полностью метаболизируется. Большинство метаболитов в плазме крови представлены кислотными формами дроспиренона. Дроспиренон также является субстратом для окислительного метаболизма, катализируемого изоферментом СYР 3А4. Скорость метаболического клиренса дроспиренона из плазмы крови составляет 1,5±0,2 мл/мин/кг. Выведение Концентрация дроспиренона в плазме крови снижается двухфазно. Вторая, окончательная фаза имеет период полувыведения (T1/2) около 31 часа. В неизмененной форме дроспиренон экскретируется в следовых количествах. Его метаболиты выводятся через желудочно-кишечный тракт и почками в соотношении примерно 1,2:1.4. Период полувыведения метаболитов дроспиренона составляет примерно 40 часов. Равновесная концентрация Концентрация ГСПГ не оказывает влияния на показатели фармакокинетики дроспиренона. При ежедневном применении препарата внутрь концентрация дроспиренона в плазме крови повышается в 2-3 раза, равновесная концентрация достигается через 8 дней приема препарата. При нарушении функции почек Исследования показали, что концентрация дроспиренона в плазме крови женщин с легким нарушением функции почек (клиренс креатинина (КК) - 50-80 мл/мин) при достижении равновесного состояния и у женщин с сохранной функцией почек (КК - более 80 мл/мин) сопоставимы. Тем не менее у женщин с умеренным нарушением функции почек (КК - 30-50 мл/мин) средняя концентрация дроспиренона в плазме крови была на 37% выше, чем у пациенток с сохранной функцией почек. Не отмечено изменения концентрации калия в плазме крови при применении дроспиренона. При нарушении функции печени У женщин с умеренным нарушением функции печени (класс В по шкале Чайлд-Пью) площадь под кривой "концентрация-время" (AUC) сопоставима с соответствующим показателем у здоровых женщин с близкими значениями Сmax в фазе абсорбции и распределения. Т1/2 дроспиренона у больных с умеренным нарушением функции печени оказался в 1,8 раз выше, чем у здоровых добровольцев. У больных с умеренным нарушением функции печени отмечено снижение клиренса дроспиренона приблизительно на 50% по сравнению со здоровыми женщинами, при этом не отмечено различий в концентрации калия в плазме крови в изучаемых группах. При выявлении сахарного диабета и сопутствующем применении спиронолактона (оба состояния расцениваются как факторы, предрасполагающие к развитию гиперкалиемии) повышения концентрации калия в плазме крови не установлено. Таким образом, можно заключить, что переносимость дроспиренона у женщин с легким и умеренным нарушением функции печени хорошая (класс В по шкале Чайлд-Пью). Этническая принадлежность Не установлено влияния этнической принадлежности (исследование проведено на когортах женщин европеоидной расы и японок) на параметры фармакокинетики дроспиренона и этинилэстрадиола. Этинилэстрадиол Абсорбция После приема внутрь этинилэстрадиол быстро и полностью абсорбируется. Сmax - 100 нг/мл достигается в течение 1-2 часов. Во время всасывания и "первого прохождения" через печень этинилэстрадиол метаболизируется, в результате чего его биодоступность при приеме внутрь составляет в среднем около 45% при высокой межиндивидуальной вариабельности - от 20 до 65%. Одновременный прием пищи в отдельных случаях сопровождается снижением биодоступности этинилэстрадиола на 25%. Распределение Этинилэстрадиол неспецифически, но прочно связывается с альбумином плазмы крови (около 98%) и индуцирует повышение концентрации в плазме крови ГСПГ. Предполагаемый объем распределения составляет 5 л/кг. Метаболизм Этинилэстрадиол подвергается значительному первичному метаболизму в кишечнике и печени. Этинилэстрадиол и его окислительные метаболиты первично конъюгированы с глюкуронидами или сульфатом. Скорость метаболического клиренса этинилэстрадиола составляет около 5 мл/мин/кг. Выведение Снижение концентрации этинилэстрадиола в плазме крови носит двухфазный характер: первая фаза характеризуется периодом полувыведения около 1 часа, вторая - 20 часов. Этинилэстрадиол практически не выводится в неизмененном виде. Метаболиты этинилэстрадиола выводятся почками и через кишечник в соотношении 4:6. Период полувыведения метаболитов составляет примерно 24 ч. Равновесная концентрация Равновесное состояние достигается во второй половине цикла приема препарата, когда концентрация этинилэстрадиола в плазме крови повышается на 40-110% по сравнению с применением разовой дозы. Особые указания Если какие-либо из состояний, заболеваний и факторов риска, указанных ниже, имеются в настоящее время, то следует тщательно взвешивать потенциальный риск и ожидаемую пользу применения препарата Ярина® в каждом индивидуальном случае и обсудить его с женщиной до того, как она решит начать прием препарата. В случае утяжеления, усиления или первого проявления любого из этих состояний, заболеваний или факторов риска, женщина должна проконсультироваться со своим врачом, который может принять решение о необходимости отмены препарата. Заболевания сердечно-сосудистой системы. Результаты эпидемиологических исследований указывают на наличие взаимосвязи между применением КОК и повышением частоты развития венозных и артериальных тромбозов и тромбоэмболий (таких как тромбоз глубоких вен, тромбоэмболия легочной артерии, инфаркт миокарда, цереброваскулярные нарушения) при приеме КОК. Данные заболевания отмечаются редко. Риск развития ВТЭ максимален в первый год приема КОК. Повышенный риск присутствует после первоначального применения КОК или возобновления применения одного и того же или другого КОК (после перерыва между приемами препарата в 4 недели и более). Данные крупномасштабного проспективного исследования с участием 3 групп пациенток показывают, что этот повышенный риск присутствует преимущественно в течение первых 3 месяцев. Общий риск ВТЭ у женщин, принимающих низкодозированные КОК (<: 0,05 мг этинилэстрадиола) в два-три раза выше, чем у небеременных пациенток, которые не принимают КОК, тем не менее этот риск остается более низким по сравнению с риском ВТЭ во время беременности и родов.ВТЭ может оказаться жизнеугрожающей или привести к летальному исходу (в 1-2% случаев).ВТЭ, проявляющаяся в виде тромбоза глубоких вен или эмболии легочной артерии, может произойти при применении любых КОК. Крайне редко при применении КОК возникает тромбоз других кровеносных сосудов, например, печеночных, брыжеечных, почечных, мозговых вен и артерий или сосудов сетчатки. Симптомы тромбоза глубоких вен: односторонний отек нижней конечности или отек вдоль вены на нижней конечности, боль или дискомфорт в нижней конечности только в вертикальном положении или при ходьбе, локальное повышение температуры в пораженной нижней конечности, покраснение или изменение окраски кожных покровов на нижней конечности. Симптомы тромбоэмболии легочной артерии: затрудненное или учащенное дыхание: внезапный кашель, в том числе с кровохарканием: острая боль в грудной клетке, которая может усиливаться при глубоком вдохе: чувство тревоги: сильное головокружение: учащенное или нерегулярное сердцебиение. Некоторые из этих симптомов (например, одышка, кашель) являются неспецифическими и могут быть истолкованы неверно как признаки других более или менее тяжелых состояний/заболеваний (например, инфекции дыхательных путей). Артериальная тромбоэмболия может привести к инсульту, окклюзии сосудов или инфаркту миокарда. Симптомы инсульта: внезапная слабость или потеря чувствительности лица, конечностей, особенно с одной стороны тела, внезапная спутанность сознания, проблемы с речью и пониманием: внезапная одно- или двухсторонняя потеря зрения: внезапное нарушение походки, головокружение, потеря равновесия или координации движений: внезапная, тяжелая или продолжительная головная боль без видимой причины: потеря сознания или обморок с эпилептическим припадком или без него. Другие признаки окклюзии сосудов: внезапная боль, отечность и слабое посинение конечностей, "острый" живот. Симптомы инфаркта миокарда: боль, дискомфорт, давление, тяжесть, чувство сжатия или распирания в груди или за грудиной, с иррадиацией в спину, челюсть, левую верхнюю конечность, область эпигастрия: холодный пот, тошнота, рвота или головокружение, сильная слабость, тревога или одышка: учащенное или нерегулярное сердцебиение. Артериальная тромбоэмболия может оказаться жизнеугрожающей или привести к летальному исходу.У женщин с сочетанием нескольких факторов риска или высокой выраженностью одного из них следует рассматривать возможность их взаимоусиления. В подобных случаях суммарное значение имеющихся факторов риска повышается. В этом случае прием препарата Ярина® противопоказан (см. раздел "Противопоказания"). Риск развития тромбоза (венозного и/или артериального) и тромбоэмболии или цереброваскулярных нарушений повышается- с возрастом- у курящих (с увеличением количества выкуриваемых сигарет или повышением возраста риск нарастает, особенно у женщин старше 35 лет):при наличии- ожирения (индекс массы тела более чем 30 кг/м 2)- семейного анамнеза (например, венозной или артериальной тромбоэмболии когда-либо у близких родственников или родителей в относительно молодом возрасте). В случае наследственной или приобретенной предрасположенности женщина должна быть осмотрена соответствующим специалистом для решения вопроса о возможности приема препарата Ярина®- длительной иммобилизации, обширного хирургического вмешательства, любой операции на нижних конечностях или обширной травмы. В этих случаях прием препарата Ярина® необходимо прекратить (в случае планируемой операции по крайней мере за четыре недели до нее) и не возобновлять прием в течение двух недель после окончания иммобилизации. Временная иммобилизация (например, авиаперелет длительностью более 4 часов) может также являться фактором риска развития венозной тромбоэмболии, особенно при наличии других факторов риска- дислипопротеинемии- артериальной гипертензии- мигрени- заболеваний клапанов сердца- фибрилляции предсердий. Вопрос о возможной роли варикозного расширения вен и поверхностного тромбофлебита в развитии ВТЭ остается спорным. Следует учитывать повышенный риск развития тромбоэмболий в послеродовом периоде. Нарушения периферического кровообращения также могут отмечаться при сахарном диабете, системной красной волчанке, гемолитико-уремическом синдроме, хронических воспалительных заболеваниях кишечника (болезнь Крона или язвенный колит) и серповидно-клеточной анемии. Увеличение частоты и тяжести мигрени во время применения КОК (что может предшествовать цереброваскулярным нарушениям) является основанием для немедленной отмены приема этих препаратов.К биохимическим показателям, указывающим на наследственную или приобретенную предрасположенность к венозному или артериальному тромбозу относится следующее: резистентность к активированному протеину С, гипергомоцистеинемия, дефицит антитромбина III, дефицит протеина С, дефицит протеина S, антифосфолипидные антитела (антитела к кардиолипину, волчаночный антикоагулянт). При оценке соотношения риска и пользы следует учитывать, что адекватное лечение соответствующего состояния может уменьшить связанный с ним риск тромбоза. Также следует учитывать, что риск тромбозов и тромбоэмболий при беременности выше, чем при приеме низкодозированных пероральных контрацептивов (<: 0,05 мг этинилэстрадиола). Опухоли. Наиболее существенным фактором риска развития рака шейки матки является персистирующая папилломавирусная инфекция. Имеются сообщения о некотором повышении риска развития рака шейки матки при длительном применении КОК. Однако связь с приемом КОК не доказана. Обсуждается возможность взаимосвязи этих данных со скринингом заболеваний шейки матки или с особенностями полового поведения (более редкое применение барьерных методов контрацепции). Мета-анализ 54 эпидемиологических исследований показал, что имеется несколько повышенный относительный риск развития рака молочной железы, диагностированного у женщин, принимающих КОК в настоящее время (относительный риск 1,24). Повышенный риск постепенно исчезает в течение 10 лет после прекращения приема этих препаратов. В связи с тем, что рак молочной железы отмечается редко у женщин до 40 лет, увеличение числа диагнозов рака молочной железы у женщин, принимающих КОК в настоящее время или принимавших недавно, является незначительным но отношению к общему риску этого заболевания. Его связь с приемом КОК не доказана. Наблюдаемое повышение риска может быть также следствием тщательного наблюдения и более ранней диагностики рака молочной железы у женщин, применяющих КОК. У женщин, когда-либо использовавших КОК, выявляются более ранние стадии рака молочной железы, чем у женщин, никогда их не применявших.В редких случаях на фоне применения КОК наблюдалось развитие доброкачественных, а в крайне редких - злокачественных опухолей печени, которые в отдельных случаях приводили к угрожающему жизни внутрибрюшному кровотечению. В случае появления сильных болей в области живота, увеличения печени или признаков внутрибрюшного кровотечения это следует учитывать при проведении дифференциального диагноза. Злокачественные опухоли могут оказаться жизнеугрожающими или привести к летальному исходу. Другие состояния. Прогестиновый компонент в препарате Ярина® является антагонистом альдостерона, обладающим калийсберегающими свойствами. В большинстве случаев не должно наблюдаться повышения концентрации калия в плазме крови. В клинических исследованиях у некоторых пациенток с легкой или умеренной почечной недостаточностью и сопутствующем приеме калийсберегающих препаратов концентрация калия в плазме крови незначительно повышалась во время приема дроспиренона. Поэтому концентрацию калия в плазме крови необходимо контролировать в течение первого цикла приема препарата у пациенток с почечной недостаточностью и при изначальной концентрации калия на верхней границе нормы, особенно при сопутствующем приеме калийсберегающих препаратов (см. раздел "Взаимодействие с другими лекарственными препаратами").У женщин с гипертриглицеридемией (или наличием этого состояния в семейном анамнезе) возможно повышение риска развития панкреатита во время приема КОК. Несмотря на то, что небольшое повышение артериального давления было описано у многих женщин, принимающих КОК, клинически значимые повышения отмечались редко. Тем не менее, если во время приема препарата развивается стойкое, клинически значимое повышение артериального давления, следует отменить эти препараты и начать лечение артериальной гипертензии. Прием препарата может быть продолжен, если с помощью гипотензивной терапии достигнуты нормальные значения артериального давления. Следующие состояния, как сообщалось, развиваются или ухудшаются как во время беременности, так и при приеме КОК, но их связь с приемом КОК не доказана: желтуха и/или зуд, связанный с холестазом: формирование камней в желчном пузыре: порфирия: системная красная волчанка: гемолитико-уремический синдром: хорея Сиденгама: герпес во время беременности: потеря слуха, связанная с отосклерозом. Также описаны случаи ухудшения течения эндогенной депрессии, эпилепсии, болезни Крона и язвенного колита на фоне применения КОК.У женщин с наследственными формами ангионевротического отека экзогенные эстрогены могут вызывать или ухудшать симптомы ангионевротического отека. Острые или хронические нарушения функции печени могут потребовать отмены препарата до тех пор, пока показатели функции печени не вернутся в норму. Рецидив холестатической желтухи, развившейся впервые во время предшествующей беременности или предыдущего приема половых гормонов, требует прекращения приема препарата. Хотя КОК могут оказывать влияние на инсулинорезистентность и толерантность к глюкозе, необходимости в коррекции дозы гипогликемических препаратов у пациенток с сахарным диабетом, использующих низкодозированные КОК (<:0,05 мг этинилэстрадиола), как правило, не возникает. Тем не менее женщины с сахарным диабетом должны тщательно наблюдаться во время приема КОК. Иногда может развиваться хлоазма, особенно у женщин с наличием в анамнезе хлоазмы беременных. Женщины со склонностью к хлоазме во время приема препарата Ярина® должны избегать длительного пребывания на солнце и воздействия ультрафиолетового излучения. Доклинические данные по безопасности. Доклинические данные, полученные в ходе стандартных исследований на предмет выявления токсичности при многократном приеме доз препарата, а также генотоксичности, канцерогенного потенциала и токсичности для репродуктивной системы, не указывают на наличие особого риска для человека. Тем не менее следует помнить, что половые гормоны могут способствовать росту некоторых гормонозависимых тканей и опухолей. Лабораторные тесты. Прием препарата Ярина® может влиять на результаты некоторых лабораторных тестов, включая показатели функции печени, почек, щитовидной железы, надпочечников, концентрацию транспортных белков в плазме, показатели углеводного обмена, параметры свертывания крови и фибринолиза. Изменения обычно не выходят за границы нормальных значений. Дроспиренон увеличивает активность ренина плазмы и концентрацию альдостерона, что связано с его антиминералокортикоидным эффектом. Снижение эффективности. Эффективность препарата Ярина® может быть снижена в следующих случаях: при пропуске таблеток, желудочно-кишечных расстройствах или в результате лекарственного взаимодействия. Частота и выраженность менструальноподобных кровотечений. На фоне приема препарата Ярина® могут наблюдаться нерегулярные (ациклические) кровотечения из влагалища ("мажущие" кровянистые выделения и/или "прорывные" маточные кровотечения), особенно в течение первых месяцев применения. Поэтому оценка любых нерегулярных менструальноподобных кровотечений должна проводиться после периода адаптации, составляющего приблизительно три цикла. Если нерегулярные менструальноподобные кровотечения повторяются или развиваются после предшествующих регулярных циклов, следует провести тщательное обследование для исключения злокачественных новообразований или беременности.У некоторых женщин во время перерыва в приеме таблеток может не развиться кровотечения "отмены". Если препарат Ярина® принимался согласно рекомендациям, маловероятно, что женщина беременна. Тем не менее при нерегулярном применении препарата и отсутствии двух подряд менструальноподобных кровотечений прием препарата не может быть продолжен до исключения беременности. Медицинские осмотры. Перед началом или возобновлением применения препарата Ярина® необходимо ознакомиться с анамнезом жизни, семейным анамнезом женщины, провести тщательное общемедицинское и гинекологическое обследование, исключить беременность. Объем исследований и частота контрольных осмотров должны основываться на существующих нормах медицинской практики при необходимом учете индивидуальных особенностей каждой пациентки. Как правило, измеряется артериальное давление, частота сердечных сокращений, определяется индекс массы тела, проверяется состояние молочных желез, брюшной полости и органов малого таза, включая цитологическое исследование эпителия шейки матки (тест по Папаниколау). Обычно контрольные обследования следует проводить не реже 1 раза в 6 месяцев. Необходимо иметь в виду, что препарат Ярина® не предохраняет от ВИЧ-инфекции (СПИД) и других заболеваний, передающихся половым путем. Состояния, требующие консультации врача- какие-либо изменения в здоровье, особенно возникновение состояний, перечисленных в разделах "Противопоказания" и "Применение с осторожностью"- локальное уплотнение в молочной железе- одновременный прием других лекарственных препаратов (см. также "Взаимодействие с другими лекарственными средствами")- если ожидается длительная неподвижность (например, на нижнюю конечность наложен гипс), планируется госпитализация или операция (по крайней мере за 4 недели до предполагаемой операции)- необычно сильное кровотечение из влагалища- пропущена таблетка в первую неделю приема упаковки и был половой контакт за семь или менее дней до этого- отсутствие очередного менструальноподобного кровотечения два раза подряд или подозрение на беременность (не следует начинать прием таблеток из следующей упаковки до консультации с врачом). Следует прекратить прием таблеток и немедленно проконсультироваться с врачом, если имеются возможные признаки тромбоза, инфаркта миокарда или инсульта: необычный кашель: необычно сильная боль за грудиной, отдающая в левую руку: неожиданно возникшая одышка, необычная, сильная и длительная головная боль или приступ мигрени: частичная или полная потеря зрения или двоение в глазах: нечленораздельная речь: внезапные изменения слуха, обоняния или вкуса: головокружение или обморок: слабость или потеря чувствительности и любой части тела: сильная боль в животе: сильная боль в нижней конечности или внезапно возникший отек любой из нижних конечностей. Влияние на способность управлять транспортными средствами: Не выявлено. Условия хранения и отпуска из аптек Условия хранения:Хранить при температуре не выше 25 °С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Ярина® Международное непатентованное название:Дроспиренон + Этинилэстрадиол. Форма выпуска:таблетки, покрытые пленочной оболочкой. Состав: Каждая таблетка, покрытая пленочной оболочкой, содержит:Ядро таблетки:активные вещества: этинилэстрадиол - 30 мкг, дроспиренон - 3 мг:вспомогательные вещества: лактозы моногидрат - 48,170 мг, крахмал кукурузный - 14,400 мг, крахмал кукурузный прежелатинизированный - 9,600 мг, повидон К25 - 4,000 мг, магния стеарат - 800 мкг. Оболочка таблетки: гипромеллоза (гидроксипропилметилцеллюлоза) - 1,0112 мг, макрогол 6000 - 202,4 мкг, тальк (магния гидросиликат) - 202,4 мкг, титана диоксид (Е 171) - 556,5 мкг, железа (II) оксид (Е 172) - 27,5 мкг. АТХ: Регистрация: Лекарственное средство П N013882/01 Фармгруппа: контрацептивное средство комбинированное (эстроген+гестаген)Дата регистрации: 02.04.2008 / 11.09.2014. Окончание регстрации: . Описание:Таблетки, покрытые пленочной оболочкой, светло-желтого цвета, с одной стороны выгравирован шестиугольник, внутри которого буквы "DO". Упаковка:Таблетки, покрытые пленочной оболочкой, 3 мг + 0,03 мг. По 21 таблетке помещают в блистер из алюминиевой фольги и поливинилхлоридной пленки. 1 или 3 блистера вместе с кармашком для ношения блистера с инструкцией по применению помещают в картонную пачку. Срок годности:3 года. Не применять по истечении срока годности. Владелец рег.удостоверения:Байер Фарма АГ Производитель:BAYER PHARMA, AG. Представительство:БАЙЕР, АО. Информация предоставлена: Компанией ГЭОТАР - http://www.lsgeotar.ru/

Модель:
RUR 834
Показания Лечение нейропатической боли у взрослых (18 лет и старше). Эффективность и. безопасность у пациентов в возрасте до 18 лет не установлены- Монотерапия парциальных судорог при эпилепсии со вторичной генерализацией и без нее у взрослых и детей в возрасте старше 12 лет. Эффективность и безопасность монотерапии у детей в возрасте до 12 лет не установлены- Как дополнительное средство при лечении парциальных судорог при эпилепсии со вторичной генерализацией и без нее у взрослых и детей в возрасте 3 лет и старше. Безопасность и эффективность дополнительной терапии габапентином у детей в возрасте менее 3 лет не установлены. Противопоказания Противопоказания Повышенная чувствительность к габапентину или вспомогательным компонентам препарата. Детский возраст до 3 лет. С осторожностью: Почечная недостаточность (см. "Способ применения и дозы"). Беременность Беременность. Данные о безопасности и эффективности применения препарата при беременности отсутствуют, поэтому применение габапентина при беременности возможно только в том случае, если предполагаемая польза для матери оправдывает возможный риск для плода. Лактация. Габапентин выводится с грудным молоком, поэтому во время лечения следует отказаться от грудного вскармливания. Применение и дозы Препарат Катэна® назначают внутрь, независимо от приема пищи. Если необходимо снизить дозу, отменить препарат или заменить его на альтернативное средство, это следует делать постепенно в течение минимум одной недели. Нейропатическая боль у взрослых. Начальная доза составляет 900 мг в сутки в три приема равными дозами: при необходимости, в зависимости от эффекта, дозу постепенно увеличивают до максимальной - 3600 мг/сут. Лечение можно начинать сразу с дозы 900 мг/сут (по 300 мг 3 раза в сутки) или в течение первых 3-х дней дозу можно увеличивать постепенно до 900 мг в сутки по следующей схеме:1- й день: 300 мг 1 раз в сутки 2- й день: по 300 мг 2 раза в сутки 3- й день: по 300 мг 3 раза в сутки. Парциальные судороги. Взрослые и дети в возрасте старше 12 лет: Эффективная доза - от 900 до 3600 мг в сутки. Терапию можно начать с дозы 300 мг 3 раза в сутки в первый день или увеличивать постепенно до 900 мг по схеме, описанной выше (см. раздел "Нейропатическая боль у взрослых"). В последующем доза может быть увеличена до максимальной - 3600 мг/сут в три приема равными дозами. Максимальный интервал между дозами при трехкратном приеме препарата не должен превышать 12 ч во избежание возобновления судорог. Отмечена хорошая переносимость препарата в дозах до 4800 мг/сут. Дети в возрасте 3-12 лет: Начальная доза препарата варьирует от 10 до 15 мг/кг/сут, которую назначают равными дозами 3 раза в сутки и повышают до эффективной приблизительно в течение 3-х дней. Эффективная доза габапентина у детей в возрасте 5 лет и старше составляет 25-35 мг/кг/сут равными дозами в 3 приема. Эффективная доза габапентина у детей в возрасте от 3 до 5 лет составляет 40 мг/кг/сут равными дозами в три приема. Отмечена хорошая переносимость препарата в дозах до 50 мг/кг/сут при длительном применении. Максимальный интервал между приемом доз препарата не должен превышать 12 часов во избежание возобновления судорог. Нет необходимости контролировать концентрацию габапентина в плазме. Препарат Катэна® может использоваться в комбинации с другими противосудорожными препаратами без учета изменения его концентрации в плазме или концентрации других противосудорожных препаратов в сыворотке. Подбор дозы при почечной недостаточности. Пациентам с почечной недостаточностью рекомендуется снижение дозы габапентина согласно таблице:ТАБЛИЦЪ Суточную дозу следует назначать в три приема. Назначают по 300 мг через день. Рекомендации для пациентов, находящихся на гемодиализе. Пациентам, находящимся на гемодиализе, которые ранее не принимали габапентин, препарат рекомендуется назначать в насыщающей дозе 300-400 мг, а затем применять его по 200-300 мг каждые 4 ч гемодиализа. Побочные эффекты и передозировка Побочные эффекты: Со стороны сердечно-сосудистой системы: симптомы вазодилатации, гипертензия. Со стороны пищеварительной системы: диспепсия, метеоризм, тошнота, рвота, боль в животе, запор, диарея, сухость во рту или глотке, анорексия, гингивит, заболевания зубов, увеличение аппетита, повышение активности "печеночных" трансаминаз. Со стороны опорно-двигательного аппарата: миалгия, артралгия, боль в спине, повышенная ломкость костей. Со стороны нервной системы: сонливость, головокружение, атаксия, амнезия, спутанность сознания, нарушении координации, повышенная утомляемость, нарушение мышления, тремор, гипестезия, депрессия, дизартрия, бессонница, нервозность, нистагм, усиление, ослабление или отсутствие рефлексов, астения, тревожность, враждебность, гиперкинезия, эмоциональная лабильность. Со стороны дыхательной системы: фарингит, ринит, одышка, кашель, пневмония, бронхит, респираторные инфекции. Со стороны мочеполовой системы: инфекции мочевых путей, импотенция. Со стороны органов чувств: нарушение зрения, амблиопия, диплопия. Со стороны органов кроветворения: лейкопения, пурпура (чаще всего ее описывают как кровоподтеки, возникавшие при физической травме). Аллергические реакции: кожная сыпь, зуд, акне. Прочие: лихорадка, вирусная инфекция, увеличение массы тела, боль различной локализации, периферические отеки, отек лица, головная боль. Пострегистрационный опыт применения. Зарегистрированы случаи внезапной необъяснимой смерти, связь которых с лечением габапентином не установлена. Другие нежелательные явления: острая почечная недостаточность, аллергические реакции, включая крапивницу, алопеция, ангионевротический отек, генерализованный отек: колебания концентрации глюкозы в крови у больных сахарным диабетом, боль в груди, увеличение в объеме молочных желез, гинекомастия, повышение показателей функции печени, мультиформная экссудативная эритема (в том числе синдром Стивенса-Джонсона), галлюцинации, двигательные расстройства, такие как хореоатетоз, дискинезия и дистония, сердцебиение, панкреатит, шум в ушах, тромбоцитопения, недержание мочи, миоклонус. Передозировка: Симптомы: головокружение, двоение в глазах, нарушение речи, сонливость, летаргия и диарея. Лечение: промывание желудка, прием активированного угля, симптоматическая терапия. Пациентам с тяжелой почечной недостаточностью может быть показан гемодиализ. Взаимодействие с другими ЛС: При одновременном применении габапентина и морфина, когда морфин принимался за 2 часа до приема габапентина, наблюдалось увеличение среднего значения площади под фармакокинетической кривой "концентрация - время" (AUC) габапентина на 44% по сравнению с ионотерапией габапентином, что ассоциировалось с увеличением болевого порога (холодовый прессорный тест). Клиническое значение этого изменения не установлено, фармакокинетические характеристики морфина при этом не изменялись. Побочные эффекты морфина при совместном приеме с габапентином не отличались от таковых при приеме морфина совместно с плацебо. Взаимодействия между габапентином и фенобарбиталом, фенитоином, вальпроевой кислотой и карбамазепином не отмечено. Фармакокинетика габапентина в равновесном состоянии одинакова у здоровых людей и пациентов, получающих другие противосудорожные средства. Одновременное применение габапентина с пероральными контрацептивами, содержащими норэтистерон и/или этинилэстрадиол, не сопровождалось изменениями фармакокинетики обоих компонентов. Одновременное применение габапентина с антацидами, содержащими алюминий и магний, сопровождается снижением биодоступности габапентина примерно на 20%. Габапентин рекомендуется принимать примерно через 2 ч после приема антацида. Пробенецид не влияет на почечную экскрецию габапентина. Небольшое снижение почечной экскреции габапентина при одновременном приеме циметидина, вероятно, не имеет клинического значения. Фармакологическое действие и фармакокинетика Габапентин по строению сходен с нейротрансмиттером гамма-аминомаслянной кислотой (ГАМК), однако его механизм действия отличается от такового некоторых других препаратов, взаимодействующих с ГАМК-рецепторами, включая вальпроат, барбитураты, бензодиазепины, ингибиторы ГАМК-трансаминазы, ингибиторы захвата ГАМК, агонисты ГАМК и про лекарственные формы ГАМК: он не обладает ГАМК-ергическими свойствами и не влияет за захват и метаболизм ГАМК. Предварительные исследования показали, что габапентин связывается с α 2-δ-субъединицей вольтаж-зависимых кальциевых каналов и подавляет поток ионов кальция, играющий важную роль в возникновении нейропатической боли. Другими механизмами, участвующими в действии габапентина при нейропатической боли являются: уменьшение глутамат-зависимой гибели нейронов, увеличение синтеза ГАМК, подавление высвобождения нейротрансмитгеров моноаминовой группы. Габапентин в клинически значимых концентрациях не связывается с рецепторами других распространенных препаратов или нейротрансмиттеров, включая рецепторы ГАМКА, ГАМКВ, бензодиазепиновые, глутамата, глицина или N-метил-D-аспартата. В отличие от фенитоина и карбамазепина габапентин не взаимодействует с натриевыми каналами. Фармакокинетика: Всасывание. Биодоступность габапентина не пропорциональна дозе: так, при увеличении дозы она снижается. После приема внутрь максимальная концентрация (Cmax) габапентина в плазме достигается через 2-3 ч. Абсолютная биодоступность габапентина в капсулах составляет около 60%. Пища, в том числе с большим содержанием жиров, не оказывает влияния на фармакокинетику. Выведение габапентина из плазмы лучше всего описывается с помощью линейной модели. Распределение. Фармакокинетика не меняется при повторном применении: равновесные концентрации в плазме можно предсказать на основании результатов однократного приема препарата. Габапентин практически не связывается с белками плазмы (<:3%) и имеет объем распределения 57,7 л. Метаболизм. Признаков метаболизма у человека не обнаружено. Препарат не индуцирует окислительные ферменты печени со смешанной функцией, участвующие в метаболизме лекарственных средств. Выведение. Период полувыведения (T1/2) из плазмы не зависит от дозы и составляет в среднем 5-7 ч. Выводится исключительно почками в неизмененном виде. Фармакокинетика в особых клинических случаях. Клиренс габапентина из плазмы снижается у пожилых людей и больных с нарушенной функцией почек. Константа скорости выведения, клиренс из плазмы и почечный клиренс прямо пропорциональны клиренсу креатинина. Габапентин удаляется из плазмы при гемодиализе. У больных с нарушенной функцией почек и пациентов, получающих лечение гемодиализом, рекомендуется коррекция дозы (см. Способ применения и дозы). Установлено, что концентрации габапентина в плазме у детей в возрасте от 4 до 12 лет в целом сходны с таковыми у взрослых. Особые указания При совместной терапии морфином у пациентов может произойти повышении концентрации габапентина. При этом необходимо обеспечить тщательное наблюдение за пациентами на предмет развития такого признака угнетения центральной нервной системы (ЦНС), как сонливость. В этом случае доза габапентина или морфина должна быть адекватно снижена (см. "Взаимодействие с другими лекарственными средствами"). Лабораторные исследования. При совместном применении габапентина и других противосудорожных средств были зарегистрированы ложноположительные результаты при определении белка.в моче с помощью тест-полосок Ames N-Multistix SG®. Для определения белка в моче рекомендуется пользоваться более специфичным методом преципитации сульфосалициловой кислотой. Влияние на способность управлять транспортными средствами: В период лечения необходимо воздержаться от вождения автотранспорта и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25°С. Хранить в недоступном для детей месте! Отпуск из аптек: По рецепту Регистрационные данные Торговое название Катэна® Международное непатентованное название:Габапентин. Форма выпуска:капсулы. Состав:Одна капсула содержит:Капсулы 100 мг: активное вещество: габапентин - 100 мг: вспомогательные вещества: лактозы моногидрат, крахмал кукурузный, тальк: капсульная оболочка: титана диоксид (Е 171), желатин. Капсулы 300 мг: активное вещество: габапентин - 300 мг: вспомогательные вещества: лактозы моногидрат, крахмал кукурузный, тальк: капсульная оболочка: титана диоксид (Е 171), краситель железа оксид желтый (Е 172), желатин. Капсулы 400 мг: активное вещество: габапентин - 400 мг: вспомогательные вещества: лактозы моногидрат, крахмал кукурузный, тальк: капсульная оболочка: титана диоксид (Е 171), краситель железа оксид желтый (Е 172), краситель железа оксид красный (Е 172), желатин. АТХ: Регистрация: Лекарственное средство ЛСР-002168/10 Фармгруппа: Противоэпилептическое средство. Дата регистрации: 17.03.2010 / 07.06.2010. Окончание регстрации: . Описание:Капсулы 100 мг: белый кристаллический порошок в капсульной оболочке белого цвета, размер 3. Капсулы 300 мг: белый кристаллический порошок в капсульной оболочке желтого цвета, размер 1. Капсулы 400 мг: белый кристаллический порошок в капсульной оболочке оранжевого цвета, размер 0. Упаковка:Капсулы 100 мг, 300 мг, 400 мг. Капсулы 100 мг: По 10 капсул в ПВХ/Ал блистере. Два блистера помещают вместе с инструкцией по применению в картонную пачку. Капсулы 300 мг и 400 мг: По 10 капсул в ПВХ/Ал блистере. Пять блистеров помещают вместе с инструкцией по применению в картонную пачку. Срок годности:3 года. Не применять по истечении срока годности. Владелец рег.удостоверения:БЕЛУПО, лекарства и косметика д.д. Производитель:BELUPO, Pharmaceuticals &: Cosmetics, d.d. Представительство:БЕЛУПО, лекарства и косметика д.д
Модель:
RUR 23
Показания Артериальная гипертензия (монотерапия или в комбинации с другими анти- гипертензивными средствами). Стенокардия напряжения, вазоспастическая стенокардия (стенокардия Принцметала). Противопоказания Противопоказания - повышенная чувствительность к амлодипину и другим производным дигидропиридина: - выраженная артериальная гипотензия: - коллапс, кардиогенный шок: - нестабильная стенокардия (за исключением стенокардии Принцметала): - беременность и период лактации: - возраст до 18 лет (эффективность и безопасность не установлены). С осторожностью: С осторожностью: нарушение функции печени, синдром слабости синусового узла (выраженная брадикардия, тахикардия), хроническая сердечная недостаточность в стадии декомпенсации, мягкая или умеренная степень артериальной гипотензии, аортальный стеноз, митральный стеноз, гипертрофическая обструктивная кардиомиопатия, острый инфаркт миокарда (и в течение 1 месяца после), сахарный диабет, нарушение липидного профиля, пожилой возраст. Беременность Противопоказан. Применение и дозы Внутрь, начальная доза для лечения артериальной гипертензии и стенокардии составляет 5 мг препарата 1 раз в сутки. Доза максимально может быть увеличена до 10 мг однократно в сутки. При артериальной гипертензии поддерживающая доза может быть 5 мг в сутки. При стенокардии напряжения и вазоспастической стенокардии - 5-10 мг/сут однократно: для профилактики приступов стенокардии -10 мг/сут. Не требуется изменения дозы при одновременном назначении с тиазидными диуретиками, бета-адреноблокаторами и ингибиторами ангиотензинпревращающего фермента (АПФ). Не требуется изменения дозы у пациентов с почечной недостаточностью. Побочные эффекты и передозировка Побочные эффекты: Со стороны сердечно-сосудистой системы: сердцебиение, одышка, выраженное снижение артериального давления, обморок, васкулит, отеки (отечность лодыжек и стоп), “приливы” крови к лицу, редко - нарушения ритма (брадикардия, желудочковая тахикардия, трепетание предсердий), боль в грудной клетке, ортостатическая гипотензия, очень редко - развитие или усугубление сердечной недостаточности, экстрасистолия, мигрень. Со стороны центральной нервной системы: головная боль, головокружение, утомляемость, сонливость, изменение настроения, судороги, редко - потеря сознания, гипестезия, нервозность, парестезии, тремор, вертиго, астения, недомогание, бессонница, депрессия, необычные сновидения, очень редко - атаксия, апатия, ажитация, амнезия. Со стороны пищеварительной системы: тошнота, рвота, боли в эпигастрии, редко - повышение уровня “печеночных” трансаминаз и желтуха (обусловленные холестазом), панкреатит, сухость во рту, метеоризм, гиперплазия десен, запор или диарея, очень редко - гастрит, повышение аппетита, анорексия, гипербилирубинемия. Со стороны мочеполовой системы: редко - поллакиурия, болезненные позывы на мочеиспускание, никтурия, нарушение сексуальной функции (в том числе снижение потенции): очень редко - дизурия, полиурия. Со стороны кожных покровов: очень редко - ксеродермия, алопеция, дерматит, пурпура, изменение цвета кожи. Аллергические реакции: кожный зуд, сыпь (в том числе эритематозная, макулопапулезная сыпь, крапивница), ангионевротический отек. Со стороны опорно-двигательного аппарата: редко - артралгия, артроз, миалгия (при длительном применении): очень редко - миастения. Прочие: редко - гинекомастия, гиперурикемия, увеличение/снижение массы тела, тромбоцитопения, лейкопения, гипергликемия, нарушение зрения, диплопия, конъюнктивит, боль в глазах, звон в ушах, боль в спине, диспноэ, носовое кровотечение, повышенное потоотделение, жажда: очень редко - холодный липкий пот, кашель, ринит, паросмия, нарушение вкусовых ощущений, нарушение аккомодации, ксерофтальмия. Передозировка: Симптомы: выраженное снижение артериального давления, тахикардия, чрезмерная периферическая вазодилатация. Лечение: промывание желудка, назначение активированного угля, поддержание функции сердечно-сосудистой системы, контроль показателей функции сердца и легких, контроль за объемом циркулирующей крови и диурезом, придание больному горизонтального положения с приподнятыми ногами. Для восстановления тонуса сосудов - применение сосудосуживающих препаратов (при отсутствии противопоказаний к их применению): для устранения последствий блокады кальциевых каналов - внутривенное введение глюконата кальция. Гемодиализ не эффективен. Взаимодействие с другими ЛС: Ингибиторы микросомального окисления повышают концентрацию амлоди-пина в плазме крови, усиливая риск развития побочных эффектов, а индукторы микросомальных ферментов печени уменьшают. Гипотензивный эффект ослабляют нестероидные противовоспалительные препараты, особенно индометацин (задержка натрия и блокада синтеза простагландинов почками), альфа-адреностимуляторы, эстрогены (задержка натрия), симпатомиметики. Тиазидные и “петлевые” диуретики, бета-адреноблокаторы, верапамил, ингибиторы АПФ и нитраты усиливают антиангинальный и гипотензивный эффекты. Амиодарон, хинидин, альфа 1-адреноблокаторы, антипсихотические лекарственные средства (нейролептики) и блокаторы “медленных” кальциевых каналов могут усиливать гипотензивное действие. Не оказывает влияния на фармакокинетические параметры дигоксина и варфарина. Циметидин не влияет на фармакокинетику амлодипина. При совместном применении с препаратами лития возможно усиление проявлений их нейротоксичности (тошнота, рвота, диарея, атаксия, тремор, шум в ушах). Препараты кальция могут уменьшить эффект блокаторов “медленных” кальциевых каналов. Прокаинамид, хинидин и другие лекарственные средства, вызывающие удлинение интервала QT, усиливают отрицательный инотропный эффект и могут повышать риск значительного удлинения интервала QT. Грейпфрутовый сок может снижать концентрацию амлодипина в плазме крови, однако это снижение настолько мало, что значимо не изменяет действие амлодипина. Фармакологическое действие и фармакокинетика Производное дигидропиридина - блокатор “медленных” кальциевых каналов II поколения, оказывает антиангинальное и гипотензивное действие. Связываясь с дигидропиридиновыми рецепторами, блокирует кальциевые каналы, снижает трансмембранный переход ионов кальция в клетку (в большей степени в гладкомышечные клетки сосудов, чем в кардиомиоциты). Антиангинальное действие обусловлено расширением коронарных и периферических артерий и артериол: при стенокардии уменьшает выраженность ишемии миокарда: расширяя периферические артериолы, снижает общее периферическое сосудистое сопротивление, уменьшает преднагрузку на сердце, снижает потребность миокарда в кислороде. Расширяя главные коронарные артерии и артериолы в неизмененных и ишемизированных зонах миокарда, увеличивает поступление кислорода в миокард (особенно при вазоспастической стенокардии): предотвращает развитие констрикции коронарных артерий (в т.ч. вызванной курением). У больных стенокардией разовая суточная доза увеличивает время выполнения физической нагрузки, замедляет развитие стенокардии и “ишемической” депрессии сегмента ST, снижает частоту приступов стенокардии и потребления нитроглицерина. Оказывает длительный дозозависимый гипотензивный эффект. Гипотензивное действие обусловлено прямым вазодилатирующим влиянием на гладкие мышцы сосудов. При артериальной гипертензии разовая доза обеспечивает клинически значимое снижение артериального давления (АД) на протяжении 24 ч (в положении больного “лежа” и “стоя”). Не вызывает резкого снижения АД, снижения толерантности к физической нагрузке, фракции выброса левого желудочка. Уменьшает степень гипертрофии миокарда левого желудочка, оказывает антиатеросклеротическое и кардиопротекторное действие при ишемической болезни сердца (ИБС). Не оказывает влияния на сократимость и проводимость миокарда, не вызывает рефлекторного увеличения частоты сердечных сокращений (ЧСС), тормозит агрегацию тромбоцитов, повышает скорость клубочковой фильтрации, обладает слабым натрийуретическим действием. При диабетической нефропатии не увеличивает выраженность микроальбуминурии. Не оказывает неблагоприятных влияний на обмен веществ и липиды плазмы крови. Время наступления эффекта - 2-4 часа, длительность эффекта 24 часа. Фармакокинетика: После перорального приема амлодипин медленно абсорбируется из желудочно-кишечного тракта. Средняя абсолютная биодоступность составляет 64 %, максимальная концентрация в сыворотке крови наблюдается через 6-9 часов. Концентрация стабильного равновесия достигается после 7 дней терапии. Пища не влияет на абсорбцию амлодипина. Средний объем распределения составляет 21 л/кг массы тела, что указывает на то, что большая часть препарата находится в тканях, а относительно меньшая - в крови. Большая часть препарата, находящегося в крови (95 %), связывается с белками плазмы крови. Амлодипин подвергается медленному, но экстенсивному метаболизму (90 %) в печени с образованием неактивных метаболитов, имеет эффект “первого прохождения” через печень. Метаболиты не обладают значимой фармакологической активностью. После однократного перорального приема период полувыведения (Т1/2) варьирует от 31 до 48 часов, при повторном назначении Т1/2 составляет приблизительно 45 часов. Около 60 % принятой внутрь дозы экскретируется с мочой преимущественно в виде метаболитов, 10 % в неизмененном виде, а 20-25 % с калом, а также с грудным молоком. Общий клиренс амлодипина составляет 0,116 мл/с/кг (7 мл/мин/кг, 0,42 л/ч/кг). У пожилых пациентов (старше 65 лет) выведение амлодипина замедлено (Т1/2 65 ч) по сравнению с молодыми пациентами, однако эта разница не имеет клинического значения. У пациентов с печеночной недостаточностью предполагается удлинение Т1/2, и при длительном назначении кумуляция препарата в организме будет выше (Т1/2 до 60 ч). Почечная недостаточность не оказывает существенного влияния на кинетику амлодипина. Препарат проникает через гематоэнцефалический барьер. При гемодиализе не удаляется. Особые указания В период лечения необходим контроль за массой тела и потреблением натрия, назначение соответствующей диеты. Необходимо поддержание гигиены зубов и частое посещение стоматолога (для предотвращения болезненности, кровоточивости и гиперплазии десен). Режим дозирования для пожилых такой же, как и для пациентов других возрастных групп. При увеличении дозы необходимо тщательное наблюдение за пожилыми пациентами. Несмотря на отсутствие у блокаторов “медленных” кальциевых каналов синдрома “отмены”, перед прекращением лечения рекомендуется постепенное уменьшение доз. Амлодипин не влияет на плазменные концентрации К, глюкозы, триглицеридов, общего холестерина, ЛПНП, мочевой кислоты, креатинина и азота мочевой кислоты. Влияние на способность управлять транспортными средствами: Не было сообщений о влиянии амлодипина на управление автомобилем или работу с механизмами. Тем не менее, у некоторых пациентов преимущественно в начале лечения могут возникать сонливость и головокружение. При их возникновении пациент должен соблюдать особые меры предосторожности при управлении автомобилем и работе с механизмами. Условия хранения и отпуска из аптек Условия хранения:В защищенном от света месте при температуре не выше 25 °С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Амлодипин Международное непатентованное название:Амлодипин. Форма выпуска:Таблетки. Состав:одна таблетка содержит активное вещество амлодипина бесилат в пересчете на амлодипин - 5 мг или 10 мг: вспомогательные вещества: целлюлоза микрокристаллическая, лактоза (сахар молочный), кроскармеллоза натрия (примеллоза), кальция стеарат (кальция октадеканоат). АТХ: Регистрация: Лекарственное средство ЛСР-008198/08 Фармгруппа: блокатор "медленных" кальциевых каналов. Дата регистрации: 16.10.2008. Окончание регстрации: . Описание:таблетки белого или почти белого цвета, плоскоцилиндрические с фаской. Упаковка:Таблетки 5 мг, 10 мг. По 10, 15, 20 или 30 таблеток в контурную ячейковую упаковку. 1, 2, 3 или 6 контурных ячейковых упаковок по 10 таблеток, 2 или 4 контурные ячейковые упаковки по 15 таблеток, 1 или 3 контурные ячейковые упаковки по 20 таблеток, или 1 или 2 контурные ячейковые упаковки по 30 таблеток вместе с инструкцией по применению помещают в пачку из картона. Срок годности:2 года. Не использовать по истечении срока годности. Владелец рег.удостоверения: Производитель:ВЕРТЕКС, АО. Представительство
Модель:
RUR 1209
Показания эссенциальная артериальная гипертензия (при неэффективности монотерапии олмесартаном медоксомилом). Противопоказания Противопоказания - повышенная чувствительность к действующему веществу или к любому из вспомогательных веществ, входящих в состав препарата (см. раздел Состав)- обструкция желчевыводящих путей- почечная недостаточность (клиренс креатинина (ЮС) менее 20 мл/мин.), состояние после трансплантации почки (нет опыта клинического применения)- беременность, период лактации: возраст до 18 лет (эффективность и безопасность не установлены)- дефицит лактазы, галактоземия или синдрюм мал абсорбции. С осторожностью: - стеноз аортального или митрального клапанов: гипертрофическая обструктивная кардиомиопатия- первичный альдостеронизм- гиперкалиемия, гипонатрнемия (риск дегидратации, артериальной гипотензии, почечной недостаточности)- почечная недостаточность (КК более 20 мл/мин.)- хроническая сердечная недостаточность- двухсторонний стеноз почечных артерий или стеноз артерии единственной почки- ишемическая болезнь сердца- цереброваскулярные заболевания- пожилой возраст (старше 65 лет)- нарушение функции печени- состояния, сопровождающиеся снижением объема циркулирующей крови (в том числе диарея, рвота), а также у пациентов, соблюдающих диету с ограничением натрия- при одновременном применении с диуретиками. Беременность Опыт применения олмесартана медоксомила у беременных отсутствует. Однако ввиду имеющихся сообщений о тяжелом тератогенном действии лекарственных средств, действующих непосредственно на ренин-ангиотензиновую систему, как и любой лекарственный препарат этого класса, олмесартан противопоказан во время беременности. В случае наступления беременности во время терапии препаратом Кардосал 10 препарат необходимо отменить. Нет данных выделяется ли олмесартан с грудным молоком, поэтому при необходимости применения препарата Кардосал 10 в период лактации грудное вскармливание на период приема препарата следует прекратить. Применение и дозы Таблетки Кардосал® плюс принимают внутрь независимо от приема пищи. Перед назначением комбинированного препарата Кардосал® плюс рекомендуется предварительный подбор дозы каждого из действующих веществ в отдельности (т.е. олмесартана медоксомила и гидрохлоротиазида). Рекомендуемая доза: Ежедневно по 1 таблетке препарата Кардосал® плюс, содержащего 20 мг олмесартана медоксомила и 12,5 мг гидрохлоротиазида, при отсутствии адекватного контроля АД на фоне монотерапии олмесартаном медоксомилом в дозе 20 мг; При отсутствии адекватного контроля артериального давления на фоне приема препарата Кардосал® плюс, содержащего 20 мг олмесартана медоксомила и 12,5 мг гидрохлоротиазида, возможно применение препарата Кардосал® плюс, содержащего 20 мг олмесартана медоксомила и 25 мг гидрохлоротиазида ежедневно по 1 таблетке. Максимальная доза препарата Кардосал® плюс составляет 20 мг олмесартана медоксомила и 25 мг гидрохлоротиазида 1 раз в сутки. Пожилым пациентам (старше 65 лет) с нормальной функцией почек (КК более 90 мл/мин) и пациентам с нарушением функции почек (КК = 30-60 мл/мин.) коррекции дозы препарата не требуется. Побочные эффекты и передозировка Побочные эффекты: Возможные побочные эффекты приведены ниже по нисходящей частоте возникновения: очень часто (>: 1/10): часто (>: 1/100 <: 1/10): иногда (>: 1/1000, <: 1/100): редко (>: 1/10000, <: 1/1000): очень редко (<: 1/10000), включая отдельные сообщения. Со стороны кровеносной и лимфатической системы:Очень редко: тромбоцитопения. Со стороны центральной нервной системы:Иногда: головокружение. Очень редко: головная боль. Со стороны дыхательной системы:Часто: фарингит, ринит. Очень редко: кашель, бронхит. Со стороны пищеварительного тракта:Часто: диарея, диспепсия, гастроэнтерит. Очень редко: боль в животе, тошнота, рвота. Со стороны кожных покровов:Очень редко: кожный зуд, сыпь, ангионевротический отек, аллергический дерматит, крапивница. Со стороны опорно-двигательного аппарата Часто: боль в спине, боль в костях, артралгия, артрит. Очень редко: судороги мышц, миалгия. Со стороны мочевыделительной системы: Часто: гематурия, инфекция мочевых путей. Очень редко: острая почечная недостаточность. Со стороны лабораторных показателей:Очень редко: повышение уровня креатинина и мочевины в сыворотке крови, повышение активности ферментов печени. Со стороны сердечно-сосудистой системы: Редко: избыточное снижение АД. Иногда: стенокардия, тахикардия. Со стороны обмена веществ:Часто: повышение уровня креатинфосфокиназы, гипертриглицеридемия, гиперурикемия. Редко: гиперкалиемия. Прочие нарушения. Часто: боль в грудной клетке, гриппоподобные симптомы, периферические отеки. Очень редко: астения, утомляемость, недомогание, сонливость. Передозировка: Симптомы: выраженное снижение АД. Лечение: при выраженном снижении АД рекомендуется уложить пациента на спину, приподняв ноги. Рекомендовано промывание желудка и/или прием активированного угля, терапия, направленная на коррекцию дегидратации и нарушений водно-солевого обмена, восполнение объема циркулирующей крови. Взаимодействие с другими ЛС: Не рекомендуется совместное применение с калийсберегающими диуретиками, препаратами калия, заменителями солей, содержащих калий, или другими лекарственными средствами, способными повысить уровень калия в сыворотке крови (например, гепарин), это может привести к повышению уровня калия в сыворотке крови (см. раздел Особые указания). Анти гипертензивный эффект от терапии олмесартаном может быть усилен при комбинированном применении с другими гипотензивными средствами. Нестероидные противовоспалительные препараты (НПВП), включая ацетилсалициловую кислоту в дозах более 3 г/сут, а также ингибиторы циклооксигеназы-2 (ЦОГ-2), и антагонисты рецепторов ангиотензина II могут действовать синергично, уменьшая гломерулярную фильтрацию. При одновременном применении НПВП и антагонистов рецепторов ангиотензина II может возникнуть риск развития острой почечной недостаточности, поэтому рекомендуется контроль функции почек в начале лечения, а также регулярный прием достаточного количества жидкости. Вместе с тем, одновременное лечение может уменьшить анти гипертензивное действие антагонистов рецепторов ангиотензина II, приводя к частичной потере их терапевтической эффективности. При одновременном применении с антацидами (магния и алюминия гидроксид) возможно умеренное снижение биодоступности олмесартана. Имеются сообщения об обратимом повышении концентрации лития в сыворотке крови и проявлении токсичности во время одновременного применения препаратов лития с ингибиторами ангиотензин-превращающего фермента (АПФ) и с антагонистами рецепторов ангиотензина II, поэтому применение олмесартана медоксомила в комбинации с препаратами лития не рекомендуется (см. раздел Особые указания). В случае необходимости применения соответствующей комбинированной терапии рекомендуется регулярный контроль уровня лития в сыворотке крови. Фармакологическое действие и фармакокинетика Кардосал® плюс - это комбинированный препарат, в состав которого входят антагонист рецепторов ангиотензина II (олмесартана медоксомил) и тиазидный диуретик (гидрохлоротиазид). Сочетание двух действующих веществ обладает комбинированным антигипергензивным действием, вследствие чего АД снижается в большей степени, чем при приеме каждого из них в отдельности. При приеме препарата один раз в сутки достигается эффективное и равномерное снижение АД в течение 24 ч. Олмесартана медоксомил является специфическим антагонистом рецепторов ангиотензина II (типа AT1). Ангиотензин II является первичным вазоактивным компонентом ренин-ангиотензин-альдостероновой системы (РААС) и играет значимую роль в патофизиологии артериальной гипертензии посредством влияния на AT1-рецепторы. Предполагается, что олмесартана медоксомил блокирует все эффекты ангиотензина П, опосредованные АТ1-рецепторами независимо от источника и пути синтеза ангиотензина II. При артериальной гипертензии олмесартана медоксомил вызывает дозозависимое продолжительное снижение АД. Нет данных о развитии артериальной гипотензии после приема первой дозы препарата и о развитии синдрома «отмены» (резкое повышение АД после отмены препарата). Прием олмесартана медоксомила один раз в сутки обеспечивает эффективное и мягкое снижение АД в течение 24 ч. Гипотензивное действие олмесартана медоксомила наступает, как правило, уже через 2 нед, а максимальный эффект развивается приблизительно через 8 нед. после начала терапии. Гидрохлоротиазид - тиазидный диуретик - нарушает реабсорбцию ионов натрия, хлора и воды в почечных канальцах. Увеличивает выведение ионов калия, магния, гидрокарбонатов, задерживает в организме ионы кальция. Диуретический эффект наступает через 2 ч после приема гидрохлоротиазида внутрь, достигает максимума через 4 ч и продолжается до 12 ч. Способствует снижению повышенного АД. При сочетанном приеме олмесартана медоксомила и гидрохлоротиазида происходит уменьшение потерь ионов калия, вызванных действием диуретика. Результатом комбинированной терапии олмесартана медоксомилом и гидрохлоротиазидом является потенцирование гипотензивного эффекта, который зависит от дозы каждого компонента препарата. Комбинированная терапия хорошо переносится пациентами. При длительном лечении эффективность комбинированной терапии (олмесартана медоксомил/гидрохлоротиазид) сохраняется, развития синдрома «отмены» не наблюдается. Фармакокинетика Абсорбция и распределение Олмесартана медоксомил является пролекарством. Он быстро превращается в фармакологически активный метаболит олмесартан под действием ферментов в слизистой оболочке кишечника и в периферической крови во время абсорбции из ЖКТ и циркулирует в крови в виде метаболита (олмесартан). Биодоступность олмесартана в среднем составляет 25.6 %. Cmax олмесартана в плазме крови в среднем достигается через 2 ч после приема внутрь и возрастает приблизительно линейно с увеличением однократной дозы до 80 мг. Прием пищи не оказывает значительного влияния на биодоступность олмесартана медоксомила, поэтому олмесартана медоксомил можно принимать независимо от приема пищи. Клинически значимых различий в фармакокинетических показателях олмесаргана медоксомила в зависимости от пола не выявлено. Олмесарган обладает высокой степенью связывания с белками плазмы крови (99.7%). При одновременном применении олмесартана медоксомила с другими лекарственными средствами, характеризующимися высокой степенью связывания с белками плазмы крови, не происходит значительных изменений указанной величины (подтверждением тому служит отсутствие клинически значимого взаимодействия между олмесартаном медоксомилом и варфарином). Связь олмесартана с клетками крови незначительна. После приема внутрь олмесартана медоксомила в комбинации с гидрохлороти азидом среднее время достижения Cmax гидрохлоротиазида составляет 1.5-2 ч. Гидрохлоротиазид связывается с белками плазмы крови на 68%. Системная биодоступность гидрохлоротиазида при одновременном применении с олмесартаном медоксомилом уменьшается примерно на 20%, но это небольшое уменьшение в клиническом отношении не является значимым. Одновременное назначение гидрохлоротиазида, со своей стороны, не оказывает существенного влияния на кинетику олмесартана медоксомила. В контролируемых клинических исследованиях был выявлен выраженный антигилертензивный эффект данной комбинации, который превышал эффект каждого из компонентов в отдельности, а также эффект плацебо. Метаболизм и выведение Общий плазменный клиренс олмесартана обычно составляет 1.3 л/ч (коэффициент вариации - 19 %) и является относительно низким по сравнению с печеночным кровотоком (примерно 90 л/ч). Почечное выведение олмесартана составляет приблизительно 40 %, с желчью через кишечник — около 60%; внепеченочная циркуляция — минимальна. Поскольку большая часть олмесартана медоксомила метаболизируется в печени, то его применение у пациентов с обструкцией желчевыводящих путей противопоказано. Период полувыведения олмесартана составляет 10-15 ч. Устойчивый эффект от терапии достигается в течение первых 14 дней ежедневного приема олмесартана медоксомила. Почечный клиренс составляет приблизительно 0.5-0.7 л/ч и не является дозозависимым. Гидрохлоротиазид в организме не метаболизируется и почти полностью в неизмененном виде выводится почками. После приема внутрь около 60 % принятой дозы гидрохлоротиазида в неизмененном виде выводится в течение 48 ч. Почечный клиренс гидрохлоротиазида составляет около 250-300 мл/мин; T1/2 конечной фазы составляет 10-15 ч. Фармакокннетнка у различных категории пациентов У пациентов в возрасте 65-75 лет с артериальной шпертензией площадь под кривой «концентрация-время» (AUC) для олмесартана в стадии насыщения увеличивается по сравнению с группой пациентов моложе 65 лет приблизительно на 35%, у пациентов старше 75 лет - примерно на 44%. Имеющиеся данные позволяют сделать вывод о том, что системный клиренс гидрохлоротиазида как у здоровых пожилых добровольцев, так и у пожилых пациентов с артериальной гипертензией снижен по сравнению с добровольцами более молодого возраста. У пациентов с нарушением функции почек (КК = 30-60 мл/мин.) AUC для олмесартана в стадии насыщения увеличивается приблизительно на 62, 82 и 179% в случае легкого, умеренного и тяжелого нарушения функции почек, соответственно, по сравнению со здоровыми добровольцами. Для данной категории пациентов возможно увеличение T1/2 гидрохлоротиазида. пациентов с нарушением функции печени легкой и средней степеней тяжести после однократного приема внутрь значения AUC для олмесартана были на 6 и 65% выше, соответственно в сравнении со здоровыми добровольцами. Несвязанная фракция олмесартана через 2 ч после приема дозы препарата у здоровых добровольцев, у пациентов с легкой и умеренной степенями нарушения функции печени составляла 0.26; 0.34 и 0.41 % соответственно. Влияние нарушений функции печени на фармакокинетику гидрохлоротиазида незначительно. В отношении пациентов с тяжелым нарушением функции печени (более 9 баллов по шкале Чайлд-Пью) данные по фармакокинетике олмесартана медоксомила отсутствуют. Особые указания Симптоматическая артериальная гипотензия, особенно после приема первой дозы препарата, может встречаться у пациентов со сниженным объемом циркулирующей крови и/или сниженным уровнем натрия вследствие интенсивной терапии диуретиками, ограничения потребления соли с пищей при диетическом питании, а также вследствие диареи или рвоты. Соответствующие факторы следует устранить до начала применения препарата Кардосал 10.У пациентов, у которых сосудистый тонус и функция почек зависят в большой степени от активности ренин-ангиотензин-альдостероновой системы (например, у пациентов с тяжелой хронической сердечной недостаточностью или нарушением функции почек, включая стеноз почечных артерий), лечение другими лекарственными средствами, действующими на эту систему, связано с возможностью развития острой артериальной гипотензии, азотемии, олигурии или, в редких случаях, острой почечной недостаточности. Возможность сходного действия не может быть исключена при применении антагонистов рецепторов ангиотензина II. Имеется повышенный риск развития тяжелой артериальной гипотензии и почечной недостаточности в том случае, если пациент с двухсторонним стенозом почечных артерий или стенозом артерии единственной функционирующей почки получает терапию лекарственными средствами, влияющими на ренин-ангиотензин-альдостероновую систему. При применении препарата Кардосал 10 у пациентов с нарушением функции почек рекомендуется проводить периодический контроль уровня калия и креатинина в сыворотке крови. Опыт применения препарата Кардосал 10 у пациентов с недавно проведенной трансплантацией почки или у пациентов с последней стадией нарушения функции почек (например, КК менее 12 мл/мин) отсутствует. Как и в случае других антагонистов рецепторов ангиотензина II и ингибиторов АПФ, при лечении препаратом Кардосал 10 может развиваться гиперкалиемия, если пациент страдает нарушением функции почек и/или хронической сердечной недостаточностью (см. раздел Взаимодействие с другими лекарственными средствами). У пациентов этой группы риска рекомендуется контроль уровня калия в сыворотке крови. Как и в случае других антагонистов рецепторов ангиотензина И, не рекомендуется комбинация препаратов лития и препарата Кардосал 10 (см. раздел Взаимодействие с другими лекарственными средствами). Как и в случае других антагонистов рецепторов ангиотензина II, у пациентов негроидной расы, страдающих артериальной гипертензией, эффективность терапии препаратом Кардосал 10 несколько ниже, чем у пациентов других рас. Как в случае любого анти гипертензивного средства, чрезмерное снижение АД у пациентов с ишемической болезнью сердца или с цереброваскулярной недостаточностью может привести к инфаркту миокарда или инсульту. Влияние на способность управлять транспортными средствами: Влияние препарата Кардосал 10 на способность к вождению автотранспорта и управлению механизмами не изучалось, поэтому в период лечения препаратом Кардосал 10 следует соблюдать осторожность при вождении автотранспорта и занятиях потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций (возможны головокружение и слабость). Условия хранения и отпуска из аптек Условия хранения:Хранить при температуре не выше 300 С. Хранить в недоступном для детей месте! Отпуск из аптек: По рецепту Регистрационные данные Торговое название Кардосал 10 Международное непатентованное название:Олмесартана медоксомил. Форма выпуска:таблетки покрытые пленочной оболочкой. Состав:1 таблетка, покрытая пленочной оболочкой содержит:Ядро. Действующее вещество: олмесартана медоксомил - 10,00 мг:Вспомогательные вещества: целлюлоза микрокристаллическая, гипролоза (с низкой степенью замещения), лактозы моногидрат, гипролоза (вязкость 6-10 м. Па-с), магния стеарат. Оболочка: титана диоксид (Е 171), тальк, гипромеллоза (вязкость 5м. Пас). АТХ: Регистрация: Лекарственное средство ЛСР-010758/09 Фармгруппа: Антагонист рецепторов ангиотензина II в комбинации с диуретиком. Дата регистрации: 29.12.2009. Окончание регстрации: . Описание:белые, круглые, двояковыпуклые таблетки, покрытые пленочной оболочкой, с оттиском "03" на одной стороне, с едва уловимым специфическим запахом. Упаковка:Таблетки, покрытые пленочной оболочкой, 10 мг. По 14 таблеток в контурной ячейковой упаковке (блистере), изготовленной из ламинированной пленки (полиамид / алюминий / ПВХ) и фольги алюминиевой. По 1,2, 4 или 7 блистеров вместе с инструкцией по применению в картонной пачке. Срок годности:3 года. Не применять по истечении срока годности, указанного на упаковке. Владелец рег.удостоверения:Берлин-Хеми/Менарини Фарма, ГмбХ Производитель:DAIICHI SANKYO EUROPE, GmbH. Представительство. Информация предоставлена: Компанией ГЭОТАР - http://www.lsgeotar.ru/

Модель:
RUR 25
Показания Язвенная болезнь желудка и двенадцатиперстной кишки: - Рефлюкс-эзофагит: - Эрозивно-язвенные поражения желудка и двенадцатиперстной кишки, связанные с приемом НПВП, стрессовые язвы: - Эрозивно-язвенные поражения желудка и двенадцатиперстной кишки, ассоциированные с Helicobacter pylori (в составе комплексной терапии): - Синдром Золлингера - Эллисона. Противопоказания Противопоказания Повышенная чувствительность к препарату, детский возраст, беременность, период лактации. С осторожностью: Почечная и/или печеночная недостаточность. Беременность Противопоказано. Применение и дозы Внутрь, запивая небольшим количеством воды (содержимое капсулы нельзя разжевывать). Язвенная болезнь двенадцатиперстной кишки в фазе обострения - по 1 капсуле (20 мг) в сутки в течение 2-4 недель (в резистентных случаях до 2 капсулы в сутки). Язвенная болезнь желудка в фазе обострения и эрозивно-язвенный эзофагит - по 1-2 капсуле в сутки в течение 4 - 8 недель. Эрозивно-язвенные поражения ЖКТ, вызванные приемом НПВП - по 1 капсуле в сутки в течение 4-8 недель. Эрадикация Helicobacter pylori - по 1 капсуле 2 раза в сутки в течение 7 дней в сочетании с антибактериальными средствами. Противорецидивное лечение язвенной болезни желудка и 12-перстной кишки - по 1 капсуле в сутки. Противорецидивное лечение рефлюкс-эзофагита - 1 капсула в сутки в течение длительного времени (до 6 месяцев). Синдром Золингера - Эллисона - доза подбирается индивидуально в зависимости от исходного уровня желудочной секреции, обычно начиная с 60 мг в сутки. При необходимости дозу увеличивают до 80 - 120 мг в сутки, в этом случае ее делят на два приема. Побочные эффекты и передозировка Побочные эффекты: В редких случаях могут возникать следующие, обычно обратимые, побочные явления: Со стороны органов пищеварения: диарея или запор, тошнота, рвота, метеоризм, боль в животе, сухость во рту, нарушения вкуса, стоматит, транзиторное повышение уровня "печеночных ферментов в плазме: у больных с предшествующим тяжелым заболеванием печени - гепатит (в т.ч. с желтухой), нарушение функции печени. Со стороны нервной системы: головная боль, головокружение, возбуждение, сонливость, бессонница, парестезии, депрессия, галлюцинации: у больных с тяжелыми сопутствующими соматическими заболеваниями, больных с предшествующим тяжелым заболеванием печени - энцефалопатия. Со стороны опорно-двигательного аппарата: мышечная слабость, миалгия, артралгия. Со стороны системы кроветворения: лейкопения, тромбоцитопения, в отдельных случаях - агранулоцитоз, панцитопения. Со стороны кожных покровов: зуд: редко, в отдельных случаях - фотосенсибилизация, мультиформная эритема, алопеция. Аллергические реакции: крапивница, ангионевротический отек, бронхоспазм, интерстициальный нефрит и анафилактический шок. Прочие: нарушения зрения, периферические отеки, усиление потоотделения, лихорадка, гинекомастия: редко - образование желудочных грандулярных кист во время длительного лечения (следствие ингибирования секреции соляной.кислоты, носит доброкачественный обратимый характер). Передозировка: Симптомами передозировки являются нарушение зрения, сонливость, возбуждение, спутанность сознания, головная боль, повышение потоотделения, сухость во рту, тошнота, аритмия. Специфического антидота не существует. Лечение симптоматическое. Гемодиализ недостаточно эффективен. Взаимодействие с другими ЛС: Длительное применение омепразола в дозе 20 мг 1 раз в сутки в комбинации с кофеином, теофиллином, пироксикамом, диклофенаком, напроксеном, метопрололом, пропранололом, этанолом, циклоспорином, лидокаином, хинидином и эстрадиолом не приводило к изменению их концентрации в плазме. Не отмечено взаимодействия с одновременно принимаемыми антацидами. Изменяет биодоступность любого препарата, всасывание которого зависит от значения pH (например, солей железа). Фармакологическое действие и фармакокинетика Омепразол ингибирует фермент Н+/К-АТФ-азу ("протонный насос") в париетальных клетках желудка и блокирует тем самым заключительную стадию синтеза соляной кислоты. Это приводит к снижению уровня базальной и стимулированной секреции, независимо от природы раздражителя. После однократного приема препарата внутрь действие омепразола наступает в течение первого часа и продолжается в течение 24 часов, максимум эффекта достигается через 2 часа. У больных с язвенной болезнью двенадцатиперстной кишки прием 20 мг омепразола поддерживает внутрижелудочный pH 3,0 в течение 17 часов. После прекращения приема препарата секреторная активность полностью восстанавливается после 3-5 суток. Фармакокинетика: Омепразол быстро абсорбируется из ЖКТ, пик концентрации в плазме через 0,5-1 час. Биодоступность составляет 30-40 %. Связывание с белками плазмы - около 90 %. Омепразол практически полностью метаболизируется в печени. Период полувыведения - 0,5-1 час. Выводится в основном почками в виде метаболитов. При ХПН выведение снижается пропорционально снижению клиренса креатинина. У пожилых пациентов выведение уменьшается, биодоступность возрастает. При печеночной недостаточности биодоступность - 100 %, период полувыведения - 3 часа. Особые указания Перед началом терапии необходимо исключить наличие злокачественного процесса (особенно при язве желудка), т.к. лечение, маскируя симптоматику, может отсрочить постановку правильного диагноза. Прием одновременно с пищей не влияет на его эффективность. При возникновении трудности с проглатыванием целой капсулы, можно проглотить ее содержимое после вскрытия или рассасывание капсулы, а также можно смешать содержимое капсулы со слегка подкисленной жидкостью (соком, йогуртом) и использовать полученную суспензию в течение 30 мин. У больных с тяжелой печеночной недостаточностью суточная доза не должна превышать 20 мг. Влияние на способность управлять транспортными средствами: Условия хранения и отпуска из аптек Условия хранения:Список Б. Хранить в сухом, защищенном от света, недоступном для детей месте, при температуре не выше 25 °С. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Омепразол Международное непатентованное название:Омепразол. Форма выпуска:капсулы. Состав:Каждая капсула содержит омепразола 20 мг (в пеллетах). Состав капсулы: Пеллеты омепразола (омепразол, метакриловая кислота и этилакрилат сополимер (акриловое покрытие L30D), кальция карбонат, калия гидрофосфат (двузамещенный калия фосфат),гидрооксипропилметилцеллюлоза (гипромеллоза), маннитол, сахарные пеллеты (сахароза), сахарный сироп (сахароза), макрогол - 6000 (полиэтиленгликоль 6000), повидон К-30 (поливинилпирролидон К-30), натрия гидроксид, натрия лаурилсульфат, тальк, титана диоксид, полисорбат-80 (твин 80) Капсула твердая желатиновая: (желатин, титана диоксид Е171, краситель солнечный закат желтый Е110 (желтый закат FCF-FD&:C желтый 6 Е110), краситель хинолиновый желтый Е104 (хинолин желтый Е104), вода). АТХ: Регистрация: Лекарственное средство Р N002333/01 Фармгруппа: Протонного насоса ингибитор. Дата регистрации: 15.07.2008. Окончание регстрации: . Описание:Твердые желатиновые капсулы №2 с корпусом и крышкой желтого цвета. Содержимое капсул - белые или почти белые сферические пеллеты. Упаковка:Капсулы по 20 мг. По 7, 10 капсул в контурной ячейковой упаковке: по 2, 3 или 4 контурные ячейковые упаковки вместе с инструкцией по применению в пачке из картона. Срок годности:2 года. Не применять по истечении срока годности указанного на упаковке. Владелец рег.удостоверения:ПРОИЗВОДСТВО МЕДИКАМЕНТОВ, ООО Производитель:ПРОИЗВОДСТВО МЕДИКАМЕНТОВ, ООО. Представительство

Модель:
RUR 451
Показания Применяют для лечения желудочно-кишечных симптомов, связанных с замедленной моторикой желудка и функциональной неязвенной диспепсией (хроническим гастритом), таких как: вздутие живота, быстрое насыщение, чувство переполнения в желудке после приема пищи, боль или дискомфорт в эпигастральной области, анорексия, изжога, тошнота и рвота. Противопоказания Противопоказания - Повышенная чувствительность к итоприду или любому вспомогательному компоненту препарата: - пациенты с желудочно-кишечным кровотечением, механической обструкцией или перфорацией: - детский возраст (до 16 лет): - беременность и период лактации. С осторожностью: Вследствие усиления итопридом действия ацетилхолина, следует назначать с осторожностью из-за возможного развития холинэргических побочных реакций у категории пациентов, для которых их появление может усугубить течение основного заболевания. Итоприд следует назначать с осторожностью пациентам пожилого возраста в связи с частым снижением функции печени и почек, наличием сопутствующих заболеваний или другого лечения. Беременность Беременность Нет достаточных данных применения итоприда гидрохлорида беременными. Применение во время беременности возможно только в случае, когда отсутствует альтернативная терапия, а потенциальная польза для матери превышает потенциальный риск для плода. Период грудного вскармливания Существует потенциальный риск развития побочных реакций у грудного ребенка, также имеются данные о выделении итоприда с молоком у крыс. При необходимости приема в период лактации грудное вскармливание необходимо прекратить. Применение и дозы Обычно взрослым назначают внутрь по 1 таблетке препарата Ганатон 50 мг 3 раза в сутки до еды. Рекомендуемая суточная доза составляет 150 мг. Указанная доза может быть снижена с учетом возраста и симптомов больного. В клинических исследованиях продолжительность лечения препаратом Ганатон была до 8 недель. Побочные эффекты и передозировка Побочные эффекты: Со стороны крови и лимфатической системы: лейкопения, тромбоцитопения. Аллергические реакции: гиперемия кожи, кожный зуд, сыпь, анафилаксия. Эндокринные нарушения: повышение уровня пролактина, гинекомастия. Со стороны нервной системы: головокружение, головная боль, тремор. Со стороны ЖКТ: диарея, запор, боль в животе, повышенное слюноотделение, тошнота, желтуха. Изменения лабораторных показателей: повышение активности аспартатаминотрансферазы (ACT), аланинаминотрансферазы (АЛТ), гамма-глутамилтранспептидазы, щелочной фосфатазы и уровня билирубина. Передозировка: Случаи передозировки у человека не описаны. При передозировке показаны промывание желудка и симптоматическая терапия. Взаимодействие с другими ЛС: Метаболическое взаимодействие вряд ли возможно, так как итоприд метаболизируется под действием флавиновой монооксигеназы, а не CYP450. При одновременном применении варфарина, диазепама, диклофенака натрия, тиклопидина гидрохлорида, нифедипина и никардипина гидрохлорида изменений связывания с белками не наблюдали. Итоприд усиливает моторику желудка, поэтому он может повлиять на всасывание других препаратов, которые назначают внутрь. Особую осторожность следует соблюдать при применении препаратов с низким терапевтическим индексом, а также форм с замедленным высвобождением активного вещества или препаратов с кишечно-растворимой оболочкой. Противоязвенные средства, такие как циметидин, ранитидин, тепренон и цетраксат, не влияют на прокинетическое действие итоприда. Антихолинергические средства могут ослабить эффект итоприда. Фармакологическое действие и фармакокинетика Итоприда гидрохлорид усиливает моторику ЖКТ за счет антагонизма D2-допаминовых рецепторов и ингибирования ацетилхолинэстеразы. Итоприд активирует высвобождение ацетилхолина и подавляет его разрушение. Итоприда гидрохлорид дает также противорвотный эффект за счет взаимодействия с D2-рецепторами, расположенными в триггерной зоне. Итоприд вызывал дозозависимое подавление рвоты, вызванной апоморфином. Итоприда гидрохлорид активирует пропульсивную моторику желудка за счет антагонизма D2-рецепторов и дозозависимого ингибирования активности ацетилхолинэстеразы. Итоприда гидрохлорид оказывает специфическое действие на верхний отдел ЖКТ, ускоряет транзит по желудку и улучшает его опорожнение. Итоприда гидрохлорид не влияет на сывороточные уровни гастрина. Фармакокинетика: Всасывание Итоприда гидрохлорид быстро и практически полностью всасывается в ЖКТ. Относительная биодоступность его составляет 60%, что связано с метаболизмом при первом прохождении через печень. Пища не оказывает влияния на биодоступность. Максимальная концентрация в плазме (Сmах) 0,28 мкг/мл достигается через 0,5-0,75 ч после приема 50 мг итоприда гидрохлорида. При повторном приеме итоприда гидрохлорида внутрь в дозе 50-200 мг три раза в сутки в течение 7 дней фармакокинетика препарата и его метаболитов была линейной, а кумуляция оказалась минимальной. Распределение Итоприда гидрохлорид на 96% связывается с белками плазмы, в основном с альбумином. Связывание с альфа 1-кислым гликопротеином составляет менее 15% от общего связывания. Итоприд активно распределяется в ткани (объем распределения 6,1 л/кг) и обнаруживается в высоких концентрациях в почках, тонком кишечнике, печени, надпочечниках и желудке. Проникновение в головной и спинной мозг минимальное. Итоприд проникает в грудное молоко. Метаболизм Итоприд подвергается активной биотрансформации в печени у человека. Идентифицированы 3 метаболита, только один из которых проявляет небольшую активность, которая не имеет фармакологического значения (примерно 2-3% от таковой итоприда). Первичным метаболитом у человека является N-оксид, который образуется в результате окисления четвертичной амино-N-диметильной группы. Итоприд метаболизируется под действием флавинзависимой монооксигеназы (FMО3). Количество и эффективность изоферментов FMO у человека может отличаться в зависимости от генетического полиморфизма, который в редких случаях приводит к развитию аутосомно-рецессивного состояния, известного под названием триметиламинурии (синдром “запаха рыбы”). У больных с триметиламинурией период полуэлиминации итоприда увеличивается. По данным фармакокинетических исследований in vivo, итоприд не оказывает ингибирующего или индуцирующего действия на CYP2C19 и CYP2E1. Терапия итопридом не влияет на CYP или активность уридиндифосфатглюкуронизилтрансферазы. Выведение Итоприда гидрохлорид и его метаболиты выводятся в основном с мочой. Почечная экскреция итоприда и его N-оксида после однократного приема препарата внутрь в терапевтических дозах у здоровых людей составляла 3,7 и 75,4% соответственно. Терминальный период полуэлиминации итоприда гидрохлорида равняется около 6 ч. Особые указания Итоприд усиливает действие ацетилхолина и может вызвать холинэргические побочные реакции. Влияние на способность управлять транспортными средствами: Условия хранения и отпуска из аптек Условия хранения:При температуре ниже 25 °С, в сухом, защищенном от света месте. Препарат следует хранить в местах, недоступных для детей. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Ганатон Международное непатентованное название:Итоприд. Форма выпуска:таблетки, покрытые оболочкой. Состав:Активное вещество: итоприда гидрохлорид 50 мг: вспомогательные компоненты (мг в 1 таблетке): лактоза 34,975 (включая избыток вследствие потери в массе при производстве 2,93%), крахмал кукурузный 15,0, кармеллоза 20,0, кислота кремневая безводная 4,0, магния стеарат 1,0, гипромеллоза 4,4, макрогол-6000 0,4, титана диоксид 0,2, воск карнауба 0,025. АТХ: Регистрация: Лекарственное средство ЛС-002513 Фармгруппа: Моторики ЖКТ стимулятор - ацетилхолина выброса стимулятор. Дата регистрации: 09.09.2011 / 18.08.2016. Окончание регстрации: . Описание:Белые круглые таблетки, покрытые пленочной оболочкой, с риской на одной стороне и гравировкой "НС 803" на другой. Упаковка:Таблетки, покрытые оболочкой, 50 мг. По 7, 10 или 14 таблеток в блистер из ПВХ/АL-фольги. 1, 2, 3, 4 или 5 блистеров с инструкцией по применению в картонной пачке. Срок годности:5 лет. Не применять после истечения срока годности, указанного на упаковке. Владелец рег.удостоверения:ЭББОТТ ЛЭБОРАТОРИЗ, ООО Производитель:ABBOTT JAPAN, Co. Ltd. Представительство:ЭББОТТ ЛЭБОРАТОРИЗ ООО
Модель:
RUR 774
Показания заместительная терапия тестостероном при первичном или вторичном гипогонадизме у мужчин, когда дефицит тестостерона подтверждается клиническими симптомами и лабораторными тестами; позднее созревание; импотенция, вызванная дефицитом тестостерона; посткастрационный синдром; расстройства сперматогенеза. Противопоказания Противопоказания гиперчувствительность к действующим веществам (тестостерону пропионату, тестостерону фенилпропионату, тестостерону изокапроату и тестостерону деканоату) и/или к любому вспомогательному веществу препарата; аллергические реакции на арахис или сою; рак предстательной железы (диагностированный или подозрение на него); рак грудной железы (диагностированный или подозрение на него); возраст до 18 лет (в связи с отсутствием данных по эффективности и безопасности применение тестостерона в данной возрастной группе). С осторожностью: артериальная гипертензия, тромбофилические состояния, тяжелая степень печеночной, хронической почечной и сердечной недостаточности, ИБС (со склонностью к отекам); сахарный диабет, доброкачественная гипертрофия предстательной железы, эпилепсия, мигрень; синдром апноэ в анамнезе, а также такие факторы риска, как ожирение и хронические заболевания легких; возрасте старше 65 лет. Беременность Препарат Омнадрен® 250 не показан для применения у женщин, в связи с чем, его применение в период беременности и грудного вскармливания противопоказано. Применение тестостерона в период беременности может привести к вирилизации плода женского пола. Применение и дозы Препарат вводят в/м глубоко в ягодичную мышцу. Режим дозирования препарата зависит, как правило, от индивидуальной реакции пациента на терапию. Обычно вводят по 1 мл раствора 1 раз (1 инъекция) в 3 недели. Снижение прозрачности маслянистого раствора или появление "иголочек" не означает, что лекарственный препарат не годен. При нагревании ампулы в теплой воде - раствор становится прозрачным. Имеющиеся ограниченные данные не указывают на необходимость коррекции дозы препарата у пациентов пожилого возраста (старше 65 лет). Применение препарата не рекомендуется у детей и подростков в возрасте до 18 лет в связи с отсутствием клинических данных по эффективности и безопасности в данной возрастной группе. Побочные эффекты и передозировка Побочные эффекты:Частота нежелательных реакций была оценена в соответствии с классификацией систем и органов MedDRA следующим образом: очень часто ( 1/10), часто ( 1/100, < 1/10), нечасто ( 1/1000, < 1/100), редко ( 1/10 000, < 1/1000), очень редко (< 1/10 000), неизвестно (частота не может быть определена на основе имеющихся данных). Со стороны половых органов и молочной железы: частота неизвестна - гинекомастия (феминизация), приапизм, олигозооспермия, доброкачественная гиперплазия предстательной железы. Со стороны костно-мышечной системы: частота неизвестна - миалгия. Со стороны кожи и подкожных тканей: частота неизвестна - кожный зуд, акне, алопеция и себорея. Со стороны обмена веществ и питания: частота неизвестна - задержка соли и воды. Со стороны желудочно-кишечного тракта: частота неизвестна - тошнота. Со стороны печени и желчевыводящих путей: частота неизвестна - нарушение функции печени. Со стороны системы кроветворения: частота неизвестна - полицитемия. Со стороны сердечно-сосудистой системы: частота неизвестна - артериальная гипертензия. Нарушения психики: частота неизвестна - депрессия, изменение настроения, изменение либидо. Доброкачественные, злокачественные и не уточненные новообразования (включая кисты и полипы): частота неизвестна - рак предстательной железы. Лабораторные и инструментальные данные: часто - увеличение содержания гемоглобина и гематокрита, количества эритроцитов; частота неизвестна - снижение концентрации ЛПВП, ЛПНП и триглицеридов, увеличение концентрации ПСА. Общие расстройства и нарушения в месте введения: частота неизвестна - воспаление и боль в месте инъекции. Информирование о подозреваемых побочных реакциях Важно сообщать о подозреваемых побочных реакциях после применения лекарственного препарата. Это позволяет осуществлять постоянный мониторинг баланса пользы и риска, связанных с лекарственным препаратом. Медицинские работники должны сообщать о любых подозрительных побочных явлениях. Передозировка: Острая токсичность тестостерона низкая. Никаких специальных терапевтических мер при передозировке не требуется, за исключением отмены препарата или снижение его дозы. Взаимодействие с другими ЛС: Пероральные антикоагулянты При совместном применении с непрямыми пероральными антикоагулянтами производными кумарина тестостерон может увеличивать их действие, в связи с чем необходим частый мониторинг протромбинового времени и, при необходимости, снижение дозы антикоагулянтов. Инсулин и другие гипогликемические препараты Андрогены могут повышать толерантность к глюкозе и потребность пациента в инсулине или других гипогликемических препаратах, поэтому пациенты с сахарным диабетом должны периодически проводить контроль гликемии на фоне терапии тестостероном. АКТГ, ГКС Сопутствующее введение АКТГ или ГКС может вызвать усиление периферических отеков, особенно у пациентов с заболеваниями печени, сердца или склонностью к образованию отеков. Оксифенбутазон Андрогены увеличивают концентрацию оксифенбутазона при одновременном применении. Индукторы микросомальных ферментов печени Рифампицин, барбитураты, карбамазепин, салицилаты, фенитоин, примидон при одновременном применении могут снижать концентрацию тестостерона в плазме крови, что может потребовать коррекции его дозы. Ингибиторы микросомальных ферментов печени При одновременном применении могут повышать концентрацию тестостерона в плазме крови, что также может потребовать коррекцию его дозы. Андрогены могут снижать концентрацию тироксинсвязывающего глобулина, что в свою очередь приводит к снижению концентрации трийодтиронина (Т4); концентрация же свободного тироксина (Т3) не изменяется. Клинических проявлений дисфункции щитовидной железы не выявлено. Фармакологическое действие и фармакокинетика Омнадрен® 250 представляет собой смесь эфиров тестостерона, аналогичного природному мужскому гормону тестостерону, в масляном растворе. Тестостерон вырабатывается в мужских половых железах, в клетках Лейдига и является основным эндогенным гормоном необходимым для нормального роста и развития мужских половых органов и вторичных половых признаков у мужчин (рост и созревание предстательной железы, семенных пузырьков, полового члена и мошонки, развитие и распределение волос по мужскому типу, расширение гортани, изменение тембра голоса, изменения мускулатуры тела и распределение жира). У взрослых мужчин тестостерон необходим для функционирования яичек и придатка яичка, предстательной железы и семенных пузырьков, а также для поддержания либидо, хорошего самочувствия, эректильной функции. Лечение мужчин с гипогонадизмом препаратом Омнадрен® 250 приводит к клинически значимому повышению концентраций тестостерона, дигидротестостерона, эстрадиола и андростендиона в плазме, а также к снижению концентрации глобулина, связывающего половые гормоны (ГСПГ); концентрации ЛГ и ФСГ восстанавливаются до нормального значения. Лечение препаратом Омнадрен® 250 приводит к уменьшению симптомов дефицита тестостерона. Кроме того, увеличивается минеральная плотность костей и мышечная масса, у пациентов с ожирением происходит снижение массы тела. В процессе лечения нормализуются сексуальные функции, включая эректильную функцию и либидо. При применении препарата снижается концентрация в плазме крови ЛПВП, стимулируется выработка эритропоэтина в почках, повышается содержание гемоглобина и гематокрита, при этом не происходит клинически значимого изменения активности печеночных ферментов и ПСА. Препарат может вызвать увеличение размеров предстательной железы, при этом функциональных изменений не отмечается. У мужчин с гипогонадизмом и сопутствующим сахарным диабетом применение андрогенов улучшает чувствительность к инсулину и/или снижает концентрацию глюкозы в плазме крови. У женщин тестостерон оказывает антагонистическое действие на эстрогены, подавляет гипофизарные гонадотропины, подавляет лактацию. Фармакокинетика: Всасывание Препарат содержит 4 разных эфира тестостерона, каждый из которых имеет разную продолжительность действия. Эти эфиры гидролизуются до тестостерона, как только попадают в общий кровоток. Cmax тестостерона в плазме крови составляет 70 нмоль/л и достигается в течение 24-48 ч после инъекции препарата и возвращается к исходному значению через 21 день после введения препарата Омнадрен® 250. Тестостерона пропионат после инъекции сразу проявляет свое действие, продолжающееся на протяжении 24 ч. Тестостерона изокапроат и тестостерона фенилпропионат начинают оказывать свое действие через 24 ч, которое сохраняется приблизительно 2 недели. Тестостерона деканоат начинает действовать в период, когда прекращается действие тестостерона изокапроата и тестостерона фенилпропионата, и продолжается до 2 недель. Распределение В плазме крови тестостерон приблизительно на 98% связывается со специфической фракцией глобулинов, связывающих тестостерон и эстрадиол. Метаболизм и выведение Тестостерон биотрансформируется в печени до производных 17-кетостероидов, которые после связывания с глюкуроновой или серной кислотой выводятся почками, приблизительно на 90%. В то же время 6% введенной дозы выводится через кишечник в несвязанной форме. Особые указания Препарат Омнадрен® 250 предназначен исключительно для в/м инъекций. В случае болезненной эрекции введение лекарственного препарата следует прекратить. Медицинское обследование Концентрацию тестостерона следует контролировать в начале введения и регулярно во время лечения. Врачи должны корректировать дозу индивидуально, чтобы обеспечить концентрацию тестостерона при нормальной функции гонад. Определение концентрации тестостерона должно быть проведено до начала терапии препаратом, а также 1 раз в 3 месяца в течение первого года терапии, далее - 1 раз в год необходимо проводить пальцевое ректальное исследование предстательной железы и определение концентрации ПСА с целью исключения доброкачественной гиперплазии предстательной железы и субклинического рака предстательной железы. У пациентов, получающих длительную терапию андрогенами, необходимо регулярно контролировать следующие лабораторные параметры: гемоглобин и гематокрит, тесты функции печени и липидный профиль. Новообразования У пациентов с раком грудной железы и метастазами в кости развивается гиперкальциемия либо спонтанно (на фоне злокачественного новообразования), либо на фоне терапии андрогенами/анаболическими стероидами. У таких пациентов рекомендуется регулярный контроль концентрации кальция в плазме крови. В случае выявления гиперкальциемии введение тестостерона следует прекратить и провести соответствующее лечение. Терапия тестостероном может быть продолжена только после восстановления нормальной концентрации кальция в плазме крови. Тяжелая степень печеночной, хронической почечной и сердечной недостаточности, ИБС Лечение тестостероном может вызывать задержку натрия и воды в организме. В случае развития у таких пациентов серьезных осложнений, характеризующихся периферическими отеками при наличии или отсутствии хронической сердечной недостаточности, требуется прекращение терапии тестостероном. Артериальная гипертензия Тестостерон может вызвать повышение АД, поэтому препарат Омнадрен® 250 следует применять с осторожностью у пациентов с артериальной гипертензией. Нарушение свертываемости крови Следует проявлять осторожность при применении тестостерона у пациентов с тромбофилией, поскольку анализ пострегистрационных исследований показал наличие случаев тромбоза у этих пациентов во время лечения тестостероном. Следует учитывать риск развития кровотечений при в/м введении тестостерона пациентам с врожденными или приобретенными нарушениями свертываемости крови. Пожилые пациенты У пожилых пациентов наблюдается повышенный риск развития гиперплазии или рака предстательной железы. Перед и во время лечения следует проверить состояние предстательной железы и контролировать концентрацию ПСА. Существует ограниченный опыт в области безопасности и эффективности применения препарата Омнадрен® 250 у пациентов старше 65 лет. В настоящее время нет консенсуса относительно соответствующих возрасту рекомендованных показателей уровня тестостерона. Однако следует учитывать, что физиологическая концентрация тестостерона в сыворотке плазмы крови уменьшается с возрастом. Репродуктивная функция Применение препарата Омнадрен® 250 для терапии мужчин, особенно в высоких дозах, может привести к снижению репродуктивной функции, включая олигоспермию. Другие меры предосторожности Применение препарата у пациентов с наличием аллергии на арахис или сою противопоказано. Применение препарата у пациентов с эпилепсией и мигренью должно проводиться под тщательным медицинским наблюдением, т.к. возможно ухудшение течения заболеваний на фоне терапии. У пациентов с апноэ в анамнезе и доброкачественной гипертрофией предстательной железы препарат применяют с осторожностью. В случае развития нежелательных реакций, связанных с тестостероном, терапию препаратом Омнадрен® 250 следует прекратить и возобновить ее с более низкой дозы препарата. Влияние на способность управлять транспортными средствами: Применение препарата Омнадрен® 250 не оказывает влияния на способность к управлению транспортными средствами и механизмами. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25°С. Хранить в недоступном для детей месте! Отпуск из аптек: По рецепту Регистрационные данные Торговое название Омнадрен® 250 Международное непатентованное название:Тестостерон. Форма выпуска:раствор для внутримышечного введения (масляный) в виде прозрачной, маслянистой жидкости светло-желтого цвета. Состав: 1 мл тестостерона пропионат 30 мг тестостерона фенилпропионат 60 мг тестостерона изокапронат 60 мг тестостерона деканоат 100 мг АТХ: Регистрация: Лекарственное средство Фармгруппа: андроген Информация предоставлена
Модель:
RUR 2109
Показания Взрослые- Артериальная гипертензия- Хроническая сердечная недостаточность (II-IV функциональный класс по классификации NYHA), у взрослых пациентов, получающих стандартную терапию одним или несколькими препаратами из следующих фармакотерапевтических групп: диуретиками, сердечными гликозидами, а также ингибиторами АПФ или бета- адреноблокаторами. Применение каждого из перечисленных препаратов не является обязательным- Для повышения выживаемости пациентов после перенесенного острого инфаркта миокарда, осложненного левожелудочковой недостаточностью и/или систолической дисфункцией левого желудочка, при наличии стабильных показателей гемодинамики. Дети и подростки- Артериальная гипертензия у детей и подростков от 6 до 18 лет. Противопоказания Противопоказания - Повышенная чувствительность к любому из компонентов препарата- беременность, период кормления грудью- тяжелые нарушения функции печени (более 9 баллов по шкале Чайлд-Пью), билиарный цирроз и холестаз- возраст до 6 лет - по показанию артериальная гипертензия, до 18 лет - по другим показаниям- одновременное использование антагонистов рецепторов ангиотензина II, включая Диован, или ингибиторов АПФ с алискиреном у пациентов с сахарным диабетом 2-го типа. С осторожностью: Если у Вас одно из перечисленных заболеваний перед приемом препарата обязательно проконсультируйтесь с врачом. Принимать с осторожностью при двустороннем стенозе почечных артерий, стенозе артерии единственной почки, первичном гиперальдостеронизме, при соблюдении диеты с ограничением потребления поваренной соли: при состояниях, сопровождающихся снижением объема циркулирующей крови (в том числе диарея, рвота): у пациентов с КК менее 10 мл/мин (нет клинических данных), у пациентов в возрасте от 6 до 18 лет и КК менее 30 мл/мин, в том числе находящихся на гемодиализе, с легкими и умеренными нарушениями функции печени билиарного и небилиарного генеза без явлений холестаза, хронической сердечной недостаточностью (ХСН) II-IV функционального класса (по NYHA), митральным или аортальным стенозом, гипертрофической обструктивной кардиомиопатией, а также у пациентов после трансплантации почки. С осторожностью осуществлять одновременное назначение антагонистов рецепторов ангиотензина II, включая Диован, с другими средствами, ингибирующими ренин-ангиотензин-альдостероновую систему (РААС), такими как ингибиторы АПФ или алискирен. Не рекомендуется применять препарат Диован одновременно с ингибиторами АПФ, поскольку данная комбинированная терапия не имеет преимуществ перед монотерапией валсартаном или ингибитором АПФ в отношении показателей общей смертности по любой причине. Беременность Как и любой другой препарат, оказывающий влияние на РААС, Диован не должен применяться у женщин, планирующих беременность. При назначении любого препарата, воздействующего на РААС, врачу следует проинформировать женщин детородного возраста о потенциальной опасности этих препаратов во время беременности. Как любой другой препарат, оказывающий непосредственное влияние на РААС, Диован не должен применяться при беременности. Учитывая механизм действия антагонистов рецепторов ангиотензина II, нельзя исключить риск для плода. Действие ингибиторов АПФ (препаратов, также оказывающих влияние на РААС) на плод, в случае их применения во втором и третьем триместре беременности, может приводить к его повреждению и гибели. По ретроспективным данным при применении ингибиторов АПФ в первом триместре беременности повышается риск рождения детей с врожденными дефектами. Имеются сообщения о самопроизвольных абортах, олигогидрамнионе и нарушениях функции почек у новорожденных, матери которых во время беременности по неосторожности принимали валсартан. Если беременность диагностирована в период лечения препаратом Диован, следует отменить лечение как можно быстрее. Неизвестно, выделяется ли валсартан с грудным молоком. Поэтому не следует применять препарат в период кормления грудью. Отсутствуют данные о влиянии препарата на фертильность человека. При исследовании на животных не наблюдалось эффектов воздействия валсартана на фертильность. Применение и дозы Таблетки принимать внутрь, не разжевывая, вне зависимости от приема пищи, запивая водой Взрослые Артериальная гипертензия Препарат может быть назначен в дозе 40 мг, 80 мг, 160 мг, 320 мг. Рекомендуемая начальная доза препарата Диован составляет 80 мг 1 раз в сутки, вне зависимости от расовой принадлежности, возраста и пола больного. Антигипертензивный эффект отмечается в первые 2 недели лечения: максимальный эффект развивается через 4 недели. Тем пациентам, у которых не удается достичь адекватного терапевтического ответа, суточная доза препарата Диован может быть постепенно увеличена до максимальной суточной дозы 320 мг или необходимо дополнительно применять диуретические средства. Хроническая сердечная недостаточность Рекомендуемая начальная доза препарата Диован составляет 40 мг 2 раза в сутки (1/2 таблетки 80 мг). Дозу препарата следует постепенно увеличить в течение как минимум 2 недель до 80 мг 2 раза в сутки, а при хорошей переносимости - до 160 мг 2 раза в сутки. Максимальная суточная доза составляет 320 мг в 2 приема. При этом может потребоваться снижение дозы одновременно принимаемых диуретиков. Для повышения выживаемости пациентов после перенесенного острого инфаркта миокарда Лечение следует начинать в течение 12 ч после перенесенного инфаркта миокарда. Начальная доза составляет 20 мг (1/2 таблетки 40 мг) 2 раза в сутки. Повышение дозы проводится методом титрования (40 мг, 80 мг, 160 мг 2 раза в сутки) в течение нескольких последующих недель, до достижения целевой дозы 160 мг 2 раза в сутки. Максимальная суточная доза составляет 320 мг в 2 приема. Как правило, рекомендуется увеличение дозы до 80 мг 2 раза в сутки к концу второй недели лечения. Достижение максимальной целевой дозы по 160 мг 2 раза в сутки рекомендуется к концу третьего месяца терапии препаратом Диован. Увеличение дозы зависит от переносимости препарата Диован в период титрования. В случае развития артериальной гипотензии, сопровождающейся клиническими проявлениями, или нарушений функции почек следует рассмотреть вопрос о снижения дозы. Оценка состояния пациентов, в период после перенесенного инфаркта миокарда, должна включать оценку функции почек. Дети и подростки Артериальная гипертензия Рекомендуемая начальная доза препарата Диован у детей и подростков от 6 до 18 лет составляет 40 мг (1/2 таблетки по 80 мг) при массе тела ребенка менее 35 кг и 80 мг при массе тела ребенка более 35 кг. Дозу рекомендовано корректировать с учетом снижения АД. Максимальные рекомендованные дозы отражены в таблице ниже. Применение более высоких доз не рекомендовано.ТАБЛИЦЪХроническая сердечная недостаточность перенесенный острый инфаркт миокарда. Диован не рекомендован для лечения хронической сердечной недостаточности и после перенесенного острого инфаркта миокарда у пациентов младше 18 лет. Пациенты в возрасте старше 65 летУ пожилых пациентов коррекции дозы препарата не требуется. Пациенты с нарушениями функции почекУ пациентов с нарушениями функции почек, коррекции дозы препарата не требуется. В настоящее время нет данных о применении препарата у пациентов с КК менее 10 мл/мин. Пациенты с нарушениями функции печени. Больным с легкими или умеренными нарушениями функции печени небилиарного генеза без явлений холестаза препарат следует применять с осторожностью, суточная доза не должна превышать 80 мг. Побочные эффекты и передозировка Побочные эффекты: У пациентов с артериальной гипертензией в контролируемых клинических исследованиях частота нежелательных явлений была сравнима с плацебо. Отсутствуют данные о зависимости частоты какого-либо из нежелательных явлений от дозы или продолжительности лечения, а также пола, возраста или расовой принадлежности. Профиль безопасности препарата Диован у пациентов с артериальной гипертензией в возрасте от 6 до 18 лет не отличается от профиля безопасности валсартана у взрослых пациентов. Ниже приведены нежелательные явления, которые наблюдались в ходе клинических исследований, а также при применении препарата в клинической практике. Для оценки частоты нежелательных явлений использованы следующие критерии: "очень часто" ( 1/10), "часто" ( 1/100, <:1/10) "нечасто" ( 1/1000,<:1/100), "редко" ( 1/10 000, <:1/1000), "очень редко" (<:1/10000), включая отдельные сообщения. В пределах каждой группы, выделенной по частоте встречаемости, нежелательные явления распределены в порядке уменьшения их важности. Для всех нежелательных явлений, выявленных в клинической практике и при анализе лабораторных показателей (частоту развития которых установить невозможно) использовалась градация "частота неизвестна". Пациенты с артериальной гипертензией Нарушения со стороны крови и лимфатической системы: частота неизвестна - снижение гемоглобина, гематокрита, нейтропения, тромбоцитопения. Нарушения со стороны иммунной системы: частота неизвестна - реакции повышенной чувствительности, включая сывороточную болезнь. Нарушения со стороны обмена веществ и питания: частота неизвестна - повышение содержания калия в сыворотке крови. Нарушения со стороны органа слуха и лабиринтные нарушения: нечасто - вертиго. Нарушения со стороны сосудов: частота неизвестна - васкулит. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: нечасто - кашель. Нарушения со стороны желудочно-кишечного тракта: нечасто - боли в животе. Нарушения со стороны печени и желчевыводящих путей: частота неизвестна - нарушение функции печени, включая повышение концентрации билирубина в плазме крови. Нарушения со стороны кожи и подкожных тканей: частота неизвестна - ангионевротический отек, буллезный дерматит, кожная сыпь, зуд. Нарушения со стороны скелетно- мышечной и соединительной ткани: частота неизвестна - миалгия. Нарушения со стороны почек и мочевыводящих путей: частота неизвестна - нарушения функции почек, повышение концентрации креатинина в сыворотке крови. Общие расстройства и нарушения в месте введения: нечасто - повышенная утомляемость. Также в ходе клинических исследований у пациентов с артериальной гипертензией наблюдались следующие нежелательные явления, причинно-следственная связь которых с приемом препарата не установлена: артралгия, астения, боль в спине, диарея, головокружение, бессонница, снижение либидо, тошнота, периферические отеки, фарингит, ринит, синусит, инфекции верхних дыхательных путей, вирусные инфекции. Пациенты, получающие препарат Диован после перенесенного острого инфаркта миокарда и /или при ХСН Нарушения со стороны крови и лимфатической системы: частота неизвестна - тромбоцитопения. Нарушения со стороны иммунной системы: частота неизвестна - реакции повышенной чувствительности, включая сывороточную болезнь. Нарушения со стороны обмена веществ и питания: нечасто - гиперкалиемия: частота неизвестна - повышение содержания калия в сыворотке крови. Нарушения со стороны нервной системы: часто - головокружение, постуральное головокружение: нечасто - обморок, головная боль. Нарушения со стороны органа слуха и лабиринтные расстройства: нечасто - вертиго. Нарушения со стороны сердца: нечасто - усиление симптомов хронической сердечной недостаточности. Нарушения со стороны сосудов: часто - выраженное снижение АД, ортостатическая гипотензия: частота неизвестна - васкулит. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения: нечасто - кашель. Нарушения со стороны желудочно-кишечного тракта: нечасто - тошнота, диарея. Нарушения со стороны печени и желчевыводящих путей: частота неизвестна - повышение активности "печеночных" ферментов. Нарушения со стороны кожи и подкожных тканей: нечасто - ангионевротический отек: частота неизвестна - буллезный дерматит, кожная сыпь, зуд. Нарушения со стороны скелетно-мышечной и соединительной ткани: редко - рабдомиолиз, частота неизвестна - миалгия. Нарушения со стороны почек и мочевыводящих путей: часто нарушение функции почек: нечасто - острая почечная недостаточность, повышение концентрации креатинина в сыворотке крови: частота неизвестна - повышение содержания азота мочевины в плазме крови. Общие расстройства и нарушения в месте введения: нечасто - астения, повышенная утомляемость. Также в ходе клинических исследований у пациентов после перенесенного острого инфаркта миокарда и/или при ХСН наблюдались следующие нежелательные явления, причинно-следственная связь которых с приемом препарата не установлена: артралгия, боли в животе, боль в спине, астения, бессонница, снижение либидо, нейтропения, периферические отеки, фарингит, ринит, синусит, инфекции верхних дыхательных путей, вирусные инфекции. Если любые из указанных в инструкции побочных эффектов усугубляются, или Вы заметили любые другие побочные эффекты не указанные в инструкции, сообщите об этом врачу. Передозировка: При передозировке препарата Диован основным проявлением является выраженное снижение АД, которое может привести к угнетению сознания, коллапсу и/или шоку. Лечение: симптоматическое, характер, которого зависит от времени, прошедшего с момента приема препарата, и от степени тяжести симптомов. При случайной передозировке следует вызвать рвоту (если препарат был принят недавно) или провести промывание желудка. В случае возникновения выраженного снижения АД в качестве терапии необходимо внутривенное введение 0,9% раствора натрия хлорида, больного следует уложить, приподняв ноги, на необходимый для терапии период времени, принять активные меры по поддержанию деятельности сердечно-сосудистой системы, включая регулярный контроль деятельности сердца и дыхательной системы, объема циркулирующей крови (ОЦК) и количества выделяемой мочи. Взаимодействие с другими ЛС: Установлено, что при монотерапии валсартаном отсутствуют клинически значимые взаимодействия со следующими лекарственными средствами: циметидином, варфарином, фуросемидом, дигоксином, атенололом, индометацином, гидрохлоротиазидом, амлодипином, глибенкламидом. Двойная блокада РААС при применении антагонистов рецепторов ангиотензина II, ингибиторов АПФ или алискирена Одновременное применение антагонистов рецепторов ангиотензина II, включая препарат Диован, с другими средствами, оказывающими влияние на РААС, связано с повышенной частотой развития артериальной гипотензии, гиперкалиемии и изменений функции почек по сравнению с монотерапией. Рекомендуется проводить мониторинг артериального давления, функции почек и содержания электролитов у пациентов, принимающих Диован и другие лекарственные средства, оказывающие влияние на РААС. Нестероидные противоспалительные препараты (НПВП) При применении валсартана одновременно с НПВП (включая селективные ингибиторы циклооксигеназы-2) возможно уменьшение его антигипертензивного действия. При применении ангиотензина II рецепторов антагонистов одновременно с НПВП возможно ухудшение функции почек и увеличение содержания калия в плазме крови. При необходимости одновременного применения валсартана и НПВП до начала лечения необходимо провести оценку функции почек и коррекцию нарушений водно-электролитного баланса. Белки-переносчики По результатам исследования in vitro на культурах печени валсартан является субстратом для белков-переносчиков ОАТР1В1 и MRP2. Одновременное назначение валсартана с ингибиторами белка-переносчика ОАТР1В1 (рифампицин, циклоспорин) и с ингибитором белка-переносчика MRP2 (ритонавир) может увеличить системную экспозицию валсартана (Сmах и AUC). Препараты лития При одновременном применении препаратов лития с ингибиторами АПФ и ангиотензина II рецепторов антагонистами отмечалось обратимое повышение содержания лития в сыворотке крови и усиление, в связи с этим, токсических проявлений, поэтому рекомендуется проводить контроль содержания лития в сыворотке крови. Одновременное применение калийсберегающих диуретиков (в т.ч. спиронолактона, триамтерена, амилорида), препаратов калия или солей, содержащих калий, а также других препаратов, способных увеличивать содержание калия (например, гепарин и т.д.), может привести к увеличению концентрации калия в сыворотке крови и у пациентов с сердечной недостаточностью к увеличению концентрации креатинина сыворотки крови. Если такое комбинированное лечение признано необходимым, следует соблюдать осторожность. У детей и подростков артериальная гипертензия часто связана с нарушением функции почек. Рекомендовано с осторожностью применять валсартан одновременно с другими препаратами, влияющими на ренин-ангиотензин-альдостероновую систему, у пациентов данной категории, т.к. это может привести к увеличению содержания калия в сыворотке крови. Следует проводить регулярный контроль функции почек и содержания калия в сыворотке крови у пациентов данной группы. Фармакологическое действие и фармакокинетика Валсартан - активный специфический антагонист рецепторов ангиотензина II, предназначенный для приема внутрь. Избирательно блокирует рецепторы подтипа АТ1, которые ответственны за эффекты ангиотензина II. Следствием блокады АТ1-рецепторов является повышение плазменной концентрации ангиотензина II, который может стимулировать незаблокированные АТ2-рецепторы. Валсартан не имеет сколько-нибудь выраженной агонистической активности в отношении АТ1-рецепторов. Сродство валсартана к рецепторам подтипа АТ1 примерно в 20 000 раз выше, чем к рецепторам подтипа АТ2. Валсартан не вступает во взаимодействие и не блокирует рецепторы других гормонов или ионные каналы, имеющие важное значение в регуляции функций сердечно-сосудистой системы. Вероятность возникновения кашля при применении валсартана очень низкая, что связано с отсутствием влияния на ангиотензинпревращающий фермент (АПФ), который отвечает за деградацию брадикинина. Сравнение валсартана с ингибитором АПФ демонстрирует, что частота развития сухого кашля достоверно (р <: 0,05) ниже у пациентов, принимающих препарат, чем у пациентов, принимающих ингибитор АПФ (2,6% против 7,9% соответственно). В группе пациентов, у которых ранее при лечении ингибитором АПФ развивался сухой кашель, при лечении валсартаном это нежелательное явление (НЯ) отмечается в 19,5% случаев, а при лечении тиазидным диуретиком - в 19,0% случаев, в то время как в группе пациентов, получавших лечение ингибитором АПФ, кашель наблюдается в 68,5% случаев (р <: 0,05). Применение при артериальной гипертензии у пациентов старше 18 лет При лечении валсартаном пациентов с артериальной гипертензией отмечается снижение артериального давления (АД), не сопровождающееся изменением частоты сердечных сокращений (ЧСС). После применения внутрь разовой дозы препарата у большинства пациентов начало антигипертензивного действия наблюдается в течение 2 ч, а максимальное снижение АД достигается в пределах 4-6 ч, сохраняющееся более 24 часов. При повторном применении препарата максимальное снижение АД, вне зависимости от принятой дозы, обычно достигается в пределах 2-4 недель, и поддерживается на достигнутом уровне в ходе длительной терапии. В случае одновременного применения препарата с гидрохлоротиазидом достигается достоверное дополнительное снижение АД. Резкое прекращение применения валсартана не сопровождается значительным повышением АД или другими НЯ. У пациентов с артериальной гипертензией, сахарным диабетом 2 типа и нефропатией, принимающих валсартан в дозе 160-320 мг, отмечается значительное снижение протеинурии (36-44%). Применение после острого инфаркта миокарда у пациентов старше 18 лет При применении препарата в течение 2-х лет у пациентов, которые начали принимать в период от 12 ч до 10 дней после перенесенного острого инфаркта миокарда (осложненного левожелудочковой недостаточностью и/или систолической дисфункцией левого желудочка), снижаются показатели общей смертности, сердечно-сосудистой смертности и увеличивается время до первой госпитализации по поводу обострения течения хронической сердечной недостаточности, повторного инфаркта миокарда, внезапной остановки сердца и инсульта (без летального исхода). Профиль безопасности валсартана у пациентов с острым инфарктом миокарда сходен с таковым при других состояниях. Хроническая сердечная недостаточность (ХСН) у пациентов старше 18 лет При применении валсартана (в средней суточной дозе 254 мг) в течение 2-х лет у пациентов с ХСН II (62%), III (36%) и IV (2%) функционального класса по классификации NYHA с фракцией выброса левого желудочка (ЛЖ) менее 40% и внутренним диастолическим диаметром ЛЖ более 2,9 см/м 2, получающих стандартную терапию, включая ингибиторы АПФ (93%), диуретики (86%), дигоксин (67%) и бета-адреноблокаторы (36%) отмечается достоверное снижение (на 27,5%) риска госпитализации по поводу обострения течения ХСН. У пациентов, не получавших ингибиторы АПФ, отмечается значительное снижение показателя общей смертности (на 33%), сердечно-сосудистой смертности и заболеваемости, связанной с ХСН (время до наступления первого сердечно-сосудистого события), которые оцениваются по следующим показателям: смерть, внезапная смерть с проведением реанимации, госпитализация по поводу обострения течения ХСН, внутривенное введение инотропных или сосудорасширяющих препаратов в течение 4 или более часов без госпитализации (на 44%). В группе пациентов, получающих ингибиторы АПФ (без бета-адреноблокаторов), на фоне лечения валсартаном не наблюдается снижения показателя общей смертности, однако уменьшаются показатели сердечно-сосудистой смертности и заболеваемости, связанной с ХСН на 18,3%. В целом применение валсартана приводит к уменьшению числа госпитализаций по поводу ХСН, замедлению прогрессирования ХСН, улучшению функционального класса ХСН по классификации NYHA, увеличению фракции выброса левого желудочка, а также уменьшению выраженности признаков и симптомов сердечной недостаточности и улучшению качества жизни по сравнению с плацебо. Применение у пациентов старше 18 лет с артериальной гипертензией и нарушением толерантности к глюкозе При применении валсартана и изменении образа жизни отмечалось статистически достоверное снижение риска развития сахарного диабета у данной категории пациентов. Валсартан не оказывал влияния на частоту летальных исходов в результате сердечно-сосудистых событий, инфаркта миокарда и ишемических атак без летального исхода, на госпитализации по причине сердечной недостаточности или нестабильной стенокардии, артериальной реваскуляризации, у пациентов с нарушением толерантности к глюкозе и артериальной гипертензией, отличающихся по возрасту, полу и расовой принадлежностью. Применение у детей и подростков от 6 до 18 лет при артериальной гипертензии У детей и подростков от 6 до 18 лет валсартан обеспечивает дозозависимое, плавное снижение АД. При применении валсартана максимальное снижение АД, вне зависимости от принятой дозы, обычно достигается в течение 2 недель и поддерживается на достигнутом уровне в ходе длительной терапии. Фармакокинетика: Всасывание После приема препарата внутрь максимальная концентрация (Сmах) валсартана в плазме крови достигается в течение 2-4 часов. Средняя абсолютная биодоступность 23%. При применении валсартана с пищей площадь под кривой “концентрация-время” (AUC) уменьшается на 48%, хотя, начиная примерно с 8-го часа после приема препарата, концентрация валсартана в плазме крови как в случае приема его натощак, так и в случае приема с пищей, одинаковые. Уменьшение AUC, тем не менее, не сопровождается клинически значимым снижением терапевтического эффекта, поэтому валсартан можно принимать независимо от времени приема пищи. Распределение Объем распределения (Vd) валсартана в период равновесного состояния после внутривенного введения составлял около 17 л, что указывает на отсутствие выраженного распределения валсартана в тканях. Валсартан в значительной степени связывается с белками сыворотки крови (94-97%), преимущественно с альбуминами. Метаболизм Валсартан не подвергается выраженному метаболизму (около 20% принятой внутрь дозы определяется в виде метаболитов). Гидроксильный метаболит определяется в плазме крови в низких концентрациях (менее чем 10% от AUC валсартана). Этот метаболит фармакологически неактивен. Выведение Валсартан выводится двухфазно: α-фаза с периодом полувыведения (Т1/2α) менее 1 часа и β-фаза с Т1/2β - около 9 часов. Валсартан выводится в основном в неизмененном виде через кишечник (около 83%) и почками (около 13%). После внутривенного введения, плазменный клиренс валсартана составляет около 2 л/ч и его почечный клиренс составляет 0,62 л/ч (около 30% общего клиренса). Т1/2 валсартана составляет 6 часов. Фармакокинетика у отдельных групп пациентов Пациенты с ХСН У данной категории больных время достижения Сmах и Т1/2 сходны с таковыми у здоровых добровольцев. Повышение AUC и Сmах прямо пропорционально увеличению дозы препарата (с 40 мг до 160 мг 2 раза). Фактор кумуляции составляет в среднем 1,7. При приеме внутрь клиренс валсартана составил приблизительно 4,5 л/час. Возраст пациентов с ХСН не оказывал влияния на клиренс валсартана. Пациенты в возрасте старше 65 лет У некоторых пациентов в возрасте старше 65 лет системная биодоступность валсартана выше таковой у пациентов молодого возраста, однако не имеет клинического значения. Пациенты с нарушениями функции почек Корреляция между функцией почек и системной биодоступностью валсартана отсутствует. У пациентов с нарушениями функции почек и клиренсом креатинина (КК) более 10 мл/мин коррекции дозы препарата не требуется. В настоящее время не имеется данных о применении у пациентов, находящихся на гемодиализе. Валсартан имеет высокую степень связывания с белками плазмы крови, поэтому его выведение при гемодиализе маловероятно. Пациенты с нарушениями функции печени У пациентов с легкими и умеренными нарушениями функции печени отмечается повышение биодоступности (AUC) валсартана в два раза по сравнению со здоровыми добровольцами. Однако не наблюдается корреляции значений AUC валсартана со степенью нарушения функции печени. Применение препарата у пациентов с тяжелыми нарушениями функции печени не изучалось. Пациенты от 6 до 18 лет Фармакокинетические свойства валсартана у детей и подростков в возрасте от 6 до 18 лет не отличаются от фармакокинетических свойств валсартана у пациентов старше 18 лет. Особые указания Пациенты с нарушением функции почек Следует избегать одновременного использования антагонистов рецепторов ангиотензина II, включая Диован, или ингибиторов АПФ с алискиреном у пациентов с тяжелыми нарушениями функции почек (СКФ <: 30 мл/мин). Гиперкалиемия При одновременном применении с биологически активными добавками, содержащими калий, калийсберегающими диуретиками, калийсодержащими заменителями соли, или с другими препаратами, которые могут вызывать повышение содержания калия в крови (например, с гепарином), следует соблюдать осторожность и проводить регулярный контроль содержания калия в крови. Трансплантация почки Данных по безопасности применения препарата Диован у пациентов, перенесших трансплантацию почки, нет. Дефицит в организме натрия и/или снижение ОЦК У пациентов с выраженным дефицитом в организме натрия и/или сниженным ОЦК, например, получающих высокие дозы диуретиков, в редких случаях в начале лечения препаратом может развиваться артериальная гипотензия, сопровождающаяся клиническими проявлениями. Перед началом лечения препаратом Диован следует провести коррекцию содержания в организме натрия и/или восполнить ОЦК, в том числе, путем уменьшения дозы диуретика. Стеноз почечной артерии Применение препарата коротким курсом у пациентов с реноваскулярной гипертензией, развившейся вторично вследствие одностороннего стеноза артерии единственной почки, не приводит к сколько-нибудь существенному изменению показателей почечной гемодинамики, концентрации креатинина сыворотки крови или азота мочевины крови. Однако, учитывая, что другие лекарственные средства, влияющие на РААС, могут вызывать повышение концентрации мочевины и креатинина в сыворотке крови у пациентов с двусторонним стенозом почечных артерий или стенозом артерии единственной почки, в качестве меры предосторожности рекомендуется контроль этих показателей. Первичный гиперальдостеронизм Препарат неэффективен для лечения артериальной гипертензии у пациентов с первичным гиперальдостеронизмом, поскольку у данной категории пациентов не отмечается активация РААС. ХСН/период после перенесенного инфаркта У пациентов с ХСН или после перенесенного инфаркта миокарда, начинающих лечение препаратом Диован, часто отмечается некоторое снижение АД, в связи с чем, рекомендуется контроль АД в начале терапии. При условии соблюдения рекомендаций по режиму дозирования обычно не возникает необходимости отмены препарата Диован по причине артериальной гипотензии. Оценка состояния больных ХСН должна включать оценку функции почек. Вследствие ингибирования РААС у некоторых пациентов возможны нарушения функции почек. У пациентов с ХСН II-IV функционального класса по классификации NYHA лечение ингибиторами АПФ и антагонистами рецепторов ангиотензина II может сопровождаться олигурией и/или нарастанием азотемии и в редких случаях развитием острой почечной недостаточности и/или летальным исходом. Поэтому у данных категорий пациентов перед применением препарата Диован, а также периодически во время лечения препаратом, необходимо проводить оценку функции почек. Комбинированная терапия при артериальной гипертензии При артериальной гипертензии препарат Диован может применяться в монотерапии, а так же совместно с другими гипотензивными средствами, в частности, с диуретиками. Комбинированная терапия в период после перенесенного инфаркта миокарда Возможно применение препарата Диован в комбинации с другими лекарственными препаратами, применяемые после перенесенного инфаркта миокарда, а именно тромболитиками, ацетилсалициловой кислотой в качестве антиагрегантного средства, бета-адреноблокаторами и ингибиторами ГМГ- КоА-редуктазы. У данной категории пациентов не рекомендуется применять препарат Диован одновременно с ингибиторами АПФ, поскольку данная комбинированная терапия не имеет преимуществ перед монотерапией валсартаном или ингибитором АПФ в отношении показателей общей смертности по любой причине. Комбинированная терапия при ХСН При ХСН препарат Диован может применяться как в монотерапии, так и одновременно с другими средствами - диуретиками, сердечными гликозидами, а также ингибиторами АПФ или бета-адреноблокаторами. У данной категории пациентов не рекомендуется применение тройной комбинированной терапии ингибитором АПФ, бета-адреноблокатором и препаратом Диован. Отек Квинке Отек Квинке, в том числе отек гортани и голосовых связок, приводящий к обструкции дыхательных путей, и/или отек лица, губ, глотки и/или отек языка, встречался у пациентов, получавших валсартан, у некоторых из этих пациентов ранее возникал отек Квинке на фоне приема других препаратов, в том числе ингибиторов АПФ. Прием препарата Диован в случае развития отека Квинке должен быть немедленно отменен, возобновление приема препарата Диован запрещено. Влияние на способность управлять транспортными средствами: Поскольку на фоне терапии препаратом возможно развитие таких нежелательных явлений как головокружение или обморок, пациентам, принимающим препарат Диован, следует соблюдать осторожность при управлении транспортными средствами и занятии потенциально опасными видами деятельности. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 30 °С. Предохранять от воздействия влаги. Хранить в оригинальной упаковке. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Диован Международное непатентованное название:Валсартан. Форма выпуска:таблетки, покрытые пленочной оболочкой. Состав:1 таблетка, покрытая оболочкой, содержит: активное вещество: валсартан 80,00 мг, 160,0 мг: вспомогательные вещества: кремния диоксид коллоидный 1,50 мг, 3,00 мг: целлюлоза микрокристаллическая 54,00 мг, 108,0 мг: магния стеарат 4,50 мг, 9,00 мг: кросповидон 15,00 мг, 30,00 мг: оболочка: гипромеллоза 4,80 мг, 7,20 мг: краситель железа оксид красный (Е172) 0,024 мг, 0,0225 мг: краситель железа оксид желтый (Е172) 0,006 мг, 0,576 мг: макрогол-8000 0,24 мг, 0,36 мг: титана диоксид 0,93 мг, 0,84 мг. Таблетки, покрытые оболочкой, 160 мг также содержат краситель железа оксид черный (E172) 0,0009 мг (оболочка). АТХ: Регистрация: Лекарственное средство П N013991/01 Фармгруппа: ангиотензина II рецепторов антагонист. Дата регистрации: 13.11.2009. Окончание регстрации: . Описание:Таблетки 80 мг: бледно-розовые, круглые со скошенными краями, с одной стороны риска и выдавленная надпись "D/V", с другой стороны - "NVR". Таблетки 160 мг: серо-оранжевые, овальные, с одной стороны риска и выдавленная надпись "DX/DX", с другой стороны - "NVR". Упаковка:Таблетки, 80 мг и 160 мг. По 14 шт. в блистере: календарная упаковка. 1, 2, 4 или 7 блистеров вместе с инструкцией по применению в картонной па