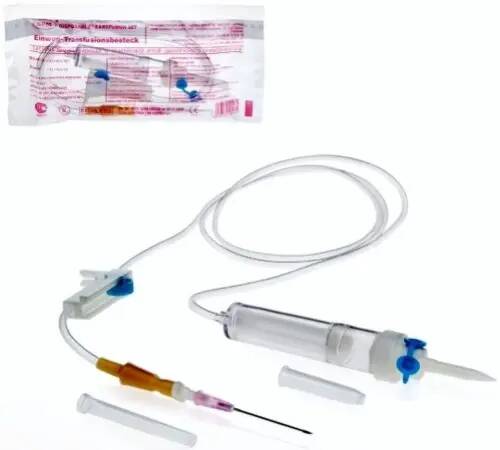
мода 80 100 шт удаление волос депиляция нетканый эпилятор восковая полоска бумага рулон вощение для женщин

Модель:
RUR 859
Бандажная лента в ролике используется при депиляции. Изготовлена из высококачественного нетканого материала, обладающего уникальными физическими и механическими характеристиками. Плотные депиляционные полоски идеальны для бандажной техники. Прочные, мягкие не промокают, не рвутся и не оставляют ворс во время процедуры. Полоска для воска имеет пористую поверхность, обеспечивая прочное сцепление. Средство для удаления воска с кожи подходит для лица: бровей и усиков, для тела: ног, рук, интимной зоны (зоны бикини), подмышек. Бандажная полоска без перфорации имеет ширину 7 см и длину 100 см, что позволяет отрезать необходимые размеры. Безопасна, гипоаллергенна, без ароматизаторов и отдушек. Профессиональная лента для удаления волос предназначена для салона красоты и для использования дома.У нас представлены любые материалы, инструменты и принадлежности для эпиляции Italwax (Италвакс). Вы можете собрать профессиональные средства в набор для депиляции и вручить как оригинальный и полезный подарок любимой жене, сестре, дочке, маме, подруге, коллеге на такие праздники как день рождения, новый год, 14 февраля (день святого валентина), выпускной и другие

Модель:
RUR 882
Полоска для депиляции в рулоне Kapous Depilation сделана из материала спанлейс. С помощью нее процесс депиляции происходит быстро и менее болезненно. Полоски не деформируются, не расслаиваются и не рвутся

Модель:
RUR 205
Почувствуй себя богиней! Одноразовые бритвы для женщин Simply Venus 2. Бритва, которая сама приспосабливается к тебе 2 лезвия обеспечивают чистое бритье. Увлажняющая полоска обеспечивает плавное скольжение и помогает защитить кожу во время бритья. Ручка в форме капли позволяет идеально контролировать движения Вашей бритвы

Модель:
RUR 209
Секрет одноразовых бритв для женщин Gillette кроется в предельной тонкости двойных лезвий. Благодаря этой особенности их головки едва скользят по коже, аккуратно сбривая волоски у самого их основания. Специальная увлажняющая полоска улучшает скольжение и

Модель:
RUR 279
Simply Venus 2 - одноразовая бритва с 2 лезвиями. Помогает сделать кожу безупречно гладкой. 2 независимо подвешенных лезвия обеспечивают более чистое бритье. Смазывающая полоска-индикатор обеспечивает плавное скольжение и помогает защитить кожу во время б
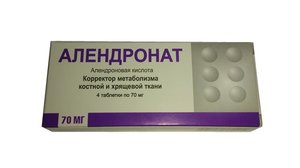
Модель:
RUR 385
Показания Остеопороз у женщин в постменопаузе (профилактика переломов костей, в.т.ч. переломов бедра и компрессионных переломов позвоночника), лечение остеопороза у мужчин с целью предотвращения возникновения переломов. Противопоказания Противопоказания Поражения пищевода, замедляющие его опорожнение, например, стриктура (сужение) или ахалазия. Невозможность стоять или сидеть прямо в течение 30 минут после приема препарата. Повышенная чувствительность к компонентам препарата. Гипокальциемия, мальабсорбция кальция, тяжелый гипопаратиреоз. Хроническая почечная недостаточность (при клиренсе креатинина менее 35 мл/мин увеличивается риск кумуляции алендроновой кислоты). Беременность и период лактации. Препарат не следует назначать беременным и кормящим женщинам, поскольку у данного контингента действие препарата не изучалось. Детский возраст. Препарат не следует назначать детям, поскольку у данного контингента действие препарата не изучалось. Дефицит лактазы, непереносимость лактозы, глюкозо-галактозная мальабсорбция. С осторожностью: Применять при заболеваниях верхних отделов желудочно-кишечного тракта в фазе обострения (дисфагия, эзофагит, гастрит, дуоденит, язвенная болезнь желудка и 12-перстной кишки), предрасположенности к гипокальциемии (гипопаратиреоз легкой и средней степени, дефицит витамина D). Беременность Алендронат противопоказан беременным и кормящим женщинам. Применение и дозы Для лечения остеопороза у женщин и у мужчин препарат назначают в дозе 70 мг 1 один раз в неделю. Алендронат необходимо принимать утром, внутрь, не разжевывая, желательно за 2 часа, но не менее чем за 30 минут до первого приема пищи, питья или приема других лекарственных, средств запивая только чистой не минерализованной водой. Другие напитки (включая минеральную воду), еда и некоторые лекарственные средства могут снизить всасывание алендроновой кислоты. Нельзя разжевывать или рассасывать таблетку в полости рта, поскольку при этом существует риск возникновения язв ротовой полости и глотки. Для облегчения поступления в желудок и, тем самым, уменьшения раздражения пищевода Алендронат следует принимать утром сразу после подъема с постели, запивая полным стаканом воды. После этого пациентам не следует ложиться до первого приема пищи, который следует производить как минимум через 30 минут после приема препарата. Алендронат не следует принимать в горизонтальном положении, перед сном или перед подъемом с постели. Несоблюдение этих, указаний может увеличить риск побочных реакций со стороны пищевода. Для пожилых пациентов и пациентов с легкой и умеренной почечной недостаточностью (клиренс креатинина от 35 до 60 мл/мин) коррекции доз не требуется. В связи с отсутствием данных Алендронат не рекомендуется для применения у больных с более тяжелой почечной недостаточностью (клиренс креатинина <:35 мл/мин). Побочные эффекты и передозировка Побочные эффекты: Со стороны желудочно-кишечного тракта: боль в животе, диспепсия, кислая отрыжка, тошнота, рвота, запор, диарея, дисфагия, метеоризм, гастрит, язва желудка, в том числе язвенная болезнь желудка, осложненная кровотечением (мелена), эрозии или язвы пищевода, эзофагит, стриктура пищевода, перфорация пищевода, язва ротоглотки, локальный остеонекроз челюсти, ассоциированный главным образом с предшествующей экстракцией зуба и/или локальной инфекцией (включая остеомиелит), часто с медленным выздоровлением. Со стороны опорно-двигательного аппарата: миалгия, боли в костях, боли в суставах, редко - тяжелые мышечные судороги, припухлость суставов, низкоэнергетические переломы тела бедренной кости. Со стороны нервной системы: головная боль, головокружение, системное головокружение, нарушение вкусовых ощущений. Кожные реакции: кожная сыпь, эритема, фотосенсибилизация, зуд, алопеция, редко - тяжелые кожные реакции, включая синдром Стивенса-Джонсона и токсический эпидермальный некролиз. Со стороны органов чувств: увеит, склерит, эписклерит. Организм в целом: реакции гиперчувствительности, включая крапивницу и редко -ангионевротический отек, преходящие симптомы реакции острой фазы в начале лечения (миалгия, недомогание, астения, редко лихорадка), гипокальциемия. Редко -периферические отеки. Передозировка: При пероральной передозировке могут возникать гипокальциемия, гипофосфатемия и побочные реакции со стороны верхних отделов желудочно-кишечного тракта, такие как расстройство пищеварения, изжога, эзофагит, гастрит, язвы желудка или пищевода. Для связывания алендроновой кислоты нужно дать выпить молоко или принять содержащие кальций антациды. В связи с риском раздражения пищевода рвоту вызывать не следует, и больной должен сохранять полностью вертикальное положение. Взаимодействие с другими ЛС: Всасывание алендроновой кислоты может нарушиться, если она принимается одновременно с препаратами кальция (включая пищевые добавки) и антацидами и другими пероральными препаратами. В связи с этим интервал между приемом Алендроната и других лекарственных средств, принимаемых внутрь, должен составлять не менее 30 минут. Комбинированное применение заместительной гормональной терапии препаратами, содержащими эстроген ± прогестин, и алендроновой кислоты у женщин с остеопорозом в период менопаузы по безопасности и переносимости сопоставимо с индивидуальным лечением каждым из этих препаратов. Известно, что внутривенное введение ранитидина удваивает биодоступность алендроновой кислоты при оральном приеме. Нестероидные противовоспалительные препараты, в том числе ацетилсалициловая кислота, могут усиливать побочные действия алендроновой кислоты со стороны желудочно-кишечного тракта. Фармакологическое действие и фармакокинетика Алендронат относится к бисфосфонатам - соединениям, которые на клеточном уровне локализуются преимущественно в зонах активной резорбции кости, под остеокластами. Алендронат не влияет на присоединение остеокластов, но угнетает их активность, тем самым ингибируют процесс резорбции костной ткани, не оказывая прямого влияния на процесс образования новой костной ткани. Во время лечения препаратом формируется нормальная костная ткань, в матрикс которой встраивается алендронат. Когда алендронат включен в костный матрикс, он фармакологически неактивен, в связи с этим алендронат должен применяться постоянно для подавления остеокластов на вновь сформированных поверхностях резорбции. Лечение алендронатом сокращает ремоделирование кости (то есть количество мест, в которых ремоделируется кость) при этом остеогенез в местах ремоделирования превышает резорбцию кости, что ведет к нарастающему росту костной массы. Фармакокинетика: Всасывание: Биодоступность алендроновой кислоты у женщин при приеме внутрь натощак не позднее, чем за 2 часа до завтрака в дозе 70 мг составляет 0,64%: у мужчин она составляет 0,6%. При приеме за 30-60 мин до еды биодоступность снижается на 40% по сравнению с дозой, принятой за 2 ч перед едой. Биодоступность алендроновой кислоты значительно снижается, если препарат принимается менее чем за 30 минут до приема пищи или жидкости, биодоступность минимальна при приеме вместе с пищей или, или в течение двух часов после еды. Совместный прием алендроновой кислоты с кофе или апельсиновым соком снижает ее биодоступность приблизительно на 60%. Распределение: Средний объем распределения алендроновой кислоты в равновесном состоянии (за исключением костной ткани) составляет, по меньшей мере, 28 л. При приеме терапевтических доз концентрация алендроновой кислоты в плазме крови незначительна (менее 5 нг/мл). Связывание алендроновой кислоты с белками плазмы составляет приблизительно 78%. Метаболизм: Нет подтверждений того, что алендроновая кислота подвергается метаболизму в организме человека или животных. Выведение: После однократного внутривенного введения алендроновой кислоты, меченной атомами углерода 14С, приблизительно 50% выводится почками в течение 72 часов: выведение меченого вещества с калом не определялось или было незначительным. После однократного внутривенного введения 10 мг алендроновой кислоты ее почечный клиренс составлял 71 мл/мин, а системный клиренс не превышал 200 мл/мин. Через 6 часов после внутривенного введения концентрация в плазме крови снижается более чем на 95%. Конечный период полувыведения превышает 10 лет, что отражает высвобождение алендроновой кислоты из косной ткани. Алендроновая кислота выводится почками. Несколько большее накопление алендроновой кислоты в костной ткани можно ожидать у пациентов с нарушением функции почек. Особые указания Алендроновая кислота, как и другие бисфосфонаты для перорального приема, может вызвать местное раздражение слизистой оболочки верхних отделов желудочно-кишечного тракта. В связи с этим необходимо с осторожностью назначать Алендронат пациентам с проблемами верхних отделов желудочно-кишечного тракта (такими как пищевод Барретта, дисфагия, другие заболевания пищевода, гастрит, дуоденит или язвы). У пациентов, принимающих алендроновую кислоту, отмечаются такие побочные реакции, как эзофагит, язва пищевода и эрозия пищевода, иногда с кровотечениями, изредка приводящие к возникновению стриктур или перфорации пищевода. В некоторых случаях данные нежелательные явления могут быть тяжелыми и требовать госпитализации. Поэтому врачам следует особенно внимательно контролировать любые симптомы, указывающие на возможные реакции со стороны пищевода. Пациентов следует предупредить о необходимости прекратить приём Алендроната и обратиться к врачу в случае появления дисфагии, боли при глотании или за грудиной, появлении или усилении изжоги. Риск возникновения тяжелых нежелательных явлений со стороны пищевода выше у пациентов, нарушающих рекомендации по приему препарата: нельзя принимать горизонтальное положение после употребления препарат и/или принимать его, не запивая, согласно рекомендациям, полным стаканом воды (170 - 230 мл), и/или продолжать принимать его при появлении симптомов раздражения пищевода. Пациенты, которые не могут выполнять указания по дозированию в силу психического заболевания, должны принимать лечение Алендронатом под соответствующим контролем. В случае пропуска приема очередной еженедельной дозы препарата следует принять 1 таблетку Алендроната в ближайший день, утром. Не рекомендуется принимать 2 таблетки в 1 день. В дальнейшем следует вернуться к приему Алендроната 1 раз в неделю, в тот же день недели, который был выбран для приема препарата изначально. При наличии гипокальциемии уровень кальция в крови необходимо нормализовать до начала лечения Алендронатом. Другие нарушения минерального обмена (например, дефицит витамина D) также должны быть устранены. У пациентов с данными нарушениями в ходе лечения Алендронатом необходимо контролировать содержание кальция в сыворотке крови и симптомы гипокальциемии. В связи с тем, что алендроновая кислота увеличивает содержание минеральных веществ в костной ткани, может наблюдаться небольшое бессимптомное снижение концентрации, кальция и фосфатов в сыворотке крови, особенно при костной болезни Педжета, с исходно значительно повышенной скоростью метаболизма костной ткани, а также у пациентов, получающих глюкокортикоиды, что сопровождается возможным уменьшением всасывания кальция. Особенно важно обеспечить адекватное поступление в организм кальция и витамина D у этих пациентов. В редких случаях гипокальциемия может быть тяжелой, обычно у пациентов с предрасположенностью к этому осложнению (гипопаратиреоидизм, дефицит витамина D, мальабсорбция кальция). Стоматология. У пациентов, принимающих бисфосфонаты, в том числе алендроновую кислоту, отмечались случаи локального остеонекроза челюсти, ассоциированного главным образом с предшествующей экстракцией зуба и/или местной инфекцией (включая остеомиелит), часто с медленным выздоровлением. В большинстве случаев локальный остеонекроз челюсти на фоне приема бисфосфонатов возникает у онкологических пациентов, получающих бисфосфонаты внутривенно. К факторам риска для локального остеонекроза челюсти относятся инвазивные зубоврачебные процедуры (например, удаление зуба, зубные, импланты, хирургические операции на кости), онкологическое заболевание, сопутствующая терапия (например химиотерапия, лучевая терапия, кортикостероиды), недостаточная гигиена полости рта, сопутствующие патологии (например, заболевания периодонта и/или другие заболевания зубов/анемия, коагулопатия, инфекция, неправильно сидящие зубные протезы) и курение. У пациентов, для которых необходимо проведение инвазивных зубоврачебных процедур, прекращение лечения бисфосфонатами может снизить риск возникновения остеонекроза челюсти. При составлении плана лечения каждого пациента необходимо руководствоваться клиническим решением лечащего врача. и/или хирурга-стоматолога, принятым на основании индивидуальной оценки соотношения польза/риск. Пациенты, у которых во время лечения бисфосфонатом развился локальный остеонекроз челюсти, должны находиться под наблюдением хирурга-стоматолога. Состояние этих пациентов может усугубиться обширной стоматологической операцией для лечения остеонекроза челюсти. Следует рассмотреть необходимость прекращения терапии бисфосфонатом, исходя из индивидуальной оценки соотношения польза/риск. Скелетно-мышечные боли. Отмечались сильные, иногда инвалидизирующие боли в костях, суставах и/или мышцах у пациентов, принимающих бисфосфонаты (в том числе алендроновую кислоту), назначенные для лечения остеопороза, в большинстве своем у женщин в постклимактерическом периоде. Симптомы появляются в период от одного дня до нескольких месяцев после начала приема препарата. При развитии тяжелых симптомов прием препарата необходимо прекратить. У большинства пациентов симптомы проходят после прекращения приема препарата. При появлении сильных скелетно-мышечных болей пациенту следует проинформировать об этом врача. Атипичные подвертельные и диафизарные переломы бедренной кости. Имеются данные об атипичных, низкоэнергетических, или низкотравматических переломах диафиза бедренной кости у пациентов, получающих лечение бисфосфонатами. Такие переломы могут локализоваться в любом месте диафиза бедренной кости, от перелома непосредственно под малым вертелом бедренной кости до надмыщелкового перелома, и являются поперечными или косопоперечными по направлению без признаков раздробления. Причинная зависимость не была установлена, поскольку эти переломы также случаются у пациентов, страдающих остеопорозом, не получающих лечение бисфосфонатами. Атипичные переломы бедренной кости чаще всего происходят при минимальном повреждении пораженной области или при его отсутствии. Они могут быть двусторонними, и у многих пациентов отмечаются продромальные боли в пораженной зоне, обычно проявляющиеся как тупая, ноющая боль в бедре, ощущаемая на протяжении от нескольких , недель до нескольких месяцев до полного перелома. В нескольких случаях отмечалось, что пациенты также получали лечение глюкокортикоидами на момент перелома. У всех пациентов, получающих Алендронат, с жалобами на боли в бедре или в паховой области, необходимо исключить атипичный или неполный перелом бедра. Пациенты с атипичным переломом также должны быть обследованы на наличие симптомов и признаков перелома в контрлатеральной конечности. Следует рассмотреть вопрос о прекращении терапии бисфосфонатами исходя из индивидуальной оценки соотношения польза/риск. Влияние на способность управлять транспортными средствами: Данных о влиянии приема алендроновой кислоты на способность управлять автомобилем и другими механизмами нет. Условия хранения и отпуска из аптек Условия хранения:В сухом, защищенном от света месте, при температуре не выше 25 °С. Хранить в недоступном для детей месте! Отпуск из аптек: По рецепту Регистрационные данные Торговое название Алендронат Международное непатентованное название:Алендроновая кислота. Форма выпуска:таблетки. Состав:Каждая таблетка содержит: Активное вещество: алендронат натрия тригидрат в количестве эквивалентном 70 мг алендроновой кислоты. Вспомогательные вещества: целлюлоза микрокристаллическая 216,63,мг, лактоза (лактопресс) 35,0 мг, карбоксиметилкрахмал натрия (натрия крахмал гликолят, примогель) 3,5 мг, магния стеарат 3,5 мг. АТХ: Регистрация: Лекарственное средство ЛП-000801 Фармгруппа: Костной резорбции ингибитор - бисфосфонат. Дата регистрации: 03.10.2011. Окончание регстрации: . Описание:Таблетки круглые белого или почти белого цвета, плоскоцилиндрической формы с фаской и риской. Упаковка:Таблетки 70 мг. По 4 или 10 таблеток в контурную ячейковую упаковку: по 1 контурной ячейковой упаковке вместе с инструкцией по медицинскому применению помещают в пачку картонную. По 28 таблеток в банку полимерную с крышкой. Каждую банку вместе с инструкцией по медицинскому применению помещают в пачку картонную. Срок годности:2 года. Не использовать препарат после истечения срока годности, указанного на упаковке. Владелец рег.удостоверения:Березовский фармацевтический завод, ЗАО Производитель:Березовский фармацевтический завод, ЗАО. Представительство
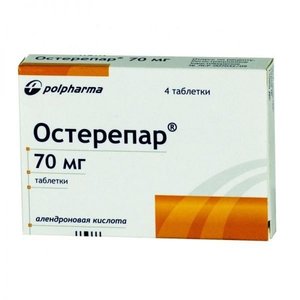
Модель:
RUR 411
Показания Лечение остеопороза у женщин в постменопаузе с целью предупреждения развития переломов, в т.ч. переломов бедра и компрессионных переломов позвоночника: - лечение остеопороза у мужчин с целью предотвращения возникновения переломов. Противопоказания Противопоказания - Повышенная чувствительность к компонентам препарата: - аномалии пищевода и другие факторы, затрудняющие проходимость пищевода (ахалазия, стриктура и т.д.): - неспособность пациента оставаться в вертикальном положении, хотя бы сидя, в течение 30 минут: - гипокальциемия: - хроническая почечная недостаточность (клиренс креатинина (КК) <: 35 мл/мин): - беременность, период грудного вскармливания: - детский возраст: - дефицит витамина D: - тяжелые нарушения минерального обмена. - дефицит лактазы, непереносимость галактозы, глюкозо-галактозная мальабсорбция (препарат содержит лактозу). С осторожностью: Заболевания пищеварительного тракта в фазе обострения (дисфагия, заболевания пищевода, гастрит, дуоденит, язва, серьезное заболевание желудочно-кишечного тракта в предшествующие 12 месяцев, например, пептическая язва, желудочно-кишечное кровотечение, хирургическое вмешательство, за исключением операций на спастическом привратнике желудка). Беременность Беременность: нет данных о применении алендроновой кислоты у беременных женщин. При исследованиях на животных было выявлено нарушение формирования костной ткани плода при применении высоких доз алендроновой кислоты, дисфункция родовой деятельности, связанная с гипокалиемией. Применение алендроновой кислоты во время беременности противопоказано. Период грудного вскармливания: данных о проникновении в грудное молоко нет: прием алендроновой кислоты в период кормления грудью противопоказан. Применение и дозы Внутрь, не разжевывая, запивая питьевой водой, по крайней мере, за 30 минут до первого приема пищи, жидкости или лекарственных препаратов. Другие напитки (включая минеральную воду), пища и некоторые лекарственные средства могут уменьшить всасывание препарата Остерепар®. Для уменьшения риска возникновения раздражения пищевода препарат Остерепар® следует принимать, выполняя следующие правила: принимать утром сразу после подъема с постели: запивать полным стаканом воды для облегчения поступления таблетки в желудок: не разжевывать таблетки и не рассасывать их во рту из-за возможного образования язв в ротовой полости и глотке: пациентам не следует ложиться до первого приема пищи, который следует производить как минимум через 30 минут после приема препарата Остерепар®: препарат Остерепар® не следует принимать перед сном или перед подъемом с постели. Пациентам следует дополнительно принимать препараты кальция и витамина D, если поступление этих веществ с пищей недостаточно. Лечение остеопороза у женщин в постменопаузе: рекомендуемая доза - 1 таблетка 70 мг 1 раз в неделю. Лечение остеопороза у мужчин: рекомендуемая доза - 1 таблетка 70 мг 1 раз в неделю. Оптимальная длительность применения препарата не установлена. Необходимость продолжения терапии бисфосфонатами должна оцениваться на регулярной основе, особенно после 5 и более лет применения. Для пациентов пожилого возраста и пациентов с почечной недостаточностью легкой и средней степени тяжести (КК от 35 до 60 мл/мин) коррекции дозы не требуется. Препарат Остерепар® не рекомендуется назначать пациентам с почечной недостаточностью тяжелой степени (КК <: 35 мл/мин) в связи с отсутствием опыта применения у данных пациентов. Детский возраст: из-за отсутствия клинических данных детям препарат не назначают. Побочные эффекты и передозировка Побочные эффекты: Профили безопасности алендроновой кислоты при применении у женщин в постменопаузе в дозе 70 мг в неделю и в дозе 10 мг/сутки, по данным одногодичного клинического исследования оказались схожими. В ходе двух трехгодичных клинических исследований применения алендроновой кислоты у женщин в постменопаузе в дозе 10 мг/сутки показано, что общие профили безопасности алендроновой кислоты и плацебо подобны. В таблице 1 представлены нежелательные реакции, связь которых с приемом алендроновой кислоты возможна, вероятна или несомненна, если они отмечались с частотой не менее 1% в группе, получавшей алендроновую кислоту в дозе 70 мг в неделю в одногодичном исследовании, или с частотой не менее 1% в группе, получавшей алендроновую кислоту в дозе 10 мг/сутки в трехгодичных исследованиях. Таблица 1. ТАБЛИЦЪ В широкой клинической практике (включая данные клинических исследований и данные постмаркетингового применения) сообщалось о следующих нежелательных эффектах, которые классифицированы в соответствии с их частотой развития (классификация ВОЗ): очень часто ( 1/10), часто ( 1/100, <:1/10), нечасто ( 1/1000, <:1/100), редко ( 1/10 000, <:1/1000), очень редко (<:1/10 000, включая отдельные сообщения): Аллергические реакции: редко - реакции гиперчувствительности, включая крапивницу, ангионевротический отек. Со стороны лабораторных показателей: редко - симптоматическая гипокальциемия (особенно при наличии факторов риска). Со стороны ЦНС: часто - головная боль, головокружение: нечасто - нарушение вкусовых ощущений. Со стороны органа зрения: нечасто - увеит, склерит, эписклерит. Со стороны органов слуха и равновесия: часто - нарушение равновесия. Со стороны пищеварительной системы: часто - боли в животе, диспепсия, запор, диарея, язва пищевода, дисфагия, вздутие живота, кислая отрыжка: нечасто - тошнота, рвота, гастрит, мелена, эзофагит, эрозии пищевода: редко - стриктура пищевода, изъязвление ротоглотки, перфорация, язвы, кровотечения из верхних отделов желудочно-кишечного тракта. Со стороны кожи и кожных придатков: часто - зуд, алопеция: нечасто - кожная сыпь, эритема: редко - сыпь с фотосенсибилизацией, тяжелые кожные реакции, включая синдром Стивенса-Джонсона и токсический эпидермальный некролиз. Со стороны костно-мышечной системы: очень часто - миалгия, боли в костях, боли в суставах (иногда - тяжелого течения): часто - припухлость суставов: редко - остеонекроз нижней челюсти, атипичные переломы тела бедренной кости. Со стороны организма в целом: часто - астения, периферические отеки: нечасто - преходящие симптомы реакции острой фазы в начале лечения (миалгия, недомогание, реже - лихорадка), обычно в начале лечения. Передозировка: Симптомы: боли в животе, диспептические расстройства, дисфагия, изжога, эзофагит, гастрит: могут развиться гипокальциемия и гипофосфатемия. Лечение: симптоматическое. Показано применение молока и антацидных препаратов для связывания алендроната. В связи с риском поражения пищевода не следует вызывать рвоту, пациент должен находиться в вертикальном положении. Взаимодействие с другими ЛС: Кальций, антациды, некоторые пероральные препараты, пища, напитки, в т.ч. минеральные воды влияют на всасываемость алендроната: лекарственные средства можно принимать внутрь не ранее чем через 1 ч после приема алендроната. Ранитидин повышает биодоступность (клиническое значение неизвестно). При совместном применении препарата Остерепар® и заместительной гормональной терапии (эстроген ± прогестин) безопасность и переносимость комбинированной терапии соответствуют таковым при применении каждого из этих препаратов в отдельности. В клинических исследованиях препарата Остерепар® у мужчин, женщин в постменопаузе и пациентов, принимающих глюкокортикостероиды, не было выявлено клинически значимого лекарственного взаимодействия в отношении влияния на связывание с белками, почечной экскреции и метаболизма. Частота нежелательных явлений со стороны верхнего отдела желудочно-кишечного тракта (ЖКТ) увеличивается при сочетании препарата Остерепар® в дозе более 10 мг/сут с препаратами, содержащими ацетилсалициловую кислоту. Однако данный эффект не наблюдался при приеме препарата Остерепар® в дозе 70 мг 1 раз в неделю. Препарат Остерепар® может быть назначен с осторожностью (из-за риска развития желудочно-кишечного кровотечения) пациентам, принимающим нестероидные противовоспалительные препараты, однако по результатам клинического исследования не было выявлено клинически значимого лекарственного взаимодействия и увеличения частоты побочных эффектов при совместном применении препаратов. Фармакологическое действие и фармакокинетика Ингибитор костной резорбции. Относится к группе бисфософонатов, которые, локализуясь в зонах активной резорбции кости, под остеокластами, ингибируют процесс резорбции костной ткани, обусловленный остеокластами, не оказывая прямого влияния на процесс образования новой костной ткани. Поскольку резорбция кости и появление новой костной ткани взаимосвязаны, образование кости также снижается, но в меньшей степени, чем резорбция, что приводит к прогрессирующему увеличению костной массы. Во время лечения алендронатом формируется нормальная костная ткань, в матрикс которой встраивается алендронат, оставаясь фармакологически неактивным. В терапевтических дозах алендронат не вызывает остеомаляцию. Фармакокинетика: Всасывание После приема внутрь в дозах 5-70 мг натощак не позднее, чем за 2 ч до стандартного завтрака биодоступность алендроната составляет 0,64% у женщин и 0,6% - у мужчин. После приема алендроната натощак за 1-1,5 ч до стандартного завтрака биодоступность снижается приблизительно на 40%. У пациентов с остеопорозом препарат Остерепар® эффективен при применении натощак не позднее, чем за 30 минут до первого приема пищи или жидкости. Биодоступность алендроната незначительна при его назначении одновременно с приемом пищи или в течение 2 ч после приема пищи. Одновременный прием с кофе или апельсиновым соком снижает биодоступность препарата приблизительно на 60%. При приеме преднизолона в дозе 20 мг 3 раза/сут в течение 5 дней не происходит клинически значимого изменения биодоступности алендроната. Распределение Средний объем распределения алендроната в равновесном состоянии (за исключением костной ткани) составляет, по меньшей мере, 28 л. При приеме в терапевтических дозах концентрация препарата в плазме крови незначительна (менее 5 нг/мл). Связывание алендроната с белками плазмы составляет приблизительно 78%. Метаболизм Нет данных о том, что алендронат подвергается метаболизму в организме человека или животных. Выведение После однократного внутривенного (в/в) введения алендроната, меченного атомами углерода [14С], приблизительно 50% препарата выводится с мочой в течение 72 ч: выведение меченого препарата с калом было незначительным или не определялось. После однократного в/в введения алендроната в дозе 10 мг его почечный клиренс составляет 71 мл/мин. Через 6 ч после в/в ведения концентрация в плазме крови снижается более чем на 95%. Конечный T1/2 превышает 10 лет, что отражает высвобождение препарата из костной ткани. Алендронат не нарушает выведение препаратов через кислотные и основные транспортные системы почек. Пол. Биодоступность алендроновой кислоты существенно не отличается у мужчин и женщин. Пожилой возраст. Биодоступность и выведение алендроновой кислоты сходны у пожилых и молодых пациентов. Раса. Фармакокинетические различия по расовому признаку не были изучены. Нарушение функции печени. У пациентов с нарушением функции печени нет необходимости корригировать дозу алендроновой кислоты, поскольку она не метаболизируется и не выводится с желчью. Особые указания Препарат Остерепар®, как и другие бисфосфонаты, может вызывать местное раздражение слизистой оболочки верхних отделов ЖКТ. У пациентов, получающих лечение препаратом Остерепар®, отмечаются такие побочные реакции, как эзофагит, язва пищевода и эрозия пищевода, изредка приводящие к возникновению стриктур или перфорации пищевода. В некоторых случаях данные нежелательные явления могут быть тяжелыми и требовать госпитализации, поэтому следует особенно внимательно контролировать любые симптомы, указывающие на возможные нарушения со стороны пищевода. Пациентов следует предупредить о необходимости прекратить прием препарата Остерепар® и обратиться к врачу в случае появления дисфагии, боли при глотании или за грудиной, появлении или усилении изжоги. Риск возникновения тяжелых нежелательных явлений со стороны пищевода выше у пациентов, которые нарушают рекомендации по приему препарата и/или продолжают принимать его при появлении симптомов раздражения пищевода. Особенно важно, чтобы пациент имел рекомендации по приему препарата, понимал их и был информирован о том, что риск развития поражения пищевода возрастает в случае невыполнения данных рекомендаций. Известны редкие случаи появления язвы желудка и двенадцатиперстной кишки, иногда тяжелой и осложненной (причинно-следственная связь с приемом препарата не установлена). Препарат Остерепар® следует назначать с осторожностью пациентам с обострениями заболеваний верхних отделов ЖКТ, такими как дисфагия, заболевания пищевода, гастрит, дуоденит и язвы из-за возможного раздражающего действия препарата на слизистую оболочку верхних отделов ЖКТ и ухудшением течения основного заболевания. Решение о проведении лечения необходимо принимать для каждого пациента индивидуально после тщательной оценки соотношения риск/польза, особенно для пациентов с пищеводом Барретта. Известны случаи появления локального остеонекроза челюсти, ассоциированного главным образом с предшествующей экстракцией зуба и/или локальной инфекцией (включая остеомиелит), часто с медленным выздоровлением. В большинстве случаев остеонекроз челюсти на фоне приема бисфосфонатов возникает у онкологических пациентов, получающих бисфосфонаты в/в. Известные факторы риска остеонекроза челюсти включают онкологическое заболевание, сопутствующую терапию (например, химиотерапия, лучевая терапия, кортикостероиды), плохую гигиену полости рта и сопутствующие патологии (например, заболевания периодонта и/или другие заболевания зубов, анемия, коагулопатия, инфекция) и курение. Пациентам, у которых развивается остеонекроз челюсти, должна быть оказана специализированная медицинская помощь челюстно-лицевым хирургом, а вопрос об отмене терапии бисфосфонатами должен быть рассмотрен, исходя из индивидуальной оценки соотношения риск/польза. Стоматологическое хирургическое вмешательство может привести к ухудшению состояния. Тактика лечения каждого пациента, которому требуется инвазивное стоматологическое вмешательство (например, удаление зуба, имплантация), включая терапию бисфосфонатами, должна основываться на клиническом суждении лечащего врача и/или челюстно-лицевого хирурга и индивидуальной оценке соотношения риск/польза. Сообщалось о возникновении болей в костях, суставах и/или мышцах у пациентов, получающих бисфосфонаты. Эти симптомы редко носят тяжелый характер и/или приводят к потере трудоспособности. Время до появления симптомов варьирует от одного дня до нескольких месяцев от начала терапии. У большинства пациентов после прекращения терапии симптомы отступают, но у некоторых пациентов появляются вновь после возобновления приема того же препарата или другого бисфосфоната. Сообщалось о возникновении патологических (т.е. при воздействии незначительной силы или самопроизвольных) подвертельных переломов или переломов проксимальных отделов диафиза бедренной кости у небольшого количества пациентов, принимающих бисфосфонаты. Некоторые из переломов относились к категории стрессовых (также известны под названиями нагрузочный перелом, маршевый перелом, перелом Дойчлендера), возникающих в отсутствие травмы. Некоторые пациенты за недели или месяцы до возникновения полного перелома испытывали продромальные боли в пораженной области, часто связанные с характерной рентгенологической картиной стрессового перелома. Количество сообщений было очень небольшим, кроме того, стрессовые переломы со сходными клиническими особенностями возникают и у пациентов, не принимающих бисфосфонаты. Пациентов со стрессовыми переломами необходимо обследовать с оценкой известных причин и факторов риска (например, дефицит витамина D, нарушение всасывания, применение кортикостероидов, стрессовый перелом в анамнезе, артрит или перелом нижней конечности, чрезмерные или увеличенные нагрузки, сахарный диабет, хронический алкоголизм) и предоставить им надлежащую ортопедическую помощь. Приблизительно одна треть стрессовых переломов являлась двусторонними: соответственно, у пациентов, перенесших перелом тела бедренной кости, должно быть обследовано контралатеральное бедро. До получения результатов обследования следует рассмотреть вопрос о приостановке приема бисфосфонатов у пациентов со стрессовыми переломами, исходя из оценки соотношения польза/риск в каждом конкретном случае. Пациентов следует предупредить, что при случайном пропуске приема препарата Остерепар® 1 раз в неделю, они должны принять одну таблетку утром ближайшего дня. Не следует принимать две дозы в один день, но в последующем надо вернуться к приему препарата 1 раз в неделю в тот день недели, который был выбран в начале лечения. Следует принимать во внимание и другие причины остеопороза, помимо дефицита эстрогенов, возраста и лечения глюкокортикоидами. При наличии гипокальциемии уровень кальция в крови необходимо нормализовать до начала лечения препаратом Остерепар®. Другие нарушения минерального обмена (например, дефицит витамина D) также должны быть устранены. У пациентов с данными нарушениями необходимо контролировать содержание кальция в крови и симптомы гипокальциемии. Поскольку препарат Остерепар® увеличивает содержание минеральных веществ в костях, может наблюдаться небольшое бессимптомное снижение уровня кальция и фосфатов в сыворотке крови, особенно при костной болезни Педжета, с исходно значительно повышенной скоростью метаболизма костной ткани, а также у пациентов, получающих глюкокортикоиды, что сопровождается возможным уменьшением всасывания кальция. Особенно важно обеспечить адекватное поступление в организм кальция и витамина D у этих пациентов. В редких случаях гипокальциемия может быть тяжелой, обычно у пациентов с предрасположенностью к этому осложнению (гипопаратиреоидизм, дефицит витамина D, мальабсорбция кальция). Препарат содержит лактозу. Пациенты с дефицитом лактазы, непереносимостью галактозы, глюкозо-галактозной мальабсорбцией должны воздержаться от применения препарата. Влияние на способность управлять транспортными средствами: Данных о влиянии препарата на способность управлять автомобилем и другими механизмами нет. Однако некоторые побочные эффекты, наблюдаемые после приема алендроната, могут у некоторых пациентов ухудшать способность к управлению транспортными средствами и обслуживанию механизмов. Условия хранения и отпуска из аптек Условия хранения:При температуре не выше 25°С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Остерепар® Международное непатентованное название:Алендроновая кислота. Форма выпуска:таблетки. Состав:1 таблетка содержит: активное вещество: натрия алендроната тригидрат - 91,36 мг (соответствует 70 мг алендроновой кислоты): вспомогательные вещества: лактозы моногидрат - 128,64 мг, микрокристаллическая целлюлоза - 65,00 мг, кроскармеллоза натрия - 15,00 мг, магния стеарат - 3,00 мг, кремния диоксид коллоидный безводный - 2,00 мг. АТХ: Регистрация: Лекарственное средство ЛСР-007042/09 Фармгруппа: Костной резорбции ингибитор - бисфосфонат. Дата регистрации: 07.09.2009 / 18.03.2014. Окончание регстрации: . Описание:Таблетки белого цвета, продолговатые, двояковыпуклые. Упаковка:Таблетки 70 мг. По 4 таблетки в блистер из фольги A1/PVC. 1 блистер вместе с инструкцией по применению помещают в картонную пачку. Срок годности:2 года. Не применять по истечении срока годности. Владелец рег.удостоверения:Фармацевтический завод "ПОЛЬФАРМА" АО Производитель:POLPHARMA, S.A. Представительство:АКРИХИН ОАО
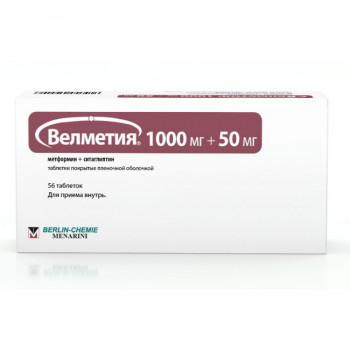
Модель:
RUR 3030
Показания Монотерапия Препарат показан в качестве стартовой терапии больным сахарным диабетом 2 типа для улучшения контроля над гликемией, если соблюдение диеты и режима физических нагрузок не позволяют добиться адекватного контроля. Препарат показан в качестве дополнения к диете и режиму физических нагрузок для улучшения контроля над гликемией у больных сахарным диабетом 2 типа, не достигших адекватного контроля на фоне монотерапии метформином или ситаглиптином, либо после неуспешного комбинированного лечения двумя препаратами. Комбинированная терапия Препарат показан пациентам с сахарным диабетом 2 типа для улучшения контроля гликемии в комбинации с производными сульфонилмочевины (тройная комбинация: метформин + ситаглиптин + производное сульфонилмочевины), когда диета и режим физических нагрузок в сочетание с двумя из этих трех препаратов: метформин, ситаглиптин или производные сульфонилмочевины не приводят к адекватному гликемическому контролю. Препарат показан пациентам с сахарным диабетом 2 типа для улучшения контроля гликемии в комбинации с тиазолидиндионами (агонистами PPARγ -рецепторов, активируемых пролифератором пероксисом), когда диета и режим физических нагрузок в сочетание с двумя из трех этих препаратов: метформин, ситаглиптин или тиазолидиндион не приводят к адекватному гликемическому контролю. Препарат показан пациентам с сахарным диабетом 2 типа для улучшения контроля гликемии в комбинации с инсулином, когда диета и режим физических нагрузок в сочетание с инсулином не приводят к адекватному гликемическому контролю. Противопоказания Противопоказания - известная повышенная чувствительность к ситаглиптину, метформину или какому-либо из компонентов препарата - сахарный диабет 1 типа- заболевание почек или снижение функции почек (при концентрации креатинина сыворотки 1,5 мг/дл и 1,4 мг/дл у мужчин и женщин, соответственно, или снижении клиренса креатинина (<: 60 мл/мин), в том числе вследствие сердечно-сосудистого коллапса (шока), острого инфаркта миокарда или септицемии- острые состояния, протекающие с риском развития нарушений функции почек- дегидратация (при диарее, рвоте), лихорадка, тяжёлые инфекционные заболевания- состояния гипоксии (шок, сепсис, почечные инфекции, бронхо-легочные заболевания)- острый или хронический метаболический ацидоз, включая диабетический кетоацидоз (с комой или без)- клинически выраженные проявления острых и хронических заболеваний, которые могут приводить к развитию тканевой гипоксии (в том числе, сердечная или дыхательная недостаточность, острый инфаркт миокарда)- обширные хирургические операции и травмы, когда показано проведение инсулинотерапии (см. раздел "Особые указания")- печеночная недостаточность, нарушение функции печени- хронический алкоголизм, острое отравление алкоголем- беременность, период грудного вскармливания- лактоацидоз (в т.ч. и в анамнезе)- применение в течение не менее 48 ч. до и в течение 48 ч. после проведения радиоизотопных или рентгенологических исследований с введением йодсодержащего контрастного вещества (см. раздел "Взаимодействие с другими лекарственными средствами")- соблюдение гипокалорийной диеты (менее 1000 ккал/сут)- детский возраст до 18 лет. С осторожностью: Применение у пожилых Поскольку основным путем выведения ситаглиптина и метформина являются почки, и поскольку с возрастом выделительная функция почек снижается, меры предосторожности при назначении препарата нарастают пропорционально возрасту. Пожилым пациентам проводят тщательный подбор дозы и регулярный контроль функции почек (см. "Особые указания", Мониторинг функции почек). Ситаглиптин. По данным клинических исследований эффективность и безопасность ситаглиптина у пожилых (>:65 лет) пациентов была сравнима с эффективностью и безопасностью у молодых (<:65 лет). Метформин. Число пожилых пациентов среди участников контролируемых исследований метформина было недостаточным для вынесения формального заключения о возрастных различиях в эффективности и безопасности препарата, хотя по имеющимся данным таких различий не наблюдали. Поскольку метформин выводится преимущественно почками, и при их нарушенной функции возрастает вероятность побочных реакций, препарат следует назначать только пациентам с подтвержденной нормальной функцией почек (см. "Противопоказания"). Беременность Не проводилось адекватно контролируемых исследований препарата или его компонентов у беременных, следовательно, данных о безопасности его применения у беременных женщин нет. Препарат, как и другие пероральные гипогликемические препараты, не рекомендован к применению во время беременности. Не проводилось экспериментальных исследований комбинированного препарата для оценки его влияния на репродуктивную функцию. Приводятся только имеющиеся данные из исследований ситаглиптина и метформина. Ситаглиптин. Ситаглиптин не продемонстрировал тератогенности в период органогенеза при пероральном введении крысам в суточных дозах до 250 мг/кг или кроликам в дозах до 125 мг/кг (что преывшает плазменную экспозицию препарата у человека в 32 и 22 раза, соответственно, после приема рекомендованной суточной терапевтической дозы 100 мг). Отмечали незначительное увеличение частоты мальформации ребер у потомства (отсутствие, гипоплазия, искривление) при пероральном введении препарата в суточных дозах 1000 мг/кг (что превышает экспозицию у человека примерно в 100 раз после приема рекомендованной суточной дозы 100 мг). Незначительное снижение массы тела у обоих полов потомства крыс в период грудного вскармливания и снижение темпов прибавки в весе по окончании грудного вскармливания у самцов при пероральном введении беременным самкам препарата в суточной дозе 1000 мг/кг. Тем не менее, данные экспериментальнх репродуктивных исследований не всегда соотносятся напрямую с влиянием препарата на репродуктивную функцию человека. Метформин. Метформин не продемонстрировал тератогенности при пероральном введении крысам в суточных дозах до 600 мг/кг. Это преывшает плазменную экспозицию препарата у человека в 2 и 6 раз (у крыс и кроликов, соответственно) после приема максимальной рекомендованной суточной терапевтической дозы 2000 мг. Значения плазменной концентрации препарата у плода свидетельствуют о частичном плацентарном переносе. Экспериментальные исследования по определению секреции компонентов комбинированного препарата в грудное молоко не проводились. По данным исследований по отдельным препаратам, как ситаглиптин, так и метформин секретируются в грудное молоко крыс. Данных о секреции ситаглиптина в грудное молоко человека нет. Следовательно, препарат не следует назначать в период лактации. Применение и дозы Общая информация: Режим дозирования препарата должен подбираться индивидуально, исходя из текущей терапии, эффективности и переносимости, но не превышая максимальную рекомендуемую суточную дозу ситаглиптина 100 мг. Препарат обычно назначают в режиме 2 раза в день во время еды, с постепенным увеличением дозы, с целью минимизации возможных побочных эффектов со стороны желудочно-кишечного тракта (ЖКТ), характерных для метформина. Рекомендации по дозированию:Начальная доза препарата зависит от текущей гипогликемической терапии. Препарат принимают 2 раза в день во время еды. Предлагаются следующие дозировки препарата:500 мг метформина / 50 мг ситаглиптина 850 мг метформина / 50 мг ситаглиптина 1000 мг метформина / 50 мг ситаглиптина Стартовая терапия:Больным сахарным диабетом 2 типа с неадекватным гликемическим контролем на фоне соблюдения диеты и режима физических нагрузок рекомендуемая стартовая доза препарата составляет 500 мг метформина / 50 мг ситаглиптина 2 раза в день. Впоследствии дозу можно увеличить до 1000 мг метформина / 50 мг ситаглиптина 2 раза в день. Для пациентов, не достигших адекватного контроля на монотерапии метформином:Рекомендуемая стартовая доза препарата для пациентов, не достигших адекватного контроля на монотерапии метформином должна обеспечить рекомендуемую терапевтическую суточную дозу ситаглиптина 100 мг, т.е. по 50 мг ситаглиптина 2 раза в день плюс текущая доза метформина. Для пациентов, не достигших адекватного контроля на монотерапии ситаглиптином:Рекомендуемая стартовая доза препарата для пациентов, не достигших адекватного контроля на монотерапии ситаглиптином, составляет 500 мг метформина / 50 мг ситаглиптина 2 раза в день. В дальнейшем доза может бытьувеличена до 1000 мг метформина / 50 мг ситаглиптина 2 раза в день. Пациентам, принимающим скорректированную ввиду почечной недостаточности дозу ситаглиптина, лечение препаратом противопоказано (см. "Противопоказания"). Для пациентов, принимающих комбинацию препаратов ситаглиптин и метформин: При переходе с комбинированного лечения ситаглиптином и метформином стартовая доза препарата может быть эквивалентной дозам принимаемых по отдельности ситаглиптина и метформина. Для пациентов, принимающих два из перечисленных трех гипогликемических препаратов - ситаглиптин, метформин или производные сулъфонилмочевины: Стартовая доза препарата должна обеспечить рекомендуемую терапевтическую суточную дозу ситаглиптина 100 мг, т.е. по 50 мг ситаглиптина 2 раза в день. Стартовую дозу метформина определяют исходя из уровня гликемического контроля и текущей (если пациент принимает этот препарат) дозы метформина. Увеличение дозы метформина должно быть постепенным для минимизации связанных с ним побочных эффектов со стороны ЖКТ. Пациентам, принимающим производное сулъфонилмочевины, будет рациональным снизить текущую дозу для снижения риска сульфонил-индуцированной гипогликемии (см. "Особые указания"). Для пациентов, принимающих два из перечисленных трех гипогликемических препаратов - ситаглиптин, метформин или агонисты PPARγ - рецепторов (тиазолидиндионы):Стартовая доза препарата должна соответствовать суточной дозе ситаглиптина 100 мг, т.е. по 50 мг ситаглиптина 2 раза в день и ранее принимаемой дозе метформина. В случае необходимости увеличения дозы метформина рекомендована постепенная титрация препарата для избежания гастроинтенстинальных побочных эффектов. Для пациентов, принимающих два из перечисленных трех гипогликемических препаратов - ситаглиптин, метформин или инсулин:Стартовая доза препарата должна соответствовать суточной дозе ситаглиптина 100 мг, т.е. по 50 мг ситаглиптина 2 раза в день и ранее принимаемой дозе метформина. В случае необходимости увеличения дозы метформина рекомендована постепенная титрация препарата для избежания гастро-интенстинальных побочных эффектов. Пациентам может потребоваться снижение дозы инсулина для предотвращения риска гипогликемии (см. "Особые указания"). Специальных исследований по оценке безопасности и эффективности перехода с лечения другими гипогликемическими препаратами на лечение комбинированным препаратом не проводилось. Любые изменения в лечении сахарного диабета 2 типа должны проводиться с осторожностью и под контролем соответствующих параметров с учетом возможных изменений гликемического контроля. Применение у детей. Безопасность препарата у детей и подростков моложе 18 лет не изучалась. Побочные эффекты и передозировка Побочные эффекты: В плацебо-контролируемых исследованиях комбинированное лечение ситаглиптином и метформином в целом хорошо переносилось пациентами с сахарным диабетом 2 типа. Частота побочных эффектов при комбинированном лечении ситаглиптином и метформином была сравнимой с частотой при приеме метформина в комбинации с плацебо. Комбинированное лечение ситаглинтином и метформином. Стартовая теpaпияВ 24-недельном плацебо-контролируемом факториальном исследовании начальной комбинированной терапии ситаглиптином и метформином (ситаглиптин 50 мг +метформин 500 мг или 1000 мг х 2 раза в сутки) в группе комбинированной терапии по сравнению с группами монотерапииметформином (500 мг или 1000 мг х 2 раза в сутки), ситаглиптином (100 мг 1 раз в сутки) или плацебо наблюдались следующие связанные с приемом препарата нежелательные реакции, наблюдавшиеся с частотой 1% в группе комбинированного лечения и чаще, чем в группе плацебо: диарея (ситаглиптин + метформин - 3,5%, метформин - 3,3%, ситаглиптин - 0,0%, плацебо -1,1 %), тошнота (1,6%, 2.5%, 0,0% и 0,6%), диспепсия (1,3%, 1,1%. 0,0% и 0,0%), метеоризм (1,3%, 0,5%, 0,0% и 0,0%), рвота (1,1%. 0,3%. 0,0% и 0,0%), головная боль (1,3%, 1,1%, 0,6% и 0,0%) и гипогликемия (1,1%, 0,5%, 0,6% и 0,0%). Добавление ситаглиптина к текущей терапии метформином В 24-недельном плацебо-контролируемом исследовании при добавлении ситаглиптииа в дозе 100 мг/сут к текущему лечению метформином единственной нежелательной реакцией, связанной с приемом препарата и наблюдавшейся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо, была тошнота (ситаглиптин + метформин - 1,1%, плацебо + метформин - 0,4%). Гиногликемия и нежелательные реакции со стороны ЖКТВ плацебо-контролируемых исследованиях комбинированного лечения ситаглиптином и метформином частота развития гипогликемии (независимо от причинно-следственной связи) в группах комбинированной терапии была сопоставимой с частотой в группах лечения метформином в сочетании с плацебо (1,3-1,6% и 2,1% соответственно). Частота отслеживаемых нежелательных реакций со стороны ЖКТ (независимо от причинно-следственной связи) в группах комбинированного лечения ситаглиптином и метформином была сопоставимой с частотой в группах монотерапии метформином: диарея (ситаглиптин +метформин - 7,5%, метформин - 7,7%), тошнота (4,8%, 5,5%), рвота (2,1%. 0,5%), боль в животе (3,0%, 3,8%). Во всех исследованиях нежелательные реакции в виде гипогликемии регистрировались на основании всех сообщений о клинически выраженных симптомах гипогликемии: дополнительное измерение концентрации глюкозы в крови не требовалось. Комбинированное лечение ситаглиптином, метформином и производным сульфонилмочевиныВ 24-недельном плацебо-контролируемом исследовании с применением ситаглиптина в дозе 100 мг/сут на фоне текущего комбинированного лечения глимепиридом в дозе 4 мг/сут и метформином в дозе 1500 мг/сут наблюдались следующие связанные с приемом препарата нежелательные реакции, наблюдавшиеся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо: гипогликемия (ситаглиптин - 13,8%, плацебо - 0,9%), запор (1,7% и 0,0%). Комбинированное лечение ситаглиптином, метформином и агонистом PPARγ По данным плацебо-контролируемого исследования с применением ситаглиптина в дозе 100 мг/сут на фоне текущего комбинированного лечения росиглитазоном и метформином на 18 неделе лечения наблюдались следующие связанные с приемом препарата нежелательные реакции, наблюдавшиеся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо: головная боль (ситаглиптин - 2,4%, плацебо - 0,0%), диарея (1,8%, 1,1%), тошнота (1,2%, 1,1%), гипогликемия (1,2%. 0,0%), рвота (1,2%, 0.0%). На 54 неделе комбинированного лечения наблюдались следующие связанные с приемом препарата нежелательные реакции, наблюдавшиеся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо: головная боль (ситаглиптин -2,4%, плацебо - 0,0%), гипогликемия (2.4%, 0,0%), инфекции верхних дыхательных путей (1,8%, 0,0%), тошнота (1,2%, 1,1 %), кашель (1,2%. 0,0%), грибковые инфекции кожи (1,2%, 0,0%), периферические отеки (1,2%. 0,0%), рвота (1,2%, 0,0%). Комбинированное лечение ситаглиптином, метформином и инсулиномВ 24-недельном плацебо-контролируемом исследовании с применением ситаглиптина в дозе 100 мг/сут на фоне текущегокомбинированного лечения метформином в дозе 1500 мг/сут и постоянной дозы инсулина единственной нежелательной реакцией, связанной с приемом препарата и наблюдавшейся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо, была гипогликемия (ситаглиптин - 10,9%, плацебо - 5,2%). В другом 24-недельном исследовании, в котором пациенты получали ситаглиптин в качестве дополнительной терапии к терапии инсулином (с или без метформина), единственной нежелательной реакцией, наблюдавшейся с частотой 1% в группе лечения ситаглиптином и метформином, и чаще чем в группе плацебо и метформина, была рвота (ситаглиптин и метформин -1,1%, плацебо и метформин - 0,4%). ПанкреатитВ обобщенном анализе 19 двойных-слепых рандомизированных клинических исследований применения ситаглиптина (в дозе 100 мг/сут) или соответствующего препарата контроля (активного или плацебо) частота развития острого панкреатита составила 0,1 случай на 100 пациенто-лет лечения в каждой группе (см. раздел "Особые указания. Панкреатит"). Клинически значимых отклонений показателей жизненно важных функций или ЭКГ (включая длительность интервала QTc) на фоне комбинированной терапии ситаглиптином и метформином не наблюдали. Нежелательные реакции, обусловленные применением ситаглиптинаУ пациентов не наблюдалось нежелательных реакций, обусловленных приемом ситаглиптина, частота которых составила 1%. Нежелательные реакции, обусловленные применением метформина. Нежелательными реакциями, наблюдавшимися в группе метформина у >:5% пациентов и чаще, чем в группе с плацебо, являются диарея, тошнота/рвота, метеоризм, астения, диспепсия, дискомфорт в области живота и головная боль. Пострегистрационные наблюденияВ ходе пострегистрационного мониторинга применения препарата или ситаглиптина, входящего в его состав, в монотерапии и/или в комбинированной терапии с другими гипогликемическими средствами были выявлены дополнительные нежелательные явления. Поскольку эти данные были получены добровольно от популяции неопределенного размера, частоту и причинно-следственную связь данных нежелательных явлений с терапией определить невозможно. К ним относятся: реакции гиперчувствительности, в том числе анафилаксия: ангионевротический отек: кожная сыпь: крапивница: кожный васкулит: эксфолиативные кожные заболевания, включая синдром Стивенса-Джонсона: острый панкреатит, включая геморрагическую и некротическую формы с летальным и без летального исхода: ухудшение функции почек, включая острую почечную недостаточность (иногда требуется диализ): инфекции верхних дыхательных путей: назофарингит: запор: рвота: головная боль: артралгия: миалгия: боль в конечности: боль в спине: зуд. Изменения лабораторных показателей. Ситаглиптин. Частота отклонений лабораторных показателей в группах лечения ситаглиптином и метформином была сравнимой с частотой в группах лечения плацебо и метформином. В большинстве, но не во всех клинических исследованиях отмечали небольшое увеличение содержания лейкоцитов (приблизительно на 200/мкл по сравнению с плацебо, среднее содержание в начале лечения 6600/мкл), обусловленное увеличением количества нейтрофилов. Данное изменение не рассматривается как клинически значимое. МетформинВ контролируемых клинических исследованиях метформина продолжительностью 29 недель отмечали снижение нормальной концентрации цианокобаламина (витамина В12) до субнормальных значений в сыворотке крови примерно у 7% пациентов, без клинических проявлений. Подобное снижение, обусловленное избирательным нарушением всасывания витамина В12 (а именно, нарушением формирования комплекса с внутренним фактором Касла, необходимого для всасывания витамина В12), очень редко приводит к развитию анемии и легко корректируется отменой метформина или дополнительным приемом витамина В12 (см. раздел "Особые указания. Метформин"). Передозировка: Ситаглиптин. Во время клинических исследований у здоровых добровольцах однократный прием ситаглиптина в дозе до 800 мг в целом хорошо переносился. Минимальные изменения интервала QT, не считающиеся клинически значимыми, отмечались в одном из исследований ситаглиптина в суточной дозе 800 мг (см. Фармакодинамика, Влияние на электрофизиологию сердца). Доза свыше 800 мг в сутки у людей не изучалась.В клинических исследованиях многократного приема препарата (I фазы) каких-либо связанных с лечением ситаглиптином побочных реакций при приеме препарата в суточной дозе до 400 мг на протяжении 28 дней не отмечали.В случае передозировки необходимо начать стандартные поддерживающие мероприятия: удаление еще невсосавшегося препарата из ЖКТ, мониторирование показателей жизнедеятельности, включая ЭКГ, а также назначение симптоматической терапии при необходимости. Ситаглиптин слабо диализируется: по данным клинических исследований в течение 3-4 часового сеанса диализа выводилось только 13,5 % дозы. В случае клинической необходимости назначают пролонгированный гемодиализ. Данных об эффективности перитонеального диализа ситаглиптина нет. Метформин. Имели место случаи передозировки метформина, включая прием в количествах, превышающих 50 г (50 000 мг). Гипогликемию наблюдали примерно в 10 % всех случаев передозировки, однако четкая связь с передозировкой метформина не была установлена. Развитие лактоацидоза сопровождало примерно 32 % всех случаев передозировки метформина (см. "Особые указания", Метформин). Возможно экстренное проведение гемодиализа (метформин диализируется со скоростью до 170 мл/мин в условиях хорошей гемодинамики) для ускоренного выведения избытка метформина при подозрении на его передозировку. Взаимодействие с другими ЛС: Ситаглиптин и метформин. Одновременный прием многократных доз ситаглиптина (по 50 мг 2 раза в стуки) и метформина (по 1000 мг 2 раза в сутки) не сопровождался значимыми изменениями фармакокинетических параметров ситаглиптина или метформина у больных сахарным диабетом 2 типа. Исследований межлекарственного влияния на фармакокинетические параметры препарата не проводили, однако проведено достаточное количество подобных исследований по каждому из компонентов препарата, ситаглиптину и метформину. СитаглиптинВ исследованиях по взаимодействию с другими лекарственными средствами, ситаглиптин не оказывал клинически значимого влияния на фармакокинетику следующих препаратов: метформина, росиглитазона, глибенкламида, симвастатина, варфарина, пероральных контрацептивов. Основываясь на этих данных, ситаглиптин не ингибирует изоферменты CYP системы цитохрома CYP3A4, 2С8 или 2С9. Данные in vitro свидетельствуют, что ситаглиптин также не подавляет изоферменты CYP2D6, 1А2, 2С19 и 2В6 и не индуцирует CYP3A4. По данным популяционного фармакокинетического анализа больных сахарным диабетом 2 типа сопутствующая терапия не оказывала клинически значимого влияния на фармакокинетику ситаглиптина. В исследовании оценивали ряд препаратов, наиболее часто используемых больными сахарным диабетом 2 типа, в том числе: гипохолестеринемические препараты (статины, фибраты, эзетимиб), антиагреганты (клопидогрел), гипотензивные препараты (ингибиторы АПФ, антагонисты рецепторов ангитензина II, бета-адреноблокаторы, блокаторы "медленных" кальциевых каналов, гидрохлоротиазид, анальгетики и нестероидные противовоспалительные препараты (напроксен, диклофенак, целекоксиб), антидепрессанты (бупропион, флуоксетин, сертралин), антигистаминные (цетиризин), ингибиторы протонной помпы (омепразол, лансопразол) и препараты для лечения эректильной дисфункции (силденафил). Отмечали увеличение AUC (11 %), а также средней Сmax (18 %) дигоксина при совместном применении с ситаглиптином. Это увеличение не считается клинически значимым, однако при одновременном приеме дигоксина рекомендуется наблюдение за пациентом. Отмечали увеличение AUC и Сmax ситаглиптина на 29 % и 68 %, соответственно, при совместном однократном пероральном приеме препарата ЯНУВИЯ™ в дозе 100 мг и циклоспорина (мощного ингибитора р-гликопротеина) в дозе 600 мг. Указанные изменения фармакокинетических параметров ситаглиптина не являются клинически значимыми. Метформин. Глибурид: в исследовании межлекарственного взаимодействия однократных доз метформина и глибурида у больных сахарным диабетом 2 типа не наблюдали каких-либо изменений фармакокинетических и фармакодинамических параметров метформина. Изменения значений AUC и Сmax глибурида были высоковариабельны. Недостаточная информация (однократный прием) и несоответствие плазменной концентрации глибурида наблюдаемым фармакодинамическим эффектам ставят под вопрос клиническую значимость этого взаимодействия. Фуросемид: в исследовании межлекарственного взаимодействия однократных доз метформина и фуросемида у здоровых добровольцев наблюдали изменение фармакокинетических параметров обоих препаратов. Фуросемид увеличивал значение концентрации Сmax метформина в плазме и цельной крови на 22 %, значение AUC метформина в цельной крови на 15 %, не изменяя при этом почечный клиренс препарата. Значения Сmax и AUC фуросемида, в свою очередь, снизились на 31 % и 12 %, соответственно, а период полувыведения снизился на 32 %, без существенных изменений почечного клиренса фуросемида. Информации о межлекарственном взаимодействии двух препаратов при длительном совместном применении нет. Нифедипин: при исследовании межлекарственного взаимодействия нифедипина и метформина после однократного приема препаратов здоровыми добровольцами выявили увеличение плазменных Сmax и AUC метформина на 20 % и 9 %, соответственно, а также увеличение количества выделяемого почками метформина. Тmax и период полувыведения метформина не изменились. В основе - увеличение абсорбции метформина в присутствии нифедипина. Влияние метформина на фармакокинетику нифедипина минимально. Катионные препараты: катионные препараты (т.е. амилорид, дигоксин, морфин, прокаинамид, хинидин, хинин, ранитидин, триамтерен, триметоприм или ванкомицин), выделяемые путем канальцевой секреции, теоретически могут вступить во взаимодействие с метформином, конкурируя за совместно используемую почечную канальцевую транспортную систему. Подобную конкуренцию наблюдали при одновременном приеме метформина и циметидина здоровыми добровольцами в исследованиях однократных и многократных доз, с 60 % увеличением концентрации Сmax метформина в плазме и цельной крови и 40 % увеличением значения AUC метформина в плазме и цельной крови. В исследовании однократных доз период полувыведения метформина не изменялся. Метформин не влиял на фармакокинетику циметидина. И хотя указанные межлекарственные взаимодействия имеют, в основном, теоретическое значение (за исключением циметидина), рекомендуется тщательное наблюдение за пациентом и коррекция дозы препарата и/или вышеуказанных катионных препаратов, экскретируемых проксимальными отделами почечных канальцев, в случаях их одновременного приема. Другие: некоторые препараты обладают гипергликемическим потенциалом и могут вмешаться в налаженный контроль над гликемией. К ним относятся тиазидные и другие диуретики, глюкокортикостероиды, фенотиазины, препараты щитовидной железы, эстрогены, пероральные контрацептивы, фенитоин, никотиновая кислота, симпатомиметики, блокаторы "медленных" кальциевых каналов и изониазид. При назначении перечисленных препаратов пациенту, получающему препарат, рекомендуется тщательное наблюдение за параметрами гликемического контроля. При одновременном приеме здоровыми добровольцами метформина и пропранолола или метформина и ибупрофена не наблюдали изменения фармакокинетических параметров этих препаратов. Лишь незначительная пропорция метформина связывается с белками плазмы, следовательно, межлекарственные взаимодействия метформина с препаратами, активно связывающимися с белками плазмы (салицилатами, сульфаниламидами, хлорамфениколом и пробенецидом), маловероятны, в отличие от производных сульфонилмочевины, которые также активно связываются с белками плазмы. Фармакологическое действие и фармакокинетика Препарат представляет собой комбинацию двух гипогликемических препаратов с взаимодополняющим (комплементарным) механизмом действия, предназначенную для улучшения контроля гликемии у больных сахарным диабетом 2 типа: ситаглиптина, ингибитора фермента дипептидилпептидазы-4 (ДПП-4), и метформина, представителя класса бигуанидов. Ситаглиптин является активным при пероральном приеме, высоко селективным ингибитором ДПП-4, предназначенным для лечения сахарного диабета 2 типа. Фармакологические эффекты класса препаратов-ингибиторов ДПП-4 опосредованы активацией инкретинов. Ингибируя ДПП-4, ситаглиптин повышает концентрацию двух известных активных гормонов семейства инкретинов: глюкагоно-подобного пептида 1 (ГПП-1) и глюкозо-зависимого инсулинотропного полипептида (ГИП). Инкретины являются частью внутренней физиологической системы регуляции гомеостаза глюкозы. При нормальной или повышенной концентрации глюкозы крови ГПП-1 и ГИП способствуют увеличению синтеза и секреции инсулина бета-клетками поджелудочной железы. ГПП-1 также подавляет секрецию глюкагона альфа-клетками поджелудочной железы, снижая, т.о, синтез глюкозы в печени. Этот механизм действия отличается от механизма действия производных сульфонилмочевины, которые стимулируют высвобождение инсулина и при низких концентрациях глюкозы крови, что чревато развитием сульфонил-индуцированной гипогликемии не только у больных сахарным диабетом 2 типа, но и у здоровых лиц. Будучи высокоселективным и эффективным ингибитором фермента ДШ1-4, ситаглиптин в терапевтических концентрациях не подавляет активности родственных ферментов ДПП-8 или ДПП-9. Ситаглиптин отличается по химической структуре и фармакологическому действию от аналогов ГПП-1, инсулина, производных сульфонилмочевины или меглитинидов, бигуанидов, агонистов гамма-рецепторов, активируемых пролифератором пероксисом (PPARy), ингибиторов альфа-гликозидазы и аналогов амилина. Метформин. Метформин является гипогликемическим препаратом, повышающим толерантность к глюкозе у больных сахарным диабетом 2 типа, снижая базальную и постпрандиальную концентрацию глюкозы в крови. Его фармакологические механизмы действия отличаются от механизмов действия пероральных гипогликемических препаратов других классов. Метформин снижает синтез глюкозы в печени, снижает всасывание глюкозы в кишечнике и повышает чувствительность к инсулину путем усиления периферического захвата и утилизации глюкозы. В отличие от производных сульфонилмочевины метформин не вызывает гипогликемии ни у больных сахарным диабетом 2 типа, ни у здоровых людей (за исключением некоторых обстоятельств, см. "С осторожностью", Метформин) и не вызывает гиперинсулинемии. Во время лечения метформином секреция инсулина не изменяется, при этом концентрация инсулина натощак и суточное значение плазменной концентрации инсулина могут снизиться. Пероральный прием одной дозы ситаглиптина больными сахарным диабетом 2 типа приводит к подавлению активности фермента ДПП-4 на 24 ч, что сопровождается двух-трехкратным увеличением концентрации циркулирующих активных ГПП-1 и ГИП, увеличением плазменной концентрации инсулина и С-пептида, снижением концентрации глюкагона и плазменной концентрации глюкозы натощак, а также уменьшением амплитуды колебаний гликемии после глюкозной или пищевой нагрузки. Прием ситаглиптина в суточной дозе 100 мг в течение 4-6 месяцев значительно улучшал функцию бета-клеток поджелудочной железы у больных сахарным диабетом 2 типа, о чем свидетельствовали соответствующие изменения таких маркеров, как НОМА-β (оценка гомеостаза в модели-β), соотношение проинсулин/инсулин, оценка реакции бета-клеток поджелудочной железы по данным панели повторных тестов на толерантность к пище. По данным клинических исследований II и III фазы эффективность гликемического контроля ситаглиптина в режиме, 50 мг х 2 раза в сутки была сопоставимой с эффективностью режима 100 мг один раз в сутки.В рандомизированном плацебо-контролируемом двойном слепом с двойной иммитацией 4-периодном перекрестном исследовании у здоровых добровольцев изучали влияние ситаглиптина в комбинации с метформином, либо только ситаглиптина, либо только метформина, либо плацебо на изменение плазменных концентраций активного и общего ГПП-1 и глюкозы после приема пищи. Средневзвешенные значения концентрации активного ГПП-1 через 4 ч после приема пищи увеличивались примерно в 2 раза после приема только ситаглиптина или только метформина в сравнении с плацебо. Сочетанный прием ситаглиптина и метформина оебспечивал суммирование эффекта с 4-кратным увеличением концентрации активного ГПП-1 по сравнению с динамикой в группе плацебо. Прием только ситаглиптина сопровождался увеличением концентрации только активного ГПП-1 вследствие ингибирования фермента ДПП-4, в то время как прием только метформина сопровождался симметричным увеличением концентрации общего и активного ГПП-1. Полученные данные отражают различные механизмы в основе увеличения концентрации активного ГПП-1 после приема этих двух препаратов. Результаты исследования также продемонстрировали, что именно ситаглиптин, а не метформин обеспечивает прирост концентрации активного ГПП-1.В исследованиях у здоровых добровольцев прием ситаглиптина не сопровождался снижением концентрации глюкозы и не вызывал гипогликемии, что подтверждает глюкозо-зависимый характер инсулинотропного действия и подавления си
Модель:
RUR 2849
Показания Монотерапия Препарат показан в качестве стартовой терапии больным сахарным диабетом 2 типа для улучшения контроля над гликемией, если соблюдение диеты и режима физических нагрузок не позволяют добиться адекватного контроля. Препарат показан в качестве дополнения к диете и режиму физических нагрузок для улучшения контроля над гликемией у больных сахарным диабетом 2 типа, не достигших адекватного контроля на фоне монотерапии метформином или ситаглиптином, либо после неуспешного комбинированного лечения двумя препаратами. Комбинированная терапия Препарат показан пациентам с сахарным диабетом 2 типа для улучшения контроля гликемии в комбинации с производными сульфонилмочевины (тройная комбинация: метформин + ситаглиптин + производное сульфонилмочевины), когда диета и режим физических нагрузок в сочетание с двумя из этих трех препаратов: метформин, ситаглиптин или производные сульфонилмочевины не приводят к адекватному гликемическому контролю. Препарат показан пациентам с сахарным диабетом 2 типа для улучшения контроля гликемии в комбинации с тиазолидиндионами (агонистами PPARγ -рецепторов, активируемых пролифератором пероксисом), когда диета и режим физических нагрузок в сочетание с двумя из трех этих препаратов: метформин, ситаглиптин или тиазолидиндион не приводят к адекватному гликемическому контролю. Препарат показан пациентам с сахарным диабетом 2 типа для улучшения контроля гликемии в комбинации с инсулином, когда диета и режим физических нагрузок в сочетание с инсулином не приводят к адекватному гликемическому контролю. Противопоказания Противопоказания - известная повышенная чувствительность к ситаглиптину, метформину или какому-либо из компонентов препарата - сахарный диабет 1 типа- заболевание почек или снижение функции почек (при концентрации креатинина сыворотки 1,5 мг/дл и 1,4 мг/дл у мужчин и женщин, соответственно, или снижении клиренса креатинина (<: 60 мл/мин), в том числе вследствие сердечно-сосудистого коллапса (шока), острого инфаркта миокарда или септицемии- острые состояния, протекающие с риском развития нарушений функции почек- дегидратация (при диарее, рвоте), лихорадка, тяжёлые инфекционные заболевания- состояния гипоксии (шок, сепсис, почечные инфекции, бронхо-легочные заболевания)- острый или хронический метаболический ацидоз, включая диабетический кетоацидоз (с комой или без)- клинически выраженные проявления острых и хронических заболеваний, которые могут приводить к развитию тканевой гипоксии (в том числе, сердечная или дыхательная недостаточность, острый инфаркт миокарда)- обширные хирургические операции и травмы, когда показано проведение инсулинотерапии (см. раздел "Особые указания")- печеночная недостаточность, нарушение функции печени- хронический алкоголизм, острое отравление алкоголем- беременность, период грудного вскармливания- лактоацидоз (в т.ч. и в анамнезе)- применение в течение не менее 48 ч. до и в течение 48 ч. после проведения радиоизотопных или рентгенологических исследований с введением йодсодержащего контрастного вещества (см. раздел "Взаимодействие с другими лекарственными средствами")- соблюдение гипокалорийной диеты (менее 1000 ккал/сут)- детский возраст до 18 лет. С осторожностью: Применение у пожилых Поскольку основным путем выведения ситаглиптина и метформина являются почки, и поскольку с возрастом выделительная функция почек снижается, меры предосторожности при назначении препарата нарастают пропорционально возрасту. Пожилым пациентам проводят тщательный подбор дозы и регулярный контроль функции почек (см. "Особые указания", Мониторинг функции почек). Ситаглиптин. По данным клинических исследований эффективность и безопасность ситаглиптина у пожилых (>:65 лет) пациентов была сравнима с эффективностью и безопасностью у молодых (<:65 лет). Метформин. Число пожилых пациентов среди участников контролируемых исследований метформина было недостаточным для вынесения формального заключения о возрастных различиях в эффективности и безопасности препарата, хотя по имеющимся данным таких различий не наблюдали. Поскольку метформин выводится преимущественно почками, и при их нарушенной функции возрастает вероятность побочных реакций, препарат следует назначать только пациентам с подтвержденной нормальной функцией почек (см. "Противопоказания"). Беременность Не проводилось адекватно контролируемых исследований препарата или его компонентов у беременных, следовательно, данных о безопасности его применения у беременных женщин нет. Препарат, как и другие пероральные гипогликемические препараты, не рекомендован к применению во время беременности. Не проводилось экспериментальных исследований комбинированного препарата для оценки его влияния на репродуктивную функцию. Приводятся только имеющиеся данные из исследований ситаглиптина и метформина. Ситаглиптин. Ситаглиптин не продемонстрировал тератогенности в период органогенеза при пероральном введении крысам в суточных дозах до 250 мг/кг или кроликам в дозах до 125 мг/кг (что преывшает плазменную экспозицию препарата у человека в 32 и 22 раза, соответственно, после приема рекомендованной суточной терапевтической дозы 100 мг). Отмечали незначительное увеличение частоты мальформации ребер у потомства (отсутствие, гипоплазия, искривление) при пероральном введении препарата в суточных дозах 1000 мг/кг (что превышает экспозицию у человека примерно в 100 раз после приема рекомендованной суточной дозы 100 мг). Незначительное снижение массы тела у обоих полов потомства крыс в период грудного вскармливания и снижение темпов прибавки в весе по окончании грудного вскармливания у самцов при пероральном введении беременным самкам препарата в суточной дозе 1000 мг/кг. Тем не менее, данные экспериментальнх репродуктивных исследований не всегда соотносятся напрямую с влиянием препарата на репродуктивную функцию человека. Метформин. Метформин не продемонстрировал тератогенности при пероральном введении крысам в суточных дозах до 600 мг/кг. Это преывшает плазменную экспозицию препарата у человека в 2 и 6 раз (у крыс и кроликов, соответственно) после приема максимальной рекомендованной суточной терапевтической дозы 2000 мг. Значения плазменной концентрации препарата у плода свидетельствуют о частичном плацентарном переносе. Экспериментальные исследования по определению секреции компонентов комбинированного препарата в грудное молоко не проводились. По данным исследований по отдельным препаратам, как ситаглиптин, так и метформин секретируются в грудное молоко крыс. Данных о секреции ситаглиптина в грудное молоко человека нет. Следовательно, препарат не следует назначать в период лактации. Применение и дозы Общая информация: Режим дозирования препарата должен подбираться индивидуально, исходя из текущей терапии, эффективности и переносимости, но не превышая максимальную рекомендуемую суточную дозу ситаглиптина 100 мг. Препарат обычно назначают в режиме 2 раза в день во время еды, с постепенным увеличением дозы, с целью минимизации возможных побочных эффектов со стороны желудочно-кишечного тракта (ЖКТ), характерных для метформина. Рекомендации по дозированию:Начальная доза препарата зависит от текущей гипогликемической терапии. Препарат принимают 2 раза в день во время еды. Предлагаются следующие дозировки препарата:500 мг метформина / 50 мг ситаглиптина 850 мг метформина / 50 мг ситаглиптина 1000 мг метформина / 50 мг ситаглиптина Стартовая терапия:Больным сахарным диабетом 2 типа с неадекватным гликемическим контролем на фоне соблюдения диеты и режима физических нагрузок рекомендуемая стартовая доза препарата составляет 500 мг метформина / 50 мг ситаглиптина 2 раза в день. Впоследствии дозу можно увеличить до 1000 мг метформина / 50 мг ситаглиптина 2 раза в день. Для пациентов, не достигших адекватного контроля на монотерапии метформином:Рекомендуемая стартовая доза препарата для пациентов, не достигших адекватного контроля на монотерапии метформином должна обеспечить рекомендуемую терапевтическую суточную дозу ситаглиптина 100 мг, т.е. по 50 мг ситаглиптина 2 раза в день плюс текущая доза метформина. Для пациентов, не достигших адекватного контроля на монотерапии ситаглиптином:Рекомендуемая стартовая доза препарата для пациентов, не достигших адекватного контроля на монотерапии ситаглиптином, составляет 500 мг метформина / 50 мг ситаглиптина 2 раза в день. В дальнейшем доза может бытьувеличена до 1000 мг метформина / 50 мг ситаглиптина 2 раза в день. Пациентам, принимающим скорректированную ввиду почечной недостаточности дозу ситаглиптина, лечение препаратом противопоказано (см. "Противопоказания"). Для пациентов, принимающих комбинацию препаратов ситаглиптин и метформин: При переходе с комбинированного лечения ситаглиптином и метформином стартовая доза препарата может быть эквивалентной дозам принимаемых по отдельности ситаглиптина и метформина. Для пациентов, принимающих два из перечисленных трех гипогликемических препаратов - ситаглиптин, метформин или производные сулъфонилмочевины: Стартовая доза препарата должна обеспечить рекомендуемую терапевтическую суточную дозу ситаглиптина 100 мг, т.е. по 50 мг ситаглиптина 2 раза в день. Стартовую дозу метформина определяют исходя из уровня гликемического контроля и текущей (если пациент принимает этот препарат) дозы метформина. Увеличение дозы метформина должно быть постепенным для минимизации связанных с ним побочных эффектов со стороны ЖКТ. Пациентам, принимающим производное сулъфонилмочевины, будет рациональным снизить текущую дозу для снижения риска сульфонил-индуцированной гипогликемии (см. "Особые указания"). Для пациентов, принимающих два из перечисленных трех гипогликемических препаратов - ситаглиптин, метформин или агонисты PPARγ - рецепторов (тиазолидиндионы):Стартовая доза препарата должна соответствовать суточной дозе ситаглиптина 100 мг, т.е. по 50 мг ситаглиптина 2 раза в день и ранее принимаемой дозе метформина. В случае необходимости увеличения дозы метформина рекомендована постепенная титрация препарата для избежания гастроинтенстинальных побочных эффектов. Для пациентов, принимающих два из перечисленных трех гипогликемических препаратов - ситаглиптин, метформин или инсулин:Стартовая доза препарата должна соответствовать суточной дозе ситаглиптина 100 мг, т.е. по 50 мг ситаглиптина 2 раза в день и ранее принимаемой дозе метформина. В случае необходимости увеличения дозы метформина рекомендована постепенная титрация препарата для избежания гастро-интенстинальных побочных эффектов. Пациентам может потребоваться снижение дозы инсулина для предотвращения риска гипогликемии (см. "Особые указания"). Специальных исследований по оценке безопасности и эффективности перехода с лечения другими гипогликемическими препаратами на лечение комбинированным препаратом не проводилось. Любые изменения в лечении сахарного диабета 2 типа должны проводиться с осторожностью и под контролем соответствующих параметров с учетом возможных изменений гликемического контроля. Применение у детей. Безопасность препарата у детей и подростков моложе 18 лет не изучалась. Побочные эффекты и передозировка Побочные эффекты: В плацебо-контролируемых исследованиях комбинированное лечение ситаглиптином и метформином в целом хорошо переносилось пациентами с сахарным диабетом 2 типа. Частота побочных эффектов при комбинированном лечении ситаглиптином и метформином была сравнимой с частотой при приеме метформина в комбинации с плацебо. Комбинированное лечение ситаглинтином и метформином. Стартовая теpaпияВ 24-недельном плацебо-контролируемом факториальном исследовании начальной комбинированной терапии ситаглиптином и метформином (ситаглиптин 50 мг +метформин 500 мг или 1000 мг х 2 раза в сутки) в группе комбинированной терапии по сравнению с группами монотерапииметформином (500 мг или 1000 мг х 2 раза в сутки), ситаглиптином (100 мг 1 раз в сутки) или плацебо наблюдались следующие связанные с приемом препарата нежелательные реакции, наблюдавшиеся с частотой 1% в группе комбинированного лечения и чаще, чем в группе плацебо: диарея (ситаглиптин + метформин - 3,5%, метформин - 3,3%, ситаглиптин - 0,0%, плацебо -1,1 %), тошнота (1,6%, 2.5%, 0,0% и 0,6%), диспепсия (1,3%, 1,1%. 0,0% и 0,0%), метеоризм (1,3%, 0,5%, 0,0% и 0,0%), рвота (1,1%. 0,3%. 0,0% и 0,0%), головная боль (1,3%, 1,1%, 0,6% и 0,0%) и гипогликемия (1,1%, 0,5%, 0,6% и 0,0%). Добавление ситаглиптина к текущей терапии метформином В 24-недельном плацебо-контролируемом исследовании при добавлении ситаглиптииа в дозе 100 мг/сут к текущему лечению метформином единственной нежелательной реакцией, связанной с приемом препарата и наблюдавшейся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо, была тошнота (ситаглиптин + метформин - 1,1%, плацебо + метформин - 0,4%). Гиногликемия и нежелательные реакции со стороны ЖКТВ плацебо-контролируемых исследованиях комбинированного лечения ситаглиптином и метформином частота развития гипогликемии (независимо от причинно-следственной связи) в группах комбинированной терапии была сопоставимой с частотой в группах лечения метформином в сочетании с плацебо (1,3-1,6% и 2,1% соответственно). Частота отслеживаемых нежелательных реакций со стороны ЖКТ (независимо от причинно-следственной связи) в группах комбинированного лечения ситаглиптином и метформином была сопоставимой с частотой в группах монотерапии метформином: диарея (ситаглиптин +метформин - 7,5%, метформин - 7,7%), тошнота (4,8%, 5,5%), рвота (2,1%. 0,5%), боль в животе (3,0%, 3,8%). Во всех исследованиях нежелательные реакции в виде гипогликемии регистрировались на основании всех сообщений о клинически выраженных симптомах гипогликемии: дополнительное измерение концентрации глюкозы в крови не требовалось. Комбинированное лечение ситаглиптином, метформином и производным сульфонилмочевиныВ 24-недельном плацебо-контролируемом исследовании с применением ситаглиптина в дозе 100 мг/сут на фоне текущего комбинированного лечения глимепиридом в дозе 4 мг/сут и метформином в дозе 1500 мг/сут наблюдались следующие связанные с приемом препарата нежелательные реакции, наблюдавшиеся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо: гипогликемия (ситаглиптин - 13,8%, плацебо - 0,9%), запор (1,7% и 0,0%). Комбинированное лечение ситаглиптином, метформином и агонистом PPARγ По данным плацебо-контролируемого исследования с применением ситаглиптина в дозе 100 мг/сут на фоне текущего комбинированного лечения росиглитазоном и метформином на 18 неделе лечения наблюдались следующие связанные с приемом препарата нежелательные реакции, наблюдавшиеся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо: головная боль (ситаглиптин - 2,4%, плацебо - 0,0%), диарея (1,8%, 1,1%), тошнота (1,2%, 1,1%), гипогликемия (1,2%. 0,0%), рвота (1,2%, 0.0%). На 54 неделе комбинированного лечения наблюдались следующие связанные с приемом препарата нежелательные реакции, наблюдавшиеся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо: головная боль (ситаглиптин -2,4%, плацебо - 0,0%), гипогликемия (2.4%, 0,0%), инфекции верхних дыхательных путей (1,8%, 0,0%), тошнота (1,2%, 1,1 %), кашель (1,2%. 0,0%), грибковые инфекции кожи (1,2%, 0,0%), периферические отеки (1,2%. 0,0%), рвота (1,2%, 0,0%). Комбинированное лечение ситаглиптином, метформином и инсулиномВ 24-недельном плацебо-контролируемом исследовании с применением ситаглиптина в дозе 100 мг/сут на фоне текущегокомбинированного лечения метформином в дозе 1500 мг/сут и постоянной дозы инсулина единственной нежелательной реакцией, связанной с приемом препарата и наблюдавшейся с частотой 1% в группе лечения с ситаглиптином и чаще, чем в группе с плацебо, была гипогликемия (ситаглиптин - 10,9%, плацебо - 5,2%). В другом 24-недельном исследовании, в котором пациенты получали ситаглиптин в качестве дополнительной терапии к терапии инсулином (с или без метформина), единственной нежелательной реакцией, наблюдавшейся с частотой 1% в группе лечения ситаглиптином и метформином, и чаще чем в группе плацебо и метформина, была рвота (ситаглиптин и метформин -1,1%, плацебо и метформин - 0,4%). ПанкреатитВ обобщенном анализе 19 двойных-слепых рандомизированных клинических исследований применения ситаглиптина (в дозе 100 мг/сут) или соответствующего препарата контроля (активного или плацебо) частота развития острого панкреатита составила 0,1 случай на 100 пациенто-лет лечения в каждой группе (см. раздел "Особые указания. Панкреатит"). Клинически значимых отклонений показателей жизненно важных функций или ЭКГ (включая длительность интервала QTc) на фоне комбинированной терапии ситаглиптином и метформином не наблюдали. Нежелательные реакции, обусловленные применением ситаглиптинаУ пациентов не наблюдалось нежелательных реакций, обусловленных приемом ситаглиптина, частота которых составила 1%. Нежелательные реакции, обусловленные применением метформина. Нежелательными реакциями, наблюдавшимися в группе метформина у >:5% пациентов и чаще, чем в группе с плацебо, являются диарея, тошнота/рвота, метеоризм, астения, диспепсия, дискомфорт в области живота и головная боль. Пострегистрационные наблюденияВ ходе пострегистрационного мониторинга применения препарата или ситаглиптина, входящего в его состав, в монотерапии и/или в комбинированной терапии с другими гипогликемическими средствами были выявлены дополнительные нежелательные явления. Поскольку эти данные были получены добровольно от популяции неопределенного размера, частоту и причинно-следственную связь данных нежелательных явлений с терапией определить невозможно. К ним относятся: реакции гиперчувствительности, в том числе анафилаксия: ангионевротический отек: кожная сыпь: крапивница: кожный васкулит: эксфолиативные кожные заболевания, включая синдром Стивенса-Джонсона: острый панкреатит, включая геморрагическую и некротическую формы с летальным и без летального исхода: ухудшение функции почек, включая острую почечную недостаточность (иногда требуется диализ): инфекции верхних дыхательных путей: назофарингит: запор: рвота: головная боль: артралгия: миалгия: боль в конечности: боль в спине: зуд. Изменения лабораторных показателей. Ситаглиптин. Частота отклонений лабораторных показателей в группах лечения ситаглиптином и метформином была сравнимой с частотой в группах лечения плацебо и метформином. В большинстве, но не во всех клинических исследованиях отмечали небольшое увеличение содержания лейкоцитов (приблизительно на 200/мкл по сравнению с плацебо, среднее содержание в начале лечения 6600/мкл), обусловленное увеличением количества нейтрофилов. Данное изменение не рассматривается как клинически значимое. МетформинВ контролируемых клинических исследованиях метформина продолжительностью 29 недель отмечали снижение нормальной концентрации цианокобаламина (витамина В12) до субнормальных значений в сыворотке крови примерно у 7% пациентов, без клинических проявлений. Подобное снижение, обусловленное избирательным нарушением всасывания витамина В12 (а именно, нарушением формирования комплекса с внутренним фактором Касла, необходимого для всасывания витамина В12), очень редко приводит к развитию анемии и легко корректируется отменой метформина или дополнительным приемом витамина В12 (см. раздел "Особые указания. Метформин"). Передозировка: Ситаглиптин. Во время клинических исследований у здоровых добровольцах однократный прием ситаглиптина в дозе до 800 мг в целом хорошо переносился. Минимальные изменения интервала QT, не считающиеся клинически значимыми, отмечались в одном из исследований ситаглиптина в суточной дозе 800 мг (см. Фармакодинамика, Влияние на электрофизиологию сердца). Доза свыше 800 мг в сутки у людей не изучалась.В клинических исследованиях многократного приема препарата (I фазы) каких-либо связанных с лечением ситаглиптином побочных реакций при приеме препарата в суточной дозе до 400 мг на протяжении 28 дней не отмечали.В случае передозировки необходимо начать стандартные поддерживающие мероприятия: удаление еще невсосавшегося препарата из ЖКТ, мониторирование показателей жизнедеятельности, включая ЭКГ, а также назначение симптоматической терапии при необходимости. Ситаглиптин слабо диализируется: по данным клинических исследований в течение 3-4 часового сеанса диализа выводилось только 13,5 % дозы. В случае клинической необходимости назначают пролонгированный гемодиализ. Данных об эффективности перитонеального диализа ситаглиптина нет. Метформин. Имели место случаи передозировки метформина, включая прием в количествах, превышающих 50 г (50 000 мг). Гипогликемию наблюдали примерно в 10 % всех случаев передозировки, однако четкая связь с передозировкой метформина не была установлена. Развитие лактоацидоза сопровождало примерно 32 % всех случаев передозировки метформина (см. "Особые указания", Метформин). Возможно экстренное проведение гемодиализа (метформин диализируется со скоростью до 170 мл/мин в условиях хорошей гемодинамики) для ускоренного выведения избытка метформина при подозрении на его передозировку. Взаимодействие с другими ЛС: Ситаглиптин и метформин. Одновременный прием многократных доз ситаглиптина (по 50 мг 2 раза в стуки) и метформина (по 1000 мг 2 раза в сутки) не сопровождался значимыми изменениями фармакокинетических параметров ситаглиптина или метформина у больных сахарным диабетом 2 типа. Исследований межлекарственного влияния на фармакокинетические параметры препарата не проводили, однако проведено достаточное количество подобных исследований по каждому из компонентов препарата, ситаглиптину и метформину. СитаглиптинВ исследованиях по взаимодействию с другими лекарственными средствами, ситаглиптин не оказывал клинически значимого влияния на фармакокинетику следующих препаратов: метформина, росиглитазона, глибенкламида, симвастатина, варфарина, пероральных контрацептивов. Основываясь на этих данных, ситаглиптин не ингибирует изоферменты CYP системы цитохрома CYP3A4, 2С8 или 2С9. Данные in vitro свидетельствуют, что ситаглиптин также не подавляет изоферменты CYP2D6, 1А2, 2С19 и 2В6 и не индуцирует CYP3A4. По данным популяционного фармакокинетического анализа больных сахарным диабетом 2 типа сопутствующая терапия не оказывала клинически значимого влияния на фармакокинетику ситаглиптина. В исследовании оценивали ряд препаратов, наиболее часто используемых больными сахарным диабетом 2 типа, в том числе: гипохолестеринемические препараты (статины, фибраты, эзетимиб), антиагреганты (клопидогрел), гипотензивные препараты (ингибиторы АПФ, антагонисты рецепторов ангитензина II, бета-адреноблокаторы, блокаторы "медленных" кальциевых каналов, гидрохлоротиазид, анальгетики и нестероидные противовоспалительные препараты (напроксен, диклофенак, целекоксиб), антидепрессанты (бупропион, флуоксетин, сертралин), антигистаминные (цетиризин), ингибиторы протонной помпы (омепразол, лансопразол) и препараты для лечения эректильной дисфункции (силденафил). Отмечали увеличение AUC (11 %), а также средней Сmax (18 %) дигоксина при совместном применении с ситаглиптином. Это увеличение не считается клинически значимым, однако при одновременном приеме дигоксина рекомендуется наблюдение за пациентом. Отмечали увеличение AUC и Сmax ситаглиптина на 29 % и 68 %, соответственно, при совместном однократном пероральном приеме препарата ЯНУВИЯ™ в дозе 100 мг и циклоспорина (мощного ингибитора р-гликопротеина) в дозе 600 мг. Указанные изменения фармакокинетических параметров ситаглиптина не являются клинически значимыми. Метформин. Глибурид: в исследовании межлекарственного взаимодействия однократных доз метформина и глибурида у больных сахарным диабетом 2 типа не наблюдали каких-либо изменений фармакокинетических и фармакодинамических параметров метформина. Изменения значений AUC и Сmax глибурида были высоковариабельны. Недостаточная информация (однократный прием) и несоответствие плазменной концентрации глибурида наблюдаемым фармакодинамическим эффектам ставят под вопрос клиническую значимость этого взаимодействия. Фуросемид: в исследовании межлекарственного взаимодействия однократных доз метформина и фуросемида у здоровых добровольцев наблюдали изменение фармакокинетических параметров обоих препаратов. Фуросемид увеличивал значение концентрации Сmax метформина в плазме и цельной крови на 22 %, значение AUC метформина в цельной крови на 15 %, не изменяя при этом почечный клиренс препарата. Значения Сmax и AUC фуросемида, в свою очередь, снизились на 31 % и 12 %, соответственно, а период полувыведения снизился на 32 %, без существенных изменений почечного клиренса фуросемида. Информации о межлекарственном взаимодействии двух препаратов при длительном совместном применении нет. Нифедипин: при исследовании межлекарственного взаимодействия нифедипина и метформина после однократного приема препаратов здоровыми добровольцами выявили увеличение плазменных Сmax и AUC метформина на 20 % и 9 %, соответственно, а также увеличение количества выделяемого почками метформина. Тmax и период полувыведения метформина не изменились. В основе - увеличение абсорбции метформина в присутствии нифедипина. Влияние метформина на фармакокинетику нифедипина минимально. Катионные препараты: катионные препараты (т.е. амилорид, дигоксин, морфин, прокаинамид, хинидин, хинин, ранитидин, триамтерен, триметоприм или ванкомицин), выделяемые путем канальцевой секреции, теоретически могут вступить во взаимодействие с метформином, конкурируя за совместно используемую почечную канальцевую транспортную систему. Подобную конкуренцию наблюдали при одновременном приеме метформина и циметидина здоровыми добровольцами в исследованиях однократных и многократных доз, с 60 % увеличением концентрации Сmax метформина в плазме и цельной крови и 40 % увеличением значения AUC метформина в плазме и цельной крови. В исследовании однократных доз период полувыведения метформина не изменялся. Метформин не влиял на фармакокинетику циметидина. И хотя указанные межлекарственные взаимодействия имеют, в основном, теоретическое значение (за исключением циметидина), рекомендуется тщательное наблюдение за пациентом и коррекция дозы препарата и/или вышеуказанных катионных препаратов, экскретируемых проксимальными отделами почечных канальцев, в случаях их одновременного приема. Другие: некоторые препараты обладают гипергликемическим потенциалом и могут вмешаться в налаженный контроль над гликемией. К ним относятся тиазидные и другие диуретики, глюкокортикостероиды, фенотиазины, препараты щитовидной железы, эстрогены, пероральные контрацептивы, фенитоин, никотиновая кислота, симпатомиметики, блокаторы "медленных" кальциевых каналов и изониазид. При назначении перечисленных препаратов пациенту, получающему препарат, рекомендуется тщательное наблюдение за параметрами гликемического контроля. При одновременном приеме здоровыми добровольцами метформина и пропранолола или метформина и ибупрофена не наблюдали изменения фармакокинетических параметров этих препаратов. Лишь незначительная пропорция метформина связывается с белками плазмы, следовательно, межлекарственные взаимодействия метформина с препаратами, активно связывающимися с белками плазмы (салицилатами, сульфаниламидами, хлорамфениколом и пробенецидом), маловероятны, в отличие от производных сульфонилмочевины, которые также активно связываются с белками плазмы. Фармакологическое действие и фармакокинетика Препарат представляет собой комбинацию двух гипогликемических препаратов с взаимодополняющим (комплементарным) механизмом действия, предназначенную для улучшения контроля гликемии у больных сахарным диабетом 2 типа: ситаглиптина, ингибитора фермента дипептидилпептидазы-4 (ДПП-4), и метформина, представителя класса бигуанидов. Ситаглиптин является активным при пероральном приеме, высоко селективным ингибитором ДПП-4, предназначенным для лечения сахарного диабета 2 типа. Фармакологические эффекты класса препаратов-ингибиторов ДПП-4 опосредованы активацией инкретинов. Ингибируя ДПП-4, ситаглиптин повышает концентрацию двух известных активных гормонов семейства инкретинов: глюкагоно-подобного пептида 1 (ГПП-1) и глюкозо-зависимого инсулинотропного полипептида (ГИП). Инкретины являются частью внутренней физиологической системы регуляции гомеостаза глюкозы. При нормальной или повышенной концентрации глюкозы крови ГПП-1 и ГИП способствуют увеличению синтеза и секреции инсулина бета-клетками поджелудочной железы. ГПП-1 также подавляет секрецию глюкагона альфа-клетками поджелудочной железы, снижая, т.о, синтез глюкозы в печени. Этот механизм действия отличается от механизма действия производных сульфонилмочевины, которые стимулируют высвобождение инсулина и при низких концентрациях глюкозы крови, что чревато развитием сульфонил-индуцированной гипогликемии не только у больных сахарным диабетом 2 типа, но и у здоровых лиц. Будучи высокоселективным и эффективным ингибитором фермента ДШ1-4, ситаглиптин в терапевтических концентрациях не подавляет активности родственных ферментов ДПП-8 или ДПП-9. Ситаглиптин отличается по химической структуре и фармакологическому действию от аналогов ГПП-1, инсулина, производных сульфонилмочевины или меглитинидов, бигуанидов, агонистов гамма-рецепторов, активируемых пролифератором пероксисом (PPARy), ингибиторов альфа-гликозидазы и аналогов амилина. Метформин. Метформин является гипогликемическим препаратом, повышающим толерантность к глюкозе у больных сахарным диабетом 2 типа, снижая базальную и постпрандиальную концентрацию глюкозы в крови. Его фармакологические механизмы действия отличаются от механизмов действия пероральных гипогликемических препаратов других классов. Метформин снижает синтез глюкозы в печени, снижает всасывание глюкозы в кишечнике и повышает чувствительность к инсулину путем усиления периферического захвата и утилизации глюкозы. В отличие от производных сульфонилмочевины метформин не вызывает гипогликемии ни у больных сахарным диабетом 2 типа, ни у здоровых людей (за исключением некоторых обстоятельств, см. "С осторожностью", Метформин) и не вызывает гиперинсулинемии. Во время лечения метформином секреция инсулина не изменяется, при этом концентрация инсулина натощак и суточное значение плазменной концентрации инсулина могут снизиться. Пероральный прием одной дозы ситаглиптина больными сахарным диабетом 2 типа приводит к подавлению активности фермента ДПП-4 на 24 ч, что сопровождается двух-трехкратным увеличением концентрации циркулирующих активных ГПП-1 и ГИП, увеличением плазменной концентрации инсулина и С-пептида, снижением концентрации глюкагона и плазменной концентрации глюкозы натощак, а также уменьшением амплитуды колебаний гликемии после глюкозной или пищевой нагрузки. Прием ситаглиптина в суточной дозе 100 мг в течение 4-6 месяцев значительно улучшал функцию бета-клеток поджелудочной железы у больных сахарным диабетом 2 типа, о чем свидетельствовали соответствующие изменения таких маркеров, как НОМА-β (оценка гомеостаза в модели-β), соотношение проинсулин/инсулин, оценка реакции бета-клеток поджелудочной железы по данным панели повторных тестов на толерантность к пище. По данным клинических исследований II и III фазы эффективность гликемического контроля ситаглиптина в режиме, 50 мг х 2 раза в сутки была сопоставимой с эффективностью режима 100 мг один раз в сутки.В рандомизированном плацебо-контролируемом двойном слепом с двойной иммитацией 4-периодном перекрестном исследовании у здоровых добровольцев изучали влияние ситаглиптина в комбинации с метформином, либо только ситаглиптина, либо только метформина, либо плацебо на изменение плазменных концентраций активного и общего ГПП-1 и глюкозы после приема пищи. Средневзвешенные значения концентрации активного ГПП-1 через 4 ч после приема пищи увеличивались примерно в 2 раза после приема только ситаглиптина или только метформина в сравнении с плацебо. Сочетанный прием ситаглиптина и метформина оебспечивал суммирование эффекта с 4-кратным увеличением концентрации активного ГПП-1 по сравнению с динамикой в группе плацебо. Прием только ситаглиптина сопровождался увеличением концентрации только активного ГПП-1 вследствие ингибирования фермента ДПП-4, в то время как прием только метформина сопровождался симметричным увеличением концентрации общего и активного ГПП-1. Полученные данные отражают различные механизмы в основе увеличения концентрации активного ГПП-1 после приема этих двух препаратов. Результаты исследования также продемонстрировали, что именно ситаглиптин, а не метформин обеспечивает прирост концентрации активного ГПП-1.В исследованиях у здоровых добровольцев прием ситаглиптина не сопровождался снижением концентрации глюкозы и не вызывал гипогликемии, что подтверждает глюкозо-зависимый характер инсулинотропного действия и подавления си
Модель:
RUR 0
Показания Взрослые: - Лечение опоясывающего герпеса (Herpes zoster) (препарат способствует купированию болевого синдрома, уменьшает его продолжительность и процент больных с болями, вызванными опоясывающим лишаем, включая острую и постгерпетическую невралгию). - Лечение инфекций кожи и слизистых оболочек, вызванных вирусом простого герпеса (ВПГ), включая впервые выявленный и рецидивирующий генитальный герпес (Herpes genitalis), а также лабиальный герпес (Herpes labialis). - Профилактика (супрессия) рецидивов инфекций кожи и слизистых оболочек, вызванных ВПГ, включая генитальный герпес. Профилактика передачи генитального герпеса здоровому партнеру при приеме в качестве супрессивной терапии в сочетании с безопасным сексом. Взрослые и подростки в возрасте от 12 лет и старше - Профилактика цитомегаловирусной (ЦМВ) инфекции, а также реакции острого отторжения трансплантата (у пациентов с трансплантатами почек). - Профилактика оппортунистических инфекций и других герпесвирусных инфекций (ВПГ, ВЗВ) после трансплантации органов. Противопоказания Противопоказания · Гиперчувствительность к валацикловиру, ацикловиру и любому вспомогательному компоненту, входящему в состав препарата. · Клинически выраженные формы ВИЧ-инфекции с содержанием CD4+ лимфоцитов менее 100/мкл. · Детский возраст (до 12 лет с целью профилактики цитомегаловирусной инфекции, до 18 лет - по остальным показаниям). С осторожностью: - почечная и печеночная недостаточность: - пожилой возраст: - гипогидратация: - одновременный прием нефротоксичных лекарственных средств: - беременность и период грудного вскармливания. Беременность Беременность. Данных о применении валацикловира при беременности недостаточно. Валацикловир Канон следует применять при беременности только в том случае, когда ожидаемый эффект терапии для материи превосходит потенциальный риск для плода. Данные регистрационных записей об исходе беременности у женщин, принимавших валацикловир, не показали увеличения числа врожденных дефектов у их детей по сравнению с общей популяцией. Поскольку в регистр включено небольшое количество женщин, принимавших валацикловир во время беременности, то достоверных и определенных заключений о безопасности валацикловира при беременности сделать нельзя. Период грудного вскармливания. Ацикловир, основной метаболит валацикловира, экскретируетея с грудным молоком. После назначения валацикловира в дозе 500 мг внутрь максимальная концентрация ацикловира (Сmах) в грудном молоке в 0,5-2,3 раза (в среднем в 1,4 раза) превышала соответствующие концентрации ацикловира в плазме матери. Отношение AUC ацикловира, находящегося в грудном молоке, к AUC ацикловира плазмы матери колебалось от 1,4 до 2,6 (среднее значение 2,2). Среднее значение концентрации ацикловира в грудном молоке составляло 2,24 мкг/мл (9,95 мкмоль/л). При приеме матерыо валацикловира в дозе 500 мг 2 раза в сутки ребенок подвергнется такому же воздействию ацикловира, как при приеме его внутрь в дозе около 0,61 мг/кг/сутки. Период полу выведения ацикловира из грудного молока такой же, как из плазмы крови. Валацикловир в неизмененном виде не определялся в плазме матери, грудном молоке или моче ребенка. В период грудного вскармливания применять только в случае, если предполагаемая польза для матери превышает потенциальный риск для ребенка. Применение и дозы Внутрь, независимо от приема пищи, таблетки следует запивать водой. Лечение опоясывающего герпеса Взрослые: по 1000 мг 3 раза в сутки в течение 7 дней. Лечение инфекций, вызванных ВПГ Взрослые: по 500 мг 2 раза в сутки в течении 5 дней. В более тяжелых первичных случаях лечение следует начинать как можно раньше, а его продолжительность должна быть увеличена с 5 до 10 дней. В случае рецидивов лечение должно продолжаться 3 или 5 дней, идеальным считается назначение валацикловира в продромальном периоде или сразу же после появления первых симптомов заболевания. В качестве альтернативы для лечения лабиального герпеса эффективно назначение валацикловира в дозе 2000 мг два раза в сутки. Вторая доза должна быть принята приблизительно через 12 часов (но не раньше, чем через 6 часов) после приема первой дозы. При использовании такого режима дозирования продолжительность лечения не должна превышать 1 дня, поскольку это, как было показано, не дает дополнительных клинических преимуществ. Терапия должна быть начата при появлении самых ранних симптомов лабиального герпеса (то есть пощипывание, зуд, жжение). Профилактика (супрессия) рецидивов инфекций, вызванных ВПГ Взрослые: у пациентов с сохраненным иммунитетом валацикловир назначается в дозе 500 мг один раз в сутки. У пациентов с очень частыми рецидивами (10 и более в год) дополнительного эффекта можно добиться при назначении валацикловира в суточной дозе 500 мг, разделенной на 2 приема (по 250 мг 2 раза в сутки). Для взрослых пациентов с иммунодефицитом рекомендованная доза валацикловира составляет 500 мг 2 раза в сутки. Продолжительность лечения 4-12 месяцев. Профилактика инфицирования генитальным герпесом здорового партнера Инфицированным взрослым с сохраненным иммунитетом и с числом обострений до 9 в год валацикловир следует принимать по 500 мг 1 раз в сутки в течение года и более, каждый день при регулярной половой жизни, при нерегулярных половых контактах прием валацикловира необходимо начинать за 3 дня до предполагаемого полового контакта. Данных о профилактике пациентов в других популяциях не существует. Профилактика ЦМВ-инфекции после трансплантации Взрослые и подростки в возрасте от 12 лет и старше: по 2000 мг 4 раза в сутки как можно раньше после трансплантации. Дозу следует снижать в зависимости от клиренса креатинина. Продолжительность курса лечения составляет 90 дней, но у больных с высоким риском лечение может быть более длительным. Особые группы пациентов Пациенты с нарушением функции почек Лечение опоясывающего герпеса и инфекций, вызываемых ВПГ, профилактика (супрессия) и снижение инфицирования здорового партнера. У таких пациентов необходимо поддерживать адекватную гидратацию. Дозу препарата Валацикловир Канон рекомендуется уменьшать у пациентов со значительным снижением функции почек (см. дозы при почечной недостаточности в таблице ниже). ТАБЛИЦЪ У пациентов, находящихся на гемодиализе, препарат Валацикловир Канон следует назначать после окончания сеанса гемодиализа. Необходимо часто определять клиренс креатинина, особенно в периоды, когда функция почек быстро меняется, например, сразу после трансплантации или приживления трансплантата, при этом доза препарата корректируется в соответствии с показателями клиренса креатинина. Пациенты с нарушением функции печени У пациентов со слабо и умеренно выраженным циррозом печени (синтетическая функция печени сохранена) корректировка дозы препарата Валацикловир Канон не требуется. Фармакокинетические данные у пациентов с тяжелым циррозом печени (с нарушением синтетической функции печени и наличием шунтов между портальной системой и общим сосудистым руслом) также не свидетельствуют о необходимости корректировать дозу препарата, однако, опыт его клинического применения при данной патологии ограничен. Дети в возрасте до 12 лет. Нет данных о применении валацикловира у детей. Пациенты пожилого возраста Коррекции дозы не требуется, за исключением значительного нарушения функции почек. Необходимо поддерживать адекватный водно-электролитный баланс. Побочные эффекты и передозировка Побочные эффекты: Нежелательные реакции перечислены ниже в соответствии с классификацией по основным системам и органам и по частоте возникновения. Классификация ВОЗ частоты развития побочных эффектов:очень часто 1/10 назначений (>:10%)часто от 1/100 до <: 1/10 назначений (>:1% и <:10%) нечасто от 1/1000 до <:1/100 назначений (>:0.1% и <:1%)редко от 1/10000 до <:1/1000 назначений (>:0.01% и <:0.1%)очень редко <:1/10000 назначений (<:0.01%)частота неизвестна по имеющимся данным установить частоту возникновения не представляется возможным. Инфекционные и паразитарные заболевания Частота неизвестна: инфекции дыхательных путей. Нарушения со стороны крови и лимфатической системы. Очень редко: лейкопения, тромбоцитопения. В основном лейкопения былаотмечена у больных со сниженным иммунитетом. Частота неизвестна: нейтропения, апластическая анемия, лейкопластический васкулит, тромбоцитопеническая пурпура. Нарушения со стороны иммунной системы Очень редко: анафилаксия. Нарушения психики. Нечасто: ажитация, включая агрессивное поведение. Редко: галлюцинации. Очень редко: психотические симптомы, включаю манию, депрессия. Нарушения со стороны нервной системы и психики Редко: головокружение, спутанность сознания, снижение умственныхспособностей, угнетение сознания. Очень редко:возбуждение, тремор, атаксия, дизартрия, судороги,энцефалопатия, кома. Нарушения со стороны органа зрения Частота неизвестна: нарушение зрение. Нарушения со стороны органа слуха и лабиринтные нарушения Частота неизвестна: назофарингит, ринорея. Нарушения со стороны дыхательной системы, органов грудной клетки и средостения. Нечасто: одышка. Нарушения со стороны сердца Частота неизвестна: тахикардия. Нарушения со стороны сосудов. Частота неизвестна: повышение артериального давления. Нарушения со стороны желудочно-кишечного тракта. Часто: тошнота. Редко: дискомфорт в животе, рвота, диарея. Нарушения со стороны печени и желчевыводящих путей. Очень редко: обратимые нарушения функциональных печеночных тестов, которые иногда расценивают как проявления гепатита. Нарушения со стороны кожи и подкожных тканей. Нечасто: высыпания, включая проявления фоточувствительности. Редко: зуд. Очень редко: крапивница, ангионевротический отек. Частота неизвестна: многоформная эритема. Нарушения со стороны скелетно-мышечной и соединительной ткани Частота неизвестна: артралгии. Нарушения со стороны почек и мочевыводящих путей Редко: нарушения функции почек. Очень редко: острая почечная недостаточность, почечная колика (может быть связана с нарушением функции почек). Частота неизвестна: осаждение кристаллов ацикловира в просвете почечных канальцев (необходимо соблюдать адекватный питьевой режим во время лечения), гематурия (часто связанная с другими нарушениями со стороны почек). Нарушения со стороны половых органов и молочной железы Частота неизвестна: дисменорея. Лабораторные и инструментальные данные. Очень редко: обратимое повышение функциональных печеночных проб, повышение концентрации билирубина. Частота не известна: снижение гемоглобина, гиперкреатининемия. Общие расстройства и нарушения в месте введения. Частота не известна: утомляемость, лихорадка (у детей), дегидратация. ПрочиеУ больных с тяжелыми нарушениями иммунитета, особенно у пациентов с далеко зашедшей стадией СПИДа, получающих высокие дозы валацикловира (8000 мг ежедневно) в течение длительного периода времени, наблюдались случаи почечной недостаточности, микроангиопатической гемолитической анемии и тромбоцитопении (иногда в комбинации). Подобные осложнения были отмечены у пациентов с такими же заболеваниями, но не получающих валацикловир. Передозировка: Симптомы и признаки: острая почечная недостаточность и неврологические нарушения, включая спутанность сознания, галлюцинации, ажитацию, угнетение сознания и кому, а также тошнота и рвота наблюдались у пациентов, получивших дозы валацикловира, превышающие рекомендованные. Подобные состояния чаще отмечались у пациентов с нарушением функции почек и у пациентов пожилого возраста, получивших повторные, превышающие рекомендованные дозы валацикловира, вследствие несоблюдения режима дозирования. Лечение: пациенты должны находиться под тщательным наблюдением для выявления признаков токсического действия. Гемодиализ значительно усиливает удаление ацикловира из крови и может считаться методом выбора при ведении пациентов с передозировкой валацикловира. Взаимодействие с другими ЛС: Клинически значимые взаимодействия не установлены. Ацикловир выводится почками в основном в неизмененном виде, активно секретируясь в почечные канальца. После назначения 1000 мг валацикловира, циметидин и пробенецид, блокируя канальцевую секрецию, повышают AUC ацикловира и снижают его почечный клиренс. Однако эта доза валацикловира не требует никакой коррекции из-за широкого терапевтического индекса ацикловира. Необходимо соблюдать осторожность в случае одновременного применения валацикловира в более высоких дозах (4000 мг в сутки и более) и лекарственных препаратов, которые конкурируют с ацикловиром за путь элиминации, так как существует потенциальная угроза повышения в плазме концентрации одного или обоих препаратов или их метаболитов. Было отмечено повышение AUC ацикловира и неактивного метаболита микофеиолата мофетила, иммуносупрессивного препарата, применяемого при трансплантации, при одновременном применении этих препаратов. Необходимо также соблюдать осторожность (мониторинг функции почек) при одновременном применении валацикловира, в частности, у пациентов, с нарушением функции почек или при приеме более высоких дозах (4000 мг в сутки и выше), а так же в сочетании с нефротоксичными препаратами в том числе аминогликлазидами, органическими соединениями платины, йодированным контрастным веществом, метотрексатом, пентамидииом, фоскарнетом, циклоспорином и такролимусом. Фармакологическое действие и фармакокинетика В организме человека валацикловир быстро и полностью превращается в ацикловир под воздействием фермента валацикловиргидролазы. Ацикловир обладает in vitro специфической ингибирующей активностью против вирусов: вирус простого герпеса (ВПГ) 1-го и 2-го типов, вирус ветряной оспы и опоясывающего герпеса (ВЗВ - варицелла зостер вирус), Цитомегаловирус (ЦМВ), вирус Эпштейна-Барр (ВЭБ), вирус герпеса человека 6-го типа. Ацикловир ингибирует синтез вирусной ДНК сразу после фосфорилировапия и превращения в активную форму трифосфат ацикловира. Первая стадия фосфорилировапия требует активности вирус специфических ферментов. Для ВПГ, ВЗВ, ВЭБ таким ферментом является вирусная тимидинкииаза, которая присутствует в пораженных вирусом клетках. Частичная селективность фосфорилировапия сохраняется у цитомегаловируса и опосредуется через продукт гена фосфотрансферазы UL 97. Активация ацикловира специфическим вирусным ферментом в огромной степени объясняет его селективность. Процесс фосфорилирования ацикловира (превращение из моно- в трифосфат) завершается клеточными киназами. Ацикловир трифосфат нуклеозида встраивается в вирусную ДНК, что приводит к облигатному разрыву цепи, прекращению синтеза ДНК и, следовательно, к блокированию репликации вируса. У пациентов с сохраненным иммунитетом ВПГ и ВЗВ с пониженной чувствительностью к валацикловиру встречаются крайне редко, но иногда могут быть обнаружены у пациентов с тяжелым нарушением иммунитета, например, у пациентов с трансплантатом костного мозга, у получающих химиотерапию по поводу злокачественных новообразований и у ВИЧ- инфицированных. Резистентность обычно обусловлена дефицитом тимидинкиназы, что приводит к чрезмерному распространению вируса в организме хозяина. Иногда снижение чувствительности к ацикловиру обусловлено появлением штаммов вируса с нарушением структуры вирусной тимидинкиназы или ДНК- полимеразы. Вирулентность этих разновидностей вируса напоминает таковую у его дикого штамма. Фармакокинетика: Общие сведения После приема внутрь валацикловир хорошо всасывается из желудочно-кишечного тракта. При участии фермента печени валацикловиргидралазы быстро и почти полностью превращается в ацикловир и валин. После однократного приема валацикловира в дозе 250-2000 мг средняя максимальная концентрация ацикловира в плазме у здоровых добровольцев с нормальной функцией почек составляет 10-37 мкмоль (2.2 - 8.3 мкг/мл), а медиана времени достижения этой концентрации 1-2 часа. При приеме валацикловира в дозе от 1000 мг биодоступность ацикловира равна 54 % и не зависит от приема пищи. Максимальная концентрация валацикловира в плазме составляет лишь 4 % от концентрации ацикловира, среднее время достижения максимальной концентрации - 30-100 минут после приема дозы, предел количественного определения валацикловира в плазме достигается через 3 часа либо раньше. Валацикловир и ацикловир имеют аналогичные фармакокинетические параметры после приема внутрь. Распределение Степень связывания валацикловира с белками плазмы очень низка (всего 15 %). Выведение У пациентов с нормальной функцией почек период полувыведения ацикловира из плазмы после приема валацикловира составляет около 3 часов. Валацикловир выводится из организма с мочой преимущественно в виде ацикловира (более 80 % дозы) и метаболита ацикловира 9-карбоксиметоксиметилгуанина, в неизмененном виде элиминируется менее 1 % препарата. Особые группы пациентов У пациентов с конечной стадией почечной недостаточности средний период полувыведения составляет около 14 часов. Характеристики пациентов Фармакокинетика валацикловира и ацикловира в значительной степени не нарушается у пациентов, инфицированных вирусами ВПГ и ВЗВ. На поздних сроках беременности устойчивый суточный показатель "площадь под кривой "концентрация-время" (AUC) после приема 1000 мг валацикловира был больше приблизительно в 2 раза, чем таковой при приеме ацикловира в дозе 1200 мг в сутки. Прием валацикловира в дозе 1000 мг или 2000 мг не нарушает диспозицию и фармакокинетические показатели валацикловира у ВИЧ-инфицированных пациентов по сравнению со здоровыми лицами. У реципиентов трансплантатов органов, получающих валацикловир в дозе 2000 мг 4 раза в сутки, пик концентрации ацикловира равен или превосходит таковой у здоровых добровольцев, получающих такую же дозу препарата, а суточные показатели AUC у них значительно выше. Особые указания Прием препарата в высоких дозах в течение длительного времени при состояниях, сопровождающихся выраженным иммунодефицитом (трансплантация костного мозга, клинически выраженные формы ВИЧ- инфекции, трансплантация почки), приводили к развитию тромбоцитопенической пурпуры и гемолитико-уремическому синдрому вплоть до летального исхода. При возникновении побочных эффектов со стороны центральной нервной системы (в т.ч. ажитации, галлюцинаций, спутанности сознания, бреда, судорог и энцефалопатии) препарат отменяют. Пациентам с риском дегидратации, особенно пациентам пожилого возраста, в период лечения валацикловиром необходимо обеспечить адекватную гидратацию организма. У пациентов с почечной недостаточностью имеется повышенный риск развития неврологических осложнений. При нарушениях функции печени у пациентов со слабо или умеренно выраженным циррозом печени коррекция дозы не требуется. Нет данных о применении валацикловира в более высоких дозах (4000 мг в сутки и более) у пациентов с заболеваниями печени, поэтому высокие дозы валацикловира им должны назначаться с осторожностью. Специальные исследования по изучению действия валацикловира при пересадке печени не проводились. Однако было показано, что профилактическое внутривенное назначение ацикловира в высоких дозах редуцирует ЦМВ-инфекцию. Супрессивная терапия валацикловиром снижает риск передачи генитального герпеса, но не исключает его полностью и не приводит к полному излечению. Терапия валацикловиром рекомендуется в сочетании с безопасным сексом. Влияние на способность управлять транспортными средствами: Необходимо учитывать клиническое состояние пациента и профиль побочных реакций валацикловира при оценке способности пациента управлять автотранспортом или другими механизмами, требующими быстроты психомоторных реакций. Условия хранения и отпуска из аптек Условия хранения:В сухом, защищенном от света месте при температуре не выше 25 °С. Хранить в недоступном для детей месте. Отпуск из аптек: По рецепту Регистрационные данные Торговое название Валацикловир Канон Международное непатентованное название:Валацикловир. Форма выпуска:таблетки, покрытые пленочной оболочкой . Состав:1 таблетка, покрытая пленочной оболочкой, содержит: активное вещество: валацикловира гидрохлорид 556,2 мг, в пересчете на валацикловир 500 мг: вспомогательные вещества: крахмал кукурузный 56,8 мг, кремния диоксид коллоидный 2 мг, кроскармеллоза натрия 29 мг, магния стеарат 4 мг, целлюлоза микрокристаллическая 72 мг: состав пленочной оболочки: Опадрай II белый 22 мг, в том числе: поливиниловый спирт 10,32 мг, макрогол (полиэтиленгликоль) 5,19 мг, тальк 3,83 мг, титана диоксид 2,66 мг. АТХ: Регистрация: Лекарственное средство ЛП-002013 Фармгруппа: Противовирусное средство. Дата регистрации: 26.02.2013 / 20.04.2015. Окончание регстрации: . Описание:Овальные двояковыпуклые таблетки с риской, покрытые пленочной оболочкой белого или почти белого цвета. На поперечном разрезе ядро почти белого цвета. Упаковка:Таблетки, покрытые пленочной оболочкой, 500 мг. По 7, 10, 14, 15 таблеток в контурную ячейковую упаковку из пленки поливинилхлоридной или пленки Г1ВХ/ПВДХ или пленки ПВХ/ПХТФЭ и фольги алюминиевой печатной лакированной. По 1, 2, 3, 6 контурных ячейковых упаковок по 7 таблеток или по 1, 2, 3, 6 контурных ячейковых упаковок по 10 таблеток, или по 1,3 контурных ячейковых упаковки по 14 таблеток, или по 2, 4 контурных ячейковых упаковки по 15 таблеток вместе с инструкцией по применению помещают в пачку из картона. Срок годности:2 года. Не применять по истечении срока годности. Владелец рег.удостоверения:КАНОНФАРМА ПРОДАКШН, ЗАО Производитель:КАНОНФАРМА ПРОДАКШН, ЗАО. Представительство

Модель:
RUR 540
BLanx® Med Intensive Stain Removal (Зубная паста Интенсивное удаление пятен) - лечебно-профилактическая и отбеливающая зубная паста для удаления пигментированного налета от табака, кофе, красного вина и других красящих продуктов. Внешний вид и свойства: пастообразная, белый цвет, освежающий запах, вкус нейтральный. Blanx Med Intensive Stain Removal осветляет эмаль благодаря уникальному компоненту - экстракту Цетрарии Исландской (арктического мха)Формула BlanX Med Intensive Stain Removal основана на натуральных компонентах - концентрированном арктическом лишайнике Cetraria Islandica и северо-европейском лишайнике Usnea Barbata, а также содержит низко-плотные полимерные микросферы. Эти ингредиенты обеспечивают выраженный очищающий и отбеливающий эффект пасты. Уникальный компонент пасты - экстракт Цетрарии Исландской, который входит в состав полирующих микрогранул. Высокая очищающая способность этих микрогранул сочетается с низким уровнем абразивности. Отбеливающее действие экстракта Цетрарии Исландской заключается в выделении атомарного кислорода, который устраняет не только поверхностные, но и глубоко въевшиеся пигменты. Экстракт Цетрарии Исландской обладает также противовоспалительным и противомикробным действием. Он препятствует размножению бактерий Streptococcus Mutants, которые являются основной причиной кариеса и воспалительных заболеваний десен. Другой активный компонент пасты - микропорошок бамбука, обладающий абсорбирующим свойством. Он усиливает отбеливающее действие пасты, эффективно очищая эмаль от пигментного налета.В качестве вспомогательного реминерализирующего вещества, в состав зубной пасты BlanX Med Intensive Stain Removal входит два разных соединения фтора:фторофосфат натрия (монофторфосфат) 0,4% и фторид натрия 0,08%. Атибактериальным компонентом служит натуральный заменитель сахара - ксилит. Уровень абразивности (RDA) - 39. Низкоабразивная. Паста содержит монофторфосфат натрия (528 ppm) и фторид натрия (362 ppm), которые способствуют профилактике кариеса. Результат: Белые зубы. Специальные особенности: Не содержит Хлоргексидин. Преимущества пасты Blanx Med Intensive Stain Removal-Восстанавливает естественную белизну эмали и блеск зубов-Избавляет от пигментных пятен благодаря мелкодисперсного порошка бамбука-Эффективно удаляет пятна, возникающие в результате курения и частом употреблении красящих напитков и пищи-Рекомендована при дисхромии эмали-Обладает антибактериальным эффектом-Благодаря низкой абразивности подходит для ежедневного использования-Не раздражает слизистую оболочку и сохраняет здоровую микрофлору полости рта

Модель:
RUR 680
Blanx Med Intensive Stain Removal - Зубная паста Интенсивное удаление пятен - особенно подходит тем, у кого зубной налет, а также тем кто много курит, пьёт чай, кофе или красное вино. Уникальная формула с арктическим лишайником, микропудрой бамбука и мягкими микрогранулами восстанавливает естественную белизну эмали. Инновационные активные ингредиенты борются с бактериями, которые являются причиной зубной дисхромии, появления зубного камня и кариеса, а также эффективно и бережно очищают и отбеливают зубную эмаль. Обладает низкой абразивностью и повышенным очищающим действием. Способ применения: Небольшое количество зубной пасты нанести на влажную щетину зубной щетки. Чистить зубы в течение 3-х мин круговыми движениями. Не глотать! После чистки рекомендуется сплюнуть излишки зубной пасты и ополоснуть полость рта небольшим количеством воды или ополаскивателя, задерживая его на 20-30 секунд. Рекомендуется к использованию 2 раза в день, а также после приема пищи. Объем: 75 мл

Модель:
RUR 1490
Мицеллярный гель очищает кожу, освежает и полностью удаляет макияж. Сочетание активных компонентов обеспечивает эффективное удаление макияжа даже для чувствительной кожи: мицеллы очищают кожу, захватывая жиры и загрязнения, а восстанавливающий пребиотик (сахар, питающий полезную кожную флору) помогает коже сохранить водный баланс. Гелевая текстура с очень освежающим ароматом делает кожу мягкой и чистой. Активные компоненты: Мицеллярный гель с пребиотиком и мицеллами глубоко очищает кожу и полностью снимает макияж. Восстанавливающий баланс пребиотик питает полезную микрофлору кожи и помогает поддерживать ее водный баланс. Мицеллы очищают кожу, захватывая жиры и загрязнения. Эффективность: • Мягко очищает кожу: 85%* женщин подтверждают • Сохраняет баланс: 88% женщин подтверждают • Смягчает кожу: 88%* женщин подтверждают * Самостоятельное тестирование эффективности проведено при участии 26 добровольцев, применявших средство 2 раза в день в течение 3 недель. Советы по применению: 1. Снимите макияж и очистите лицо мицеллярным очищающим гелем 2. Возьмите небольшое количество геля, нанесите средство на лицо и шею, помассируйте мицеллярный гель кончиками пальцев 3. Смойте чистой водой Наш совет: выполняя процедуру помассируйте лицо, чтобы активировать микроциркуляцию кожу

Модель:
RUR 1490
Мицеллярная вода марки Доктор Пьер Рико для снятия макияжа очищает кожу, освежает ее, делает контуры более четкими. Сочетание активных компонентов обеспечивает эффективное удаление макияжа даже для чувствительной кожи: мицеллы очищают кожу, захватывая жиры и загрязнения, а восстанавливающий пребиотик (сахар, питающий полезную кожную флору) помогает коже сохранить водный баланс. Свежая текстура без запаха идеально очищает кожу и готовит ее под средство по уходу. Активные компоненты: Мицеллярная вода, обогащенная восстанавливающими баланс пребиотиками и очищающими мицеллами, для идеального очищения и ощущения свежести на коже. Восстанавливающий баланс пребиотик питает полезную флору кожи и помогает ей поддерживать баланс. Мицеллы очищают кожу, удаляя излишки себума и загрязнения. Эффективность: • Восстановление баланса чувствительной кожи: 100%* женщин подтверждают Очищение кожи от загрязнений: 96%* женщин подтверждают *Самостоятельное тестирование эффективности с участием 24 добровольцев с применением 2 раза в день в течение 3 недель Советы по применению: 1. Нанесите мицеллярную воду с помощью ватного диска на все лицо и глаза и очищайе их, пока кожа не станет идеально чистой. Эта мицеллярная вода не требует смывания. 2. Теперь вы можете применить средства по уходу за кожей в соответствии с потребностями вашей кожи и для ее увлажнения. Маленький совет: не трите лицо ватным диском, т.к. это может вызвать раздражение кожи. Вместо этого слегка приложите ватный диск к коже, чтобы он впитал влагу, особенно вокруг глаз. Можно также использовать многоразовый ватный диск